Høydosebehandling med autolog stamcellestøtte – endelig et fremskritt ved myelomatose
Basert på artikkel publisert i Blood (11)
Myelomatose karakteriseres av infiltrerende vekst av maligne plasmaceller i beinmargen. Dette kan føre til destruksjon av beinvev, utvikling av osteolytiske lesjoner og spontanfrakturer. Hyperkalsemi, nyresvikt og infeksjoner er de viktigste komplikasjoner. Pasientene har ofte betydelig nedsatt livskvalitet, med redusert fysisk funksjonsevne, smerter og tretthet som de viktigste problemer (1). Insidensen er 5 – 6/100 000, med en lett overhyppighet hos menn (2). Median alder på diagnosetidspunktet er 70 – 71 år (2). Rapporter fra 1950- og 1960-årene, da man ikke hadde noen effektiv behandling, tydet på en median overlevelse på 7 – 8 måneder (3).
Tradisjonell cytostatikabehandling
Fra 1960-årene har melfalan (Alkeran) i kombinasjon med prednison, vanligvis gitt som fire dagers tablettkurer hver 4. – 6. uke, vært standardbehandling. Denne behandlingen, sammen med bedre og tidligere diagnostikk, har ført til en økning av den mediane overlevelse til ca. 30 måneder (4). I løpet av 1970- og 1980-årene ble det gjennomført en rekke randomiserte studier, blant annet en norsk (5), for å se om forskjellige kombinasjoner av cytostatika, ofte gitt intravenøst, var bedre enn melfalan + prednison. Dessverre var det ingen av disse regimene som gav noen klar forlengelse av overlevelsen, og en metaanalyse av 27 studier konkluderte med at kombinasjonskjemoterapi ikke var bedre enn melfalan + prednison (6). Melfalan og prednison er derfor fortsatt standardbehandling for pasienter som ikke er aktuelle for høydosebehandling med stamcellestøtte, mens kombinasjonskjemoterapi først og fremst brukes ved behandlingssvikt.
Interferon
Rundt 1990 kom det meddelelser som tydet på at subkutane injeksjoner av alfainterferon kunne forlenge overlevelsen. Det ble startet en rekke studier, blant annet i regi av Nordisk myelomatosestudiegruppe med deltakelse av de fleste norske sykehus (4). I forhold til den første entusiasmen var resultatene stort sett skuffende. Den nordiske studien viste en statistisk signifikant forlengelse av den såkalte platåfase på 5 – 6 måneder og en ikke-signifikant forlengelse av den mediane overlevelse på ca. tre måneder. En studie av livskvalitet og helseøkonomi knyttet til den nordiske studien viste at pasientenes livskvalitet var noe redusert under interferonbehandlingen, og at prisen for ett livskvalitetsjustert leveår (QALY) var så høy som 700 000 kroner (7). Av disse grunner har interferon en svært begrenset plass i behandlingen av myelomatose i de nordiske land, bortsett fra som vedlikeholdsbehandling etter høydosebehandling med stamcellestøtte.
Støttebehandling
Det har vært enkelte fremskritt i støttebehandlingen ved myelomatose i løpet av de siste årene. Nye antibiotika og antivirale midler og plasmaferese sammen med dialyse ved nyresvikt har bedret behandlingsmulighetene ved alvorlige komplikasjoner. Ved kronisk anemi hos pasienter med stabil sykdomstilstand for øvrig kan erytropoietinbehandling noen ganger gi gode resultater, men dette er meget kostbar behandling. Den forbedrede støttebehandlingen har imidlertid ikke på noen avgjørende måte innvirket på sykdommens prognose.
Bisfosfonater har en veldokumentert effekt ved hyperkalsemi. I løpet av 1990-årene ble det gjennomført flere studier for å se om regelmessig tilførsel av bisfosfonater kunne forebygge skjelettkomplikasjonene ved myelomatose. Peroral behandling med klodronat viste seg å ha en beskjeden effekt, mye på grunn av dårlig absorpsjon fra tarmen. I en randomisert studie der 90 mg pamidronat (Aredia) ble gitt intravenøst hver 4. uke i ni måneder, ble det imidlertid påvist en signifikant reduksjon i forekomst av skjelettkomplikasjoner (8). Pamidronat ved myelomatose er nå godkjent av Food and Drug Administration i USA og anbefales av det internasjonale fagmiljø, til tross for at resultatene ikke er bekreftet i noen ny placebokontrollert studie. Det hersker usikkerhet med hensyn til indikasjon, optimal dosering og behandlingsvarighet. Heller ikke er det gjort livskvalitetsstudier eller helseøkonomiske beregninger. Nordisk myelomatosestudiegruppe har nylig startet en randomisert studie som tar sikte på å besvare noen av disse spørsmålene.
Allogen stamcelletransplantasjon
Allogen stamcelletransplantasjon har vært gjennomført på enkelte yngre pasienter de siste årene. Mens dødeligheten knyttet til denne behandlingen i begynnelsen var 40 – 50 %, har omhyggelig utvelgelse av pasienter sammen med bedring av behandlingsmetodene redusert dødeligheten til under 20 %. Fordi behandlingen bare kan tilbys yngre pasienter med vevstypeforlikelig søsken, er den bare aktuell for en liten andel og har i Norge kun vært gitt til en håndfull pasienter. Langtidsoverlevelsen er ikke vist å være bedre enn ved høydosebehandling med autolog stamcellestøtte.
Høydosebehandling med autolog stamcellestøtte
Studier utført i begynnelsen av 1980-årene viste at en stor engangsdose melfalan intravenøst gav betydelig høyere responsfrekvens enn den vanlige perorale behandlingen. Dette gav imidlertid uttalt nøytropeni og trombocytopeni og tilsvarende høy behandlingsrelatert dødelighet. Det viste seg at beinmarg høstet tidlig under behandlingen og tilbakeført etter høydosebehandlingen kunne forkorte nøytropeni- og trombocytopenifasen og forebygge en del av disse komplikasjonene. En fransk randomisert studie publisert i 1996 viste at pasienter< 65 år som hadde fått høydosebehandling med etterfølgende tilbakeføring av autolog beinmarg hadde 15 måneder lengre median overlevelse enn pasienter som hadde fått vanlig cytostatikabehandling (9). Utover i 1990-årene ble metodene forbedret, og man fant at bruk av hematopoetiske stamceller høstet fra perifert blod etter stimulering med vekstfaktor både var enklere og mer effektivt enn beinmarg. I 1994 startet Nordisk myelomatosestudiegruppe en populasjonsbasert studie der pasienter< 60 år med nydiagnostisert og symptomgivende myelomatose ble tilbudt høydosebehandling med autolog stamcellestøtte dersom de hadde god respons på den innledende cytostatikabehandling. Studiens mål var å vurdere effekten av høydosebehandling på overlevelse og livskvalitet i et populasjonsbasert materiale, og å foreta en nytte-kostnad-analyse av en eventuell overlevelsesgevinst. Hensikten med denne artikkelen er å redegjøre for denne studien og å diskutere resultatene i forhold til annen aktuell behandling ved myelomatose.
Materiale og metode
Vi fant det umulig å foreta en randomisering mellom standardbehandling og høydosebehandling med autolog stamcellestøtte, fordi denne behandlingen allerede var kjent for pasientene fra massemediene og var i ferd med å bli tatt i bruk.
Det historiske kontrollmaterialet ble hentet fra fem nordiske populasjonsbaserte studier som ble gjennomført mellom 1970 og 1994. En av disse var fra daværende helseregion 1 i Norge (2). Til sammen 313 pasienter< 60 år med nydiagnostisert, behandlingstrengende myelomatose ble identifisert; av disse oppfylte 274 inklusjonskriteriene i HMAS-studien. Det betyr at de retrospektivt ble bedømt til å ha vært aktuelle for høydosebehandling med autolog stamcellestøtte, dersom denne behandlingsmuligheten hadde vært aktuell på det tidspunkt deres sykdom ble diagnostisert. Insidensen av myelomatose hos personer< 60 år i de fem studiene var nærmest identisk og svarte helt til den vi fant i HMAS-studien, nemlig en per 100 000, og median overlevelse var også meget lik i de fem studiene. Dette styrker kontrollmaterialets troverdighet. Det var ingen bedring av overlevelsen i perioden fra 1970 frem til begynnelsen av 1990-årene. Kontrollmaterialet er beskrevet i en egen artikkel (10).
I Nordisk myelomatosestudiegruppes studier blir alle pasienter med myelomatose innenfor opptaksområdet registrert, slik at vi kan vurdere hvor representativt pasientmaterialet er. I tillegg til at vi sammenliknet pasienter som var med i HMAS-studien med et tilsvarende pasientmateriale fra samme opptaksområde, kunne vi derfor også vurdere virkningen av HMAS-behandlingen på hele populasjonen av yngre myelomatosepasienter.
I studien deltok 14 universitetssykehus med tilhørende regioner i Danmark, Sverige og Norge, med et samlet befolkningsgrunnlag på 15 millioner. Hovedsekretariatet for studien var i Lund i Sverige.
Etter Nordisk myelomatosestudiegruppes protokoll ble behandlingen gitt i fire faser:
1. Induksjonsbehandling: vinkristin og adriamycin gitt intravenøst med infusjonspumpe over fire dager med tillegg av peroralt deksametason (VAD-behandling), tre kurer med fire ukers mellomrom. Forutsetningen for å gå videre til stamcellehøsting og høydosebehandling var objektiv respons på induksjonsbehandlingen. Begrunnelsen for dette var den antakelse at effekten av høydosebehandlingen ville være best hvis pasientens tumormasse var redusert så mye som mulig på forhånd.
2. Stamcellehøsting: Cyklofosfamid 4 g/m² som intravenøs bolusdose, granulocyttkolonistimulerende faktor subkutant fra dag 4, høsting ved cytaferese dag 11 – 12, nedfrysing av stamceller.
3. Høydosebehandling: melfalan 200 mg/m² som intravenøs bolus, stamcelleinfusjon etter 48 timer.
4. Vedlikeholdsbehandling: Interferon 3 – 5 millioner IE tre ganger per uke, start to måneder etter høydosebehandlingen hvis perifere blodverdier var tilfredsstillende. På den tiden da denne studien startet, forelå preliminære data fra en randomisert studie som tydet på at interferon gitt etter høydosebehandling med autolog stamcellestøtte forlenget totaloverlevelsen.
Resultater
Studien pågikk fra 1994 til 1998. Resultatene er publisert i tidsskriftet Blood i januar 2000 (11) og er også presentert i Läkartidningen (12). Til sammen ble det registrert 348 pasienter< 60 år med nydiagnostisert, behandlingstrengende myelomatose i løpet av inklusjonstiden. Av disse ble 274 inkludert i behandlingsstudien. De viktigste årsakene til at 74 pasienter ikke ble med i behandlingsstudien, var annen alvorlig sykdom, manglende ønske fra pasientens side, deltakelse i annen intensivbehandlingsprotokoll eller terminal sykdom. 214 av de 274 inkluderte pasientene har gjennomgått hele behandlingen til og med stamcelleinfusjonen. Av de 274 inkluderte pasientene oppnådde 77 % respons, der hovedkriteriet er reduksjon av M-komponenten med minst 50 %. 34 % oppnådde komplett respons, hvilket innebærer at M-komponenten forsvinner fullstendig. Disse tallene er vesentlig høyere enn ved konvensjonell behandling med melfalan og prednison.
Behandlingen var relativt lite toksisk. De fleste alvorlige komplikasjoner opptrådte under initialbehandlingen med vinkristin, adriamycin og deksametason. Av i alt ni behandlingsrelaterte dødsfall inntraff seks under VAD-behandlingen og tre i forbindelse med høydosebehandlingen.
Overlevelse
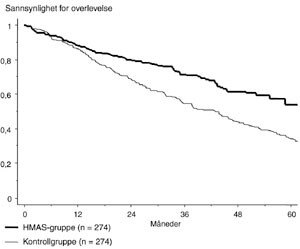
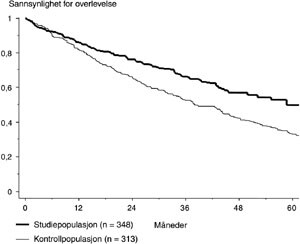
Ved presentasjonen av resultatene er samtlige 274 pasienter i behandlingsstudien tatt med, uansett om de fikk høydosebehandling med autolog stamcellestøtte eller ikke (analyse etter ”intention to treat”-prinsippet). Sammenlikning mellom de 274 HMAS-pasientene og kontrollgruppen på 274 historiske pasienter viste en høygradig signifikant forskjell i overlevelse, til fordel for høydosegruppen. Risikoratio for død var 1,65 (95 % konfidensintervall (KI) 1,28 – 2,14; p = 0,0001). Median overlevelse var 44 måneder i kontrollgruppen og 62 måneder i HMAS-gruppen (fig 1). Når vi sammenlikner overlevelsen for samtlige pasienter med behandlingstrengende myelomatose< 60 år i de to gruppene (348 mot 313) og altså inkluderer pasienter som av forskjellige grunner ikke var aktuelle for høydosebehandlingen, finner vi fortsatt en betydelig forskjell i overlevelse, med risikoratio 1,49 (95 % KI 1,20 – 1,86; p = 0,0004). Medianoverlevelsen i kontrollmaterialet var 38 måneder, og i studiegruppen, som inkluderte de høydosebehandlede, var den 59 måneder (fig 2).
På bakgrunn av kjente tall for insidens av myelomatose hos personer< 60 år og størrelsen på befolkningsgrunnlaget for kontrollmaterialet og HMAS-studien beregnet vi det forventede antall pasienter for inklusjonsperioden for de respektive studier. Vi fant at antall registrerte tilfelle for HMAS-studiens vedkommende utgjorde 77 % av det forventede antall pasienter, mens det tilsvarende tall for kontrollgruppen var 76 %. Dette innebærer at studiens resultat kan generaliseres til å gjelde hele populasjonen med myelomatosepasienter< 60 år. Til sammenlikning kan nevnes at vanlige inklusjonstall for studier i Storbritannia og USA er 5 – 15 % av det antall som kan forventes ut fra insidensen.
Helserelatert livskvalitet
Vi gjennomførte også en studie av helserelatert livskvalitet hos pasientene i HMAS-studien og sammenliknet denne med pasienter< 60 år som hadde fått konvensjonell peroral behandling med melfalan og prednison i en av Nordisk myelomatosestudiegruppes tidligere studier. I begge disse studiene ble kostnader og ressursbruk ved behandlingen registrert prospektivt, hvilket muliggjorde en nytte-kostnad-analyse av HMAS-behandlingen. Sekretariatet for livskvalitets- og helseøkonomistudien var ved Ullevål sykehus. Pasientene fylte ut EORTCs skjema for måling av helseregistrert livskvalitet (EORTC QLQ C-30) før behandlingsstart og etter en, seks, 12, 24 og 36 måneder. Under VAD-kurene og selve høydosebehandlingen, det vil si det første halve året av behandlingstiden, var livskvaliteten noe redusert i HMAS-gruppen. Både global livskvalitet, sosial funksjon og rollefunksjon var svekket sammenliknet med det kontrollpasientene oppgav (13). Dette er ikke så overraskende når man i tillegg til den kraftigere cytostatikabehandlingen tar i betraktning at HMAS-pasienten gjennomsnittlig tilbrakte 62 dager i sykehus det første halve året, mot bare 13 i kontrollgruppen. Etter det første året var det ingen statistisk signifikante forskjeller i helserelatert livskvalitet mellom gruppene, men etter 2 – 3 år var det en tendens til bedre skåre i HMAS-gruppen med henblikk på global livskvalitet og fysisk, sosial og emosjonell funksjon, samt mindre smerter og tretthet.
Nytte-kostnad-analyse
Forskjellen i gjennomsnittlig overlevelsen i de to gruppene ble estimert til 1,5 år. På bakgrunn av den noe reduserte livskvalitet det første halvåret av behandlingstiden beregnet vi behandlingens gevinst i form av såkalte livskvalitetsjusterte leveår (QALY = quality adjusted life years) til å være 1,2. Den helseøkonomiske beregningen viste at HMAS-behandlingen kostet 300 000 kroner mer enn den konvensjonelle behandling med melfalan og prednison. Prisen for ett vunnet livskvalitetsjustert leveår ble da ca. 250 000 kroner (26 000 amerikanske dollar) (14). En systematisk vurdering av premissene for denne nytte-kostnad-analysen (såkalt sensitivitetsanalyse) viste at prisen per QALY var spesielt påvirkelig av antall liggedøgn i sykehus og størrelsen på overlevelsesgevinsten. Hvis man sløyfet vedlikeholdsbehandlingen med interferon, ville prisen på ett livskvalitetsjustert leveår bli redusert med 4 200 amerikanske dollar, forutsatt at dette ikke påvirket overlevelsen. Interferonets rolle etter høydosebehandlingen er ikke avklart.
Diskusjon
Ettersom de involverte sykehusavdelinger får mer erfaring med behandlingen, kan en større del av den utføres poliklinisk. Det pågår systematisk forskning både i og utenfor Nordisk myelomatosestudiegruppe for å bedre behandlingsresultatene. Sannsynligvis vil derfor en fremtidig nytte-kostnad-analyse falle enda heldigere ut for dette behandlingsprinsippet. I internasjonal helseøkonomisk litteratur oppfattes ofte intervensjoner som koster mindre enn 50 000 amerikanske dollar som kostnadseffektive, mens helsetiltak med pris> 100 000 amerikanske dollar ansees som ikke-kostnadseffektive i forhold til alternative tiltak (15). Etter vår oppfatning er høydosebehandling med autolog stamcellestøtte til yngre myelomatosepasienter en nyttig investering for samfunnet. Helsetilsynets rådgivende gruppe for allogen stamcelletransplantasjon, der alle landets regionsykehus er representert, anser dette som etablert behandling i Norge. På bakgrunn av de positive resultatene med denne type høydosebehandling til pasienter< 60 år pågår det nå en fortsettelse av samme protokoll, med inklusjon av pasienter opp til 65 år. I denne protokollen er det tilstrekkelig at sykdommen stabiliseres under den første cytostatikabehandlingen, for at pasienten skal kunne gå videre til høsting av stamceller og til selve høydosebehandlingen. Dessverre vet vi ikke hva som er den beste behandlingen for pasienter som ikke når frem til høydosebehandlingen, eller for pasienter som får tilbakefall etter høydosebehandling.
Hittil har høydosebehandling med autolog stamcellestøtte i Norge vært finansiert ved en egen bevilgning fra Sosial- og helsedepartementet til utprøvende kreftbehandling. Fra år 2000 har dette vært gitt som en øremerket del av det statlige regionsykehustilskudd. Det er åpenbart at en så kostbar behandling ikke kan finansieres over det ordinære rammebudsjett. Derfor arbeides det for å få en egen DRG-basert finansiering av denne behandlingen.
Høydosebehandling med autolog stamcellestøtte representerer det første fremskrittet av betydning siden innføringen av melfalan-prednison-kurene i slutten av 1960-årene. Dessverre ser det ikke ut til at denne behandlingen har kurativt potensial. Før eller senere får pasientene tilbakefall. Det er to hovedårsaker til dette. Den ene er at selv høydosebehandlingen antakeligvis ikke er i stand til å utrydde alle maligne plasmaceller i kroppen. Den andre årsaken er at stamcellesuspensjonen inneholder celler tilhørende den maligne klon. Det forskes intenst på metoder til å selektere hematopoetiske stamceller og drepe tumorcellene i den høstede cellesuspensjonen. En viktig utfordring er også å finne bedre metoder til å vedlikeholde det behandlingssvaret man oppnår etter høydosebehandlingen.
Gjentatt høydosebehandling, såkalt dobbelt, autolog stamcelletransplantasjon, har ikke ført til noen avgjørende bedring av behandlingsresultatene.
Andre nye behandlingstilbud ved myelomatose
Thalidomid har vist seg å ha en hemmende effekt på enkelte tumorformer, blant annet myelomatose. Fase 2-studier, blant annet i regi av Nordisk myelomatosestudiegruppe, har vist at 30 – 40 % av pasientene får en objektiv respons. Preparatet har en del bivirkninger, og det er vanskelig å påvise noen bedring av pasientenes helserelaterte livskvalitet. Nordisk myelomatosestudiegruppe planlegger en randomisert undersøkelse av thalidomid som tillegg til melfalan og prednison ved nydiagnostisert myelomatose hos eldre pasienter.
En interessant utvikling innen transplantasjonsfeltet er de såkalte mini-allotransplantasjoner. Dette behandlingsprinsippet er under utprøving både ved maligne blodsykdommer og enkelte solide tumorformer. Det baseres på den erkjennelse at selve høydosebehandlingen er av mindre betydning for bekjempelse av tumorcellene enn den immunologiske giver-mot-tumor-effekt. Det gis en mindre intens forbehandling (kondisjonering) enn ved konvensjonelle allotransplantasjoner, men hematopoetiske stamceller fra donor overlever fordi det gis intens immunsuppressiv behandling etter transplantasjonen. De maligne cellene hos mottakeren skal bekjempes av lymfocytter fra giveren, eventuelt ved ytterligere tilførsel senere i forløpet. Kravet til vevstypeforlikelighet mellom giver og mottaker er det samme som ved ordinære allogene stamcelletransplantasjoner.
Et alternativ til å bruke donorlymfocytter til å bekjempe de maligne plasmacellene er å ruste opp pasientens eget immunforsvar ved en vaksinasjon. Den M-komponenten som utskilles av plasmacellene, kan ansees som et tumorspesifikt antigen og brukes til vaksinasjon av pasienten. Best resultater oppnås hvis antigenet presenteres via såkalte dendrittiske (antigenpresenterende) celler. Behandlingen er foreløpig eksperimentell, men gir løfter om at immunologisk behandling kan bli en realitet i fremtiden.
Konklusjon
Høydosebehandling med autolog stamcellestøtte er det første reelle fremskritt i behandlingen av myelomatose siden innføring av sykliske kurer med melfalan og prednison i 1960-årene. Gitt til pasienter< 60 år i en nordisk populasjonsbasert studie med meget høy deltakelse oppnådde man en forlengelse av den mediane overlevelse med halvannet år. Bortsett fra en moderat nedsettelse av livskvaliteten i forbindelse med induksjonskurer og selve høydosebehandlingen hadde pasientene god livskvalitet. Nytte-kostnad-analyse gav et akseptabelt resultat, og behandlingen er nå etablert som rutine ved alle norske regionsykehus. Studien er et eksempel på at nytteverdien av nye behandlingsmetoder bør dokumenteres ved populasjonsbaserte kliniske studier med integrert livskvalitets- og nytte-kostnad-analyse. Utprøvende behandling bør finansieres ved særskilte bevilgninger til veldefinerte prosjekter. Hvis behandlingen viser seg å være kostnadseffektiv, bør den deretter skaffes økonomisk basis via innsatsstyrt finansiering og egen DRG.
- 1.
Wisløff F, Eika S, Hippe E, Hjorth M, Holmberg E, Kaasa S et al. Measurement of health-related quality of life in multiple myeloma. Br J Haematol 1996; 92: 604 – 13.
- 2.
Wisløff F, Andersen P, Andersson TR, Brandt E, Eika C, Fjæstad K et al. Has the incidence of multiple myeloma in old age been underestimated? The myeloma project of health region I in Norway. Eur J Haematol 1991; 47: 333 – 7.
- 3.
Kyle RA, Bayrd ED. The monoclonal gammopathies: multiple myeloma and related cell disorders. Springfield, IL: Charles C. Thomas, 1976.
- 4.
The Nordic Myeloma Study Group. Interferon- α 2b added to melphalan-prednisone for initial and maintenance therapy in multiple myeloma. A randomized, controlled trial. Ann Intern Med 1996; 124: 212 – 22.
- 5.
Kildahl-Andersen O, Bjark P, Bondevik A, Bull O, Burgess G, Dehli O et al. Multiple myeloma in central Norway 1981 – 1982: A randomized trial of 5-drug combination therapy versus standard therapy. Scandinavian Journal of Haematology 1986; 37: 243 – 8.
- 6.
The Myeloma Trialists’ Collaborative Group. Combination chemotherapy versus Melphalan plus Prednisone as treatment for multiple myeloma: an Overview of 6,633 Patients from 27 randomized Trials. J Clin Oncol 1998; 16: 3832 – 42.
- 7.
Nord E, Wisløff F, Hjorth M, Westin J. Cost-utility analysis of melphalan-prednisone versus melphalan-prednisone + interferon in newly diagnosed multiple myeloma. Results from a randomized controlled trial. Pharmacoeconomics 1997; 12: 89 – 103.
- 8.
Berenson J, Lichtenstein A, Porter L, Dimoupolos M, Bordoni R, George S et al. Efficacy of pamidronate in reducing skeletal events in patients with advanced multiple myeloma. N Engl J Med 1996; 334: 488 – 93.
- 9.
Attal M, Harousseau JL, Stoppa AM, Sotto JJ, Fuzibet JG, Rossi JF et al. A prospective, randomized trial of autologous bone marrow transplantation and chemotherapy in multiple myeloma. N Engl J Med 1996; 335: 91 – 7.
- 10.
Hjorth M, Holmberg E, Rødjer S, Turesson I, Westin J, Wisløff F. Survival in conventionally treated younger (<60 years) multiple myeloma patients: no improvement during two decades. Eur J Haematol 1999; 62: 271 – 7.
- 11.
Lenhoff S, Hjorth M, Holmberg E, Turesson I, Westin J, Lanng Nielsen J et al. Impact on survival of high-dose therapy with autologous stem cell support in patients younger than 60 years with newly diagnosed multiple myeloma: a population-based study. Blood 2000; 95: 7 – 11.
- 12.
Hjorth M, Lenhoff S, Turesson I, Westin J. Högdos melfalan med stamcellsstöd nu etablerad terapi vid myelom. Läkartidningen 2000; 97: 4585 – 92.
- 13.
Gulbrandsen N, Wisløff F, Westin J, for the Nordic Myeloma Study Group. Health-related quality-of-life in multiple myeloma patients receiving high dose chemotherapy with autologous blood stem cell support. Medical Oncology, under trykning.
- 14.
Gulbrandsen N, Wisløff F, Nord E, Lenhoff S, Hjorth M, Westin J for the Nordic Myeloma Study Group. Cost-utility analysis of high dose melphalan with autologous stem cell support vs. melphalan plus prednisone in patients younger than 60 years with multiple myeloma. Eur J Haematol 2001; 60: 328 – 36.
- 15.
Laupacis A, Feeny D, Detsky AS,Tugwell PX. How attractive does a new technology have to be to warrant adoption and utilization? Tentative guidelines for using clinical and economic evaluations. Can Med Assoc J 1992; 146: 473 – 81.