Background.
Pain assessment in nursing home patients is often challenging because of cognitive failure. Demented patients receive less optimal pain treatment than those who are cognitively intact. Inappropriate pain assessment is likely to be an important reason for problems with proper diagnosis and treatment of pain in the cognitively impaired. Self-report of pain by standardized questionnaires is recommended for those with mild cognitive failure. For those who are unable to self-report, observational assessment is an alternative.
Materials and methods.
Structured pain assessment tools are reviewed, with emphasis on their feasibility in cognitively impaired patients.
Results.
Several assessment tools for observational pain assessment are available, but none of them is satisfactory validated. Observational tools are used by a trained observer who rates behaviour indicative of pain according to pre-defined clues. The Checklist of Non-verbal Pain Indicators (CNPI) and the Doloplus-2 are both observational tools that are translated into Norwegian. The Norwegian CNPI is in an early phase of validation, while the Doloplus-2 is tested in a Norwegian pilot validation study with promising results.
Interpretation.
It is important to establish a common standard for systematic pain assessment in the cognitively impaired, both clinically and in research. Further validation of the CNPI and the Doloplus-2 is recommended.
Eldre rapporterer mindre smerter enn yngre (1). Dette kan ha mange årsaker, som frykt for innleggelse i sykehus, frykt for avvisning, oppfatninger om at smerte er et uunngåelig normalfenomen og at det er uakseptabelt å vise at man har vondt (2). Kommunikasjonsbegrensninger som svekket hørsel, syn eller taleevne er vanlige problemer blant eldre (3), noe som kompliserer rapportering av subjektive symptomer.
Smerte er generelt underdiagnostisert blant somatisk syke pasienter, i hovedsak fordi legen ikke gjør en systematisk anamnese og smertediagnostikk (4). Antakelig er dette problemet enda større på sykehjem hvor den diagnostiske intensiteten er lavere. 60 – 80 % av sykehjemspasienter har smerter (5). Diagnostikk av subjektive symptomer som smerte er en stor utfordring i sykehjem, fordi 50 – 70 % av pasientene har ulike former for kognitiv svikt (6). Pasienter med demens får mindre smertestillende medisiner enn de som ikke er demente (7).
Ulike former for kognitiv svikt kan endre smerteopplevelsen; for eksempel hevdes det ut fra et nevrofysiologisk synspunkt at pasienter med Alzheimers sykdom kan ha mindre smerter enn andre, mens pasienter med vaskulær demens og de Creutzfeldt-Jakobs sykdom kan få økt smerteopplevelse (8). Ved å måle blodtrykk, puls og respirasjonsfrekvens før og etter venepunksjon vet man at pasienter med kognitiv svikt reagerer først etter at smerten er et faktum – og ikke før selve venepunksjonen, slik kognitivt intakte gjør (1). Dette tyder på en endret smerteforventning. Hver gang smerte oppstår, vil pasienten kunne føle frykt og overraskelse, som igjen kan bidra til å gjøre opplevelsen mer traumatisk.
Helsepersonell stiller seg ofte kritisk til rapporter fra de eldre, både når det gjelder smerteintensitet og hyppighet av smerte (9). Dette gjelder spesielt dersom pasienten har kognitiv svikt (10). Helsepersonellets evne til å gjenkjenne smerte hos demente er heller ikke tilfredsstillende (9). Samlet taler dette for å kartlegge subjektive symptomer som smerte på en systematisk, målrettet måte og ved bruk av validerte måleverktøy i denne pasientgruppen.
Målemetoder
Siden smerte er et subjektivt fenomen, anbefales vanligvis måleinstrumenter som pasienten fyller ut selv, slik som visuell analog skala og numerisk rangeringsskala (11). Selvrapporteringsmetoder har lavere validitet hos demente enn hos ikke-demente pasienter (12). Likevel ser det ut til at pasienter med lettere grad av kognitiv svikt er i stand til å bruke minst ett av de anerkjente selvrapporteringsinstrumentene, og derfor bør få prøve slike (13). For å kunne benytte seg av selvrapporteringsmetoder, er pasienten avhengig av å forstå oppgaven som skal utføres, trekke ut meningen av det språklige innholdet og å abstrahere smerteopplevelsen slik at den kan settes inn i en ny dimensjon (fra subjektiv følelse til et tall på et papir). Redusert kognitiv funksjon kan påvirke alle trinn av denne kompliserte mentale oppgaven.
De fleste selvrapporteringsmetoder bruker verst tenkelige smerte som referanse. Det krever en viss evne til å huske tidligere opplevd smerte og har lav reliabilitet blant eldre med kognitiv svikt (6). Det kan derfor være mer hensiktsmessig å benytte metoder som spør om smerteintensiteten her og nå. Dette er også i tråd med nyere generelle anbefalinger. Dersom man ønsker å vurdere endringer over tid, bør man heller designe studien prospektivt med gjentatte målinger av intensiteten her og nå. Pasienter med kognitiv svikt vil ofte ikke huske variasjon av smerte over tid.
Observasjonsbaserte smertemålingsmetoder
Ved mer omfattende kognitiv svikt er det nødvendig å bruke andre metoder for å måle smerte og andre subjektive symptomer. Et alternativ til selvrapportering er å observere pasientens atferd for å se etter tegn som kan tyde på smerte (14). Dette bør gjøres av en som kjenner pasienten. Endring i ansiktsuttrykk, væremåte, sosial omgang, verbale uttrykk, interpersonell aktivitet, mobilitet, generell aktivitet og mental status kan alle være uttrykk for smerte (ramme 1) (15).
Eksempler på atferdsbaserte smerteindikatorer (15)
-
Ansiktsuttrykk: pannerynking, trist eller skremt, rask blunking
-
Verbale uttrykk: støyende pusting, messing/synging, utrop, banning, bruk av «grove» ord
-
Bevegelse: uro, vimsing, agitasjon, økt vandring, vugging, endret ganglag eller holdning
-
Endring i interpersonell aktivitet: motsetter seg pleie, har forstyrrende/voldelig atferd, tilbaketrekking
-
Endring i aktivitetsmønster: nekter å spise, hviler lenger enn vanlig, søvnløshet, plutselig stans i normale rutiner eller aktiviteter
-
Endring i mental status: økt forvirring, irritabilitet, gråt
Eldre med kognitiv svikt kan se ut til å ha flere atferdstrekk som indikerer smerte enn personer uten kognitiv svikt (16). Særlig gjelder dette ansiktsuttrykk, som regnes som et av de sikreste tegnene (1, 17, 18).
Atferdsregistrering bør gjøres av en trent observatør og følge en systematikk ved at man observerer kjente tegn som skissert ovenfor og nedtegner funnene i pasientens journal eller kurve. Det bør benyttes standardiserte målemetoder, og ideelt sett burde man blitt enige om et felles system for bruk ved alle sykehjem i Norge.
På verdensbasis finnes flere metoder for atferdsbasert smerteregistrering. Noen av disse er presentert i tabell 1 (17) – (24). To skalaer som er oversatt til norsk og under pågående validering for norske forhold vil bli omtalt i mer detalj.
Tabell 1
Internasjonalt publiserte observasjonsbaserte smertemålingsinstrumenter med vurdering av egnethet for klinisk og vitenskapelig bruk
| Instrument | Antall spørsmål | Klinisk bruk | Forskning |
| Videofilming | – | Ikke anbefalt | Kan brukes |
| The discomfort scale-dementia of the Alzheimer’s type (DS-DAT) (19) | 9 | Ikke anbefalt | Kan brukes, men ikke smertespesifikk |
| Checklist of nonverbal pain indicators (CNPI) (18) | 6 | Kan brukes ved akutte smerter | Ikke anbefalt |
| The pain assessment in advanced dementia scale (PAINAD) (20) | 5 | Kan brukes, men lav sensitivitet | Ikke anbefalt |
| The pain assessment scale for seniors with severe dementia (PACSLAC) (17) | 60 | Kan brukes | Ikke anbefalt |
| The pain assessment for the dementing elderly (PADE) (21) | 24 | Ikke anbefalt | Ikke anbefalt |
| The non-communicative patient’s pain assessment instrument (NOPPAIN) (22) | 16 + kart og termometer | Ikke anbefalt | Ikke anbefalt |
| The Abbey pain scale (The Abbey) (23) | 6 | Ikke anbefalt | Ikke anbefalt |
| Doloplus-2 (24) | 10 | Kan brukes | Ikke anbefalt |
Checklist of nonverbal pain indicators (CNPI) består av seks punkter som skåres i ro og i bevegelse med enten ja eller nei (18). Punktene omfatter verbale smerteutsagn (ord og lyder), ansiktsuttrykk og beskyttelse av smertefulle områder. Endring i interpersonell aktivitet og aktivitetsmønster er å anse som mer uspesifikke tegn på smerte og er ikke med i dette skjemaet. Til tross for gode instruksjoner i bruk av CNPI, foreligger ingen data om hvordan resultatene skal tolkes og dermed kunne settes inn i en klinisk sammenheng. Skalaen er testet ut på demente pasienter med lårhalsbrudd, men flere valideringsstudier er ønskelig. CNPI er oversatt til norsk, og den første fase av valideringen er gjennomført i sykehjem (25). En mer detaljert validering av den norske versjonen er nødvendig før videre anbefalninger kan gis.
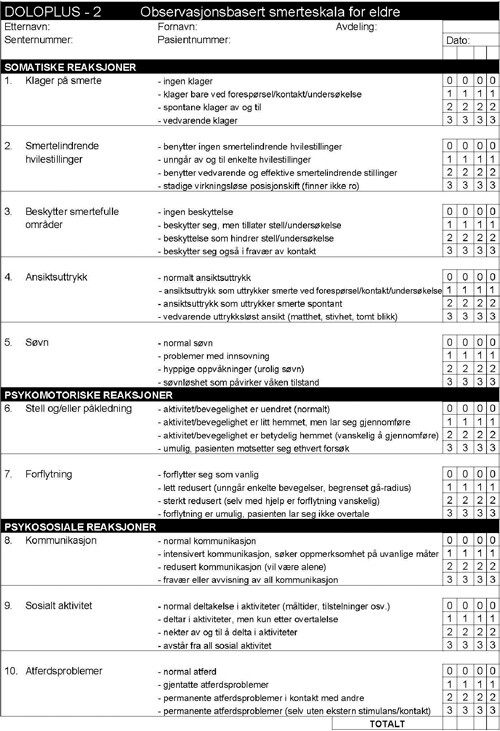
Doloplus-2 er opprinnelig et fransk instrument for måling av kroniske smerter hos eldre uten evne til verbal kommunikasjon (24), og er i utstrakt klinisk bruk i den fransktalende delen av Europa (26). Skalaen består av ti punkter, som er gruppert i tre områder; somatikk (fem punkter), psykomotorikk (to punkter) og psykososialitet (tre punkter). En observatør skårer punktene med 0 til 3 poeng for hvert, der 0 betyr at pasienten ikke viser tegn på den aktuelle atferden mens 3 betyr maksimalt nivå. Observatøren skårer i henhold til de punktene som er relevante for den enkelte pasient og summerer poengene. Total skåre kan variere mellom 0 og 30. En skåre over 5 indikerer at pasienten kan ha smerter, og bør medføre videre utredning. Konstruktørene av Doloplus-2 understreker at klinisk utprøvning av analgetika med påfølgende repeterte målinger er påkrevd for å måle effekten av behandlingen. Eventuell tvil bør komme pasienten til gode i form av analgetisk prøvebehandling ved mistanke om smerter tross lav skåre.
To publikasjoner om Doloplus-2 foreligger på fransk, og det vanskeliggjør vurderingen av dem. Doloplus-2 er oversatt til engelsk, men det foreligger ingen studier av denne versjonen. Begrunnelsen for å sette 5 som grenseverdi er dårlig dokumentert. Begrepsvaliditeten er svakt dokumentert hos pasienter med kognitiv svikt, blant annet fordi valideringen er gjennomført hos pasienter som var i stand til også å rapportere smerte på selvrapporteringsskjemaer. Doloplus-2 er oversatt til norsk (e-fig 1), og den første valideringsstudien er gjennomført (27). Foreløpige funn tyder på godt samsvar med kompetente klinikeres vurdering av smerte, men også på at deler av instrumentet har liten verdi (områdene psykomotorikk og psykososialitet).
Diskusjon
Vurdering av ansiktsuttrykk går igjen i alle måleinstrumentene (tab 1). Dette er også vist å være den mest smertesensitive komponenten i flere av skalaene (17, 18). Da mange av smertetilstandene hos eldre stammer fra bevegelsesapparatet, vil en god skala måtte omfatte smerteregistrering med pasienten mobilisert.
Flere skalaer mangler registrering av aktivitet i sosiale sammenhenger. Generell aktivitetsnedsettelse kan være et tegn på smerte. Slike subtile tegn har gjerne lav spesifisitet, men øker skalaens sensitivitet. I en klinisk situasjon vil et falskt positiv svar være å foretrekke fremfor et falskt negativt, da pasienten har lite å tape på en videre klinisk utredning. Det kan derfor synes riktig også å inkludere de mindre smertespesifikke atferdstrekkene i skalaer til klinisk bruk. Smertemålingsverktøy til bruk i forskning bør imidlertid ha både høy sensitivitet og høy spesifisitet. Til slikt bruk synes det derfor best å benytte måleverktøy uten subtile smerteindikatorer for å unngå for mange falskt positive svar. Målet bør være å komme frem til instrumenter som kan benyttes både i klinisk praksis og i forskning.
Noen svakheter går igjen i de fleste studiene. Blant annet er studiepopulasjonene små og mangelfullt beskrevet (28). Dette gjør det vanskelig å vite hvilken populasjon smertemålingsverktøyet er valid for. Få studier har data om observatørene som utførte målingene. Det er ønskelig å vite hvor mange observatører som faktisk klarte å bruke instrumentet slik det var forventet. Det mangler også en diskusjon om hvilken kategori av observatører, f.eks. leger, sykepleiere, ufaglærte pleiere eller pårørende, som egner seg best til å vurdere pasientens smerte. Angivelse av grad av samsvar mellom ulike målere er også mangelfull.
Poenggiving og tolking av smerten synes lite underbygd for flere av skalaene (17, 21) – (24). Det mangler tolkingsinstrukser eller det er ikke forklart hvordan man har kommet frem til de ulike grenseverdiene. Det er også gjennomgående mangel på instruksjoner om hvordan et mangelfullt utfylt skjema skal håndteres.
Enkelte av valideringsstudiene er begrenset til ett spesifikt smerteproblem, f.eks. knesmerter, ryggsmerter eller postoperative smerter (16). Dette gjør det vanskelig å vurdere om skalaene er valide for andre tilstander enn de som er studert.
Konklusjon
En grunnregel er å benytte enkle metoder for å måle smerte og andre subjektive symptomer hos sykehjemspasienter. Det enkleste er å benytte numerisk rangeringsskala som anbefalt i Norsk Standard i Palliasjon, også hos pasienter som har lett til moderat kognitiv svikt (29). For pasienter med mer uttalt kognitiv svikt finnes en rekke atferdsbaserte skalaer for smertemåling, men ingen er fullgodt testet med hensyn til validitet og reliabilitet (28, 30, 31). Det er derfor ønskelig med en standard eller nasjonal anbefaling om hvilket måleinstrument som bør inngå i et minste klinisk datasett ved norske sykehjem. Forskningsgrupper som arbeider innen feltet, bør etablere et nasjonalt samarbeid om disse problemstillingene.
Oppgitte interessekonflikter: Ingen
- 1.
Porter FL, Malhotra KM, Wolf CM et al. Dementia and response to pain in the elderly. Pain 1996; 68: 413 – 21.
- 2.
Brockopp D, Warden S, Colclough G et al. Elderly people’s knowledge of and attitudes to pain management. Br J Nurs 1996; 5: 556 – 62.
- 3.
Laake K. Geriatri i praksis. Oslo: Gyldendal Akademisk, 2003.
- 4.
Holtan A, Kongsgaard UE, Ohnstad HO. Smerter hos kreftpasienter innlagt i sykehus Tidsskr Nor Lægeforen 2005; 125: 416 – 8.
- 5.
Manfredi PL, Breuer B, Meier DE et al. Pain assessment in elderly patients with severe dementia. J Pain Symptom Manage 2003; 25: 48 – 52.
- 6.
Frampton M. Experience assessment and management of pain in people with dementia. Age Ageing 2003; 32: 248 – 51.
- 7.
Horgas AL, Tsai PF. Analgesic drug prescription and use in cognitively impaired nursing home residents. Nurs Res 1998; 47: 235 – 42.
- 8.
Scherder EJ, Sergeant JA, Swaab DF. Pain processing in dementia and its relation to neuropathology. Lancet Neurol 2003; 2: 677 – 86.
- 9.
Marquié L, Raufaste E, Lauque D et al. Pain rating by patients and physicians: evidence of systematic pain miscalibration. Pain 2003; 102: 289 – 96.
- 10.
Cohen-Mansfield J, Lipson S. Pain in cognitively impaired nursing home residents: how well are physicians diagnosing it? J Am Geriatr Soc 2002; 50: 1039 – 44.
- 11.
Jensen MP, Karoly P, Braver S. The measurement of clinical pain intensity: a comparison of six methods. Pain 1986; 27: 117 – 26.
- 12.
Epps CD. Recognizing pain in the institutionalized elder with dementia. Geriatr Nurs 2001; 22: 71 – 7.
- 13.
Scherder EJ, Bouma A. Visual analogue scales for pain assessment in Alzheimer’s disease. Gerontology 2000; 46: 47 – 53.
- 14.
Ferrell BA, Ferrell BR, Rivera L. Pain in cognitively impaired nursing home patients. J Pain Symptom Manage 1995; 10: 591 – 8.
- 15.
Herr K. Pain assessment in cognitively impaired older adults. Am J Nurs 2002; 102: 65 – 7.
- 16.
Bell ML. Postoperative pain management for the cognitively impaired older adult. Semin Perioper Nurs 1997; 6: 37 – 41.
- 17.
Fuchs-Lacelle S, Hadjistavropoulos T. Development and preliminary validation of the pain assessment checklist for seniors with limited ability to communicate (PACSLAC). Pain Manag Nurs 2004; 5: 37 – 49.
- 18.
Feldt KS. The checklist of nonverbal pain indicators (CNPI). Pain Manag Nurs 2000; 1: 13 – 21.
- 19.
Hurley AC, Volicer BJ, Hanrahan PA et al. Assessment of discomfort in advanced Alzheimer patients. Res Nurs Health 1992; 15: 369 – 77.
- 20.
Lane P, Kuntupis M, MacDonald S et al. A pain assessment tool for people with advanced Alzheimer’s and other progressive dementias. Home Healthc Nurse 2003; 21: 32 – 7.
- 21.
Villanueva MR, Smith TL, Erickson JS et al. Pain assessment for the dementing elderly (PADE): reliability and validity of a new measure. J Am Med Dir Assoc 2003; 4: 1 – 8.
- 22.
Snow AL, Weber JB, O’Malley KJ et al. NOPPAIN: a nursing assistant-administered pain assessment instrument for use in dementia. Dement Geriatr Cogn Disord 2004; 17: 240 – 6.
- 23.
Abbey J, Piller N, De Bellis A et al. The Abbey pain scale: a 1-minute numerical indicator for people with end-stage dementia. Int J Palliat Nurs 2004; 10: 6 – 13.
- 24.
Lefebvre-Chapiro S. The Doloplus 2 scale – evaluating pain in the elderly. Eur J Palliat Care 2001; 8: 191 – 4.
- 25.
Nygaard HA, Jarland M. Vurdering av smerteproblemer hos personer med demens. Demens 2004; nr. 4: 5 – 7.
- 26.
CNP Foundation. The Doloplus 2. www.doloplus.com/versiongb/index.htm (6.4.2005).
- 27.
Hølen JC, Saltvedt I, Fayers PM et al. The Norwegian Doloplus-2, a tool for behavioural pain assessment: Translation and pilot-validation in nursing home patients with cognitive impairment. Palliat Med 2005; 19: 1 – 7.
- 28.
Rodriguez CS. Pain measurement in the elderly: a review. Pain Manag Nurs 2001; 2: 38 – 46.
- 29.
Norsk Standard i Palliasjon 2004. www.palliativmed.org (6.4.2005).
- 30.
Richards JS, Nepomuceno C, Riles M et al. Assessing pain behavior: the UAB Pain Behavior Scale. Pain 1982; 14: 393 – 8.
- 31.
Wilkie DJ, Savedra MC, Holzemer WL et al. Use of the McGill Pain Questionnaire to measure pain: a meta-analysis. Nurs Res 1990; 39: 36 – 41.