Koronar ballongdilatasjon ved akutt transmuralt hjerteinfarkt har vært utført i mange år internasjonalt, og man begynner nå å få resultater som gjør det mulig å sammenlikne dette med den vanligste alternative behandlingen, nemlig medikamentell trombolyse. Det er vist at tidlig reetablering av blodstrøm i koronararterien ved akutt hjerteinfarkt er det viktigste for både overlevelse og bevaring av venstre ventrikkel-funksjon, enten det skjer ved trombolytisk behandling eller mekanisk. Den største ulempen ved trombolytisk behandling er manglende reperfusjon hos bortimot 30 – 40 % (1). I flere studier har man påvist at man ved primær angioplastikk kan oppnå reperfusjon hos> 95 % av pasientene (2 – 7).
Ved Ullevål sykehus har vi siden våren 1996 utført primær angioplastikk hos pasienter med transmurale infarkter. På denne tiden var det usikkerhet om metodens plass i infarktbehandlingen. De første 100 pasientene inngikk derfor i et prosjekt for å evaluere nytteverdien. Våre tidligste erfaringer ble beskrevet i 1998 (8), og resultater fra angioplastikk hos pasienter som overlevde hjertestans ble publisert i 1999 (9). I dette arbeidet vil vi beskrive våre erfaringer fra angiografilaboratoriet med de første 100 pasientene, de angiografiske funn og resultatene.
Materiale og metode
100 pasienter ble inkludert, 78 menn og 22 kvinner, med gjennomsnittsalder 59 år (23 – 85 år). Tidspunktet for ankomst til laboratoriet var dagtid (kl 7 – 17) for 73 %, kveldstid (kl 17 – 23) for 20 % og nattetid for 7 %. Ti pasienter ble behandlet lørdag eller søndag. De initiale kliniske data ble prospektivt registrert i en database. Kliniske oppfølgingsdata er skaffet ved å innkalle pasientene til etterkontroll og sjekke folkeregisterets database. Prosedyredata er skaffet retrospektivt fra laboratorieregistreringer, rapporter og gjennomgang av lagrede filmer. Radiologiske undersøkelser og prosedyrer etter den initiale behandlingen er funnet i skrivetjenestens tekstarkiv og gjennomgått.
Ved ankomst til sykehuset ble det gitt heparin 10 000 IE intravenøst og acetylsalisylsyre. På dagtid ble pasienten tatt inn til behandling når det første av to laboratorier var ledig. Utenom arbeidstid ble en radiolog og en radiograf i bakvakt tilkalt. Tilkallingstid for disse var 30 minutter. Vakthavende kardiolog og en sykepleier ved overvåkingsavdelingen var ofte til stede.
Infarktrelatert arterie er angitt i henhold til coronary artery surgery study (10). I grupperingen er intermediær-/trifurkaturgren definert som gren av CX. Stenosegrad er oppgitt som diameterstenose og målt med kvantitativ koronarangiografi. Ved blodstrømsgradering er det benyttet TIMI-gradering (11), der TIMI 0 = ingen, TIMI 1 = minimal, TIMI 2 = noe redusert og TIMI 3 = normal. Definisjon av tromber var synlige intraluminale defekter eller brått avkuttet karsegment.
Resultater
Prosedyre
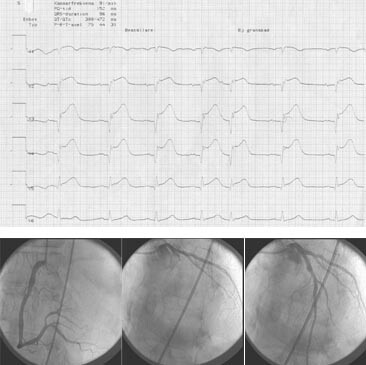
Diameter på innfører i femoralarterien var 8 F (2,7 cm) hos 89 %, 7 F hos 9 % og 6 F hos 2 % (tab 1). Denne ble trukket ut samme dag hos 23 % og ble liggende inne til neste dag hos 77 %. Planlagt strategi var angiografi av antatt frisk arterie først og deretter angiografi og angioplastikk av den infarktrelaterte arterien (fig 1). Dette ble gjennomført hos 77 %. På grunnlag av EKG og angiografifunn var vi i stand til å identifisere aktuelle okkluderte arterie hos 97 %, mens hos de øvrige 3 % måtte vi åpne mer enn ett kar. Tiden som gikk med på laboratoriet fremgår av tabell 1.
Tabell 1
Angiografiske funn og prosedyredata ved diagnostikk og angioplastikk
| (%) |
||
| Grad av karsykdom |
||
| Ettkarsykdom |
55 |
|
| To kar |
25 |
|
| Tre kar |
20 |
|
| Infarktrelatert arterie |
||
| LAD¹ |
45 |
|
| CX² |
14 |
|
| RCA³ |
40 |
|
| Bypassgraft |
1 |
|
| Perifere stenoser |
24 |
|
| Angiografisk tvil om aktuell karokklusjon |
3 |
|
| Diagnostisk tilnærming |
||
| Diagnostikk av normal side, deretter diagnostikk og behandling av infarktåren |
77 |
|
| Full diagnostikk, deretter angioplastikk |
14 |
|
| Annet |
9 |
|
| Størrelse på innfører |
||
| 8 F⁴ (2,7 mm) |
89 |
|
| 6 F⁴ eller 7 F⁴ |
11 |
|
| Fjerning av innfører |
||
| Samme dag |
23 |
|
| Neste dag |
77 |
|
| Stent |
73 |
|
| Første 50 |
64 |
|
| Siste 50 |
82 |
|
| GPIIb/IIIa-platehemmer |
11 |
|
| Laboratorietider (min) |
||
| Punksjon – etablert blodstrøm |
15 ± 8 (3 – 58) |
|
| Punksjon – avslutning |
38 ± 20 (9 – 91) |
|
| Gjennomlysning |
12 ± 9 (2 – 46) |
|
| ||
Utstyr
Gjennomsnittlig kontrastmiddelforbruk var 192 ml ± 105 (50 – 625 ml). Det ble benyttet forskjellige typer koronare ledewirer, men hos ca. 50 % kom vi igjennom lesjonen med en glatt wire med polymertupp. Den første tiden var dette andrevalg, men ble etter hvert førstevalg. Stent ble lagt inn hos 73 %, 1 – 4 stykker. Bruken av stent økte fra 64 % hos de første 50 til 82 % hos de neste 50 pasientene. Hos 13 pasienter ble det benyttet spesialutstyr som ikke inngår i en rutinemessig angioplastikk: mekanisk trombektomi (to), intravaskulær ultralyd (én), lang innfører (én), dobbeltlumen diagnostisk kateter (tre), bifurkasjonsstent (én) og sidegrensstent (fem). Fem pasienter fikk innlagt temporær pacemaker fra lysken og hos ytterligere to ble det klargjort for dette. Pasientene som fikk stent, ble behandlet med tiklopidin i 14 dager, med behandlingsstart etter prosedyren. Glykoprotein IIb/IIIa-platehemmer (abciximab) ble gitt til 11 pasienter, men var bare tilgjengelig for de siste 72 av pasientene. Kostnadene ved alt engangsutstyret inkludert medikamentene har vi beregnet til ca. 13 000 kroner.
Angiografiske resultater
Fordelingen av graden av koronararteriesykdom var ettkarsykdom hos 55 %, tokar- hos 25 % og trekar- hos 20 % (tab 1). Tabell 2 viser angiografiske funn i den infarktrelaterte arterien. 85 % var helt eller nærmest helt okkludert og i 92 % var det lite eller ingen antegrad blodstrøm. Synlig trombe eller sterk mistanke om trombe ble funnet hos 69 %. Infarktlesjonen omfattet avgangen av store sidegrener hos 12 %.
Den infarktrelaterte arterien ble åpnet med godt resultat hos 95 % (tab 2). Hele 87 pasienter hadde normal blodstrøm i den infarktrelaterte arterie (TIMI 3) og ytterligere seks pasienter hadde god antegrad blodstrøm, men noe langsommere utvasking av kontrasten enn normalt (TIMI 2). Totalt 14 pasienter hadde resttromber enten lokalt ved stenosen eller perifert i arterien ved avsluttet prosedyre. Av disse fikk halvparten platehemmeren GPIIb/IIIa.
Tabell 2
Angiografiske resultater før og etter angioplastikk av den infarktrelaterte lesjon i koronararteriene. Tre pasienter ble ikke forsøkt behandlet
| Før |
Etter |
|
| Diameter stenose (%) |
||
| 100 |
74 |
1 |
| 99 |
11 |
1 |
| 50 – 90 |
13 |
4 |
| 30 – 50 |
1 |
9 |
| < 30 |
1 |
85 |
| Blodstrøm |
||
| TIMI 0 (ingen) |
73 |
1 |
| TIMI 1 (minimal) |
19 |
6 |
| TIMI 2 (noe redusert) |
6 |
6 |
| TIMI 3 (normal) |
2 |
87 |
| Tromber |
||
| I lesjonen |
69 |
4 |
| Perifert |
14 |
Etter reetablering av blodstrøm ble det oppdaget perifere stenoser i samme arterie hos 22 %. Av disse ble 15 forsøkt åpnet. De øvrige sju ble ikke forsøkt åpnet, da man mente at disse ikke hadde avgjørende betydning for blodstrøm i arterien. Hos ti pasienter ble det samtidig forsøkt utført angioplastikk av en arterie som ikke var relatert til infarktet. Hos to pasienter valgte man å behandle øvrige arterier elektivt på et senere tidspunkt.
Prosedyrerelaterte hendelser, komplikasjoner og ny invasiv behandling
I tilknytning til angiografi og angioplastikken ble en pasient sendt til akutt bypasskirurgi (tab 3) pga. en ukontrollerbar disseksjon. Ingen pasienter døde. Ingen pasienter fikk ventrikkelflimmer. Alle de fem pasientene som fikk lagt inn temporær pacemaker hadde okklusjon av høyre koronararterie. Subakutt okklusjon av den behandlede arterien skjedde hos e…n pasient etter ca. en time, og arterien ble gjenåpnet med ny angioplastikk. Punksjonskomplikasjoner ble observert hos sju pasienter. Det var stort lyskehematom hos fem, og hos tre av dem ble det nødvendig med blodtransfusjon. Begge pasientene med pseudoaneurisme ble behandlet med ultralydveiledet kompresjon.
Tabell 3
Antall pasienter med prosedyrerelaterte komplikasjoner, alvorlige hendelser innen 30 dager og behov for ny invasiv behandling
| 0 – 24 |
||
| timer |
1 – 30 dager |
|
| Død |
0 |
1 |
| Nytt hjerte- |
infarkt |
|
| Samme åre |
0 |
0 |
| Annen åre |
0 |
0 |
| Ny angio- |
plastikk |
|
| Samme åre |
1 |
1 |
| (1 time) |
(11 dager) |
|
| Annen åre |
2 (elektiv) |
|
| Bypassoperasjon |
1 (akutt) |
1 (elektiv) |
| Punksjonsrela- |
tert |
|
| Lyskehema- |
tom |
5 |
| Pseudoaneu- |
risme |
2 |
| Temporær pace- |
maker |
5 |
| Ventrikkelflimmer/takykardi |
0 |
1 |
Diskusjon
Våre erfaringer med primær angioplastikk ved akutt hjerteinfarkt er gode hos de 100 første inkluderte pasientene. Akutt- og kortidsresultatene er vel så gode som andre publiserte data (2 – 7), også sammenliknet med norske resultater i den senere tid (12, 13). Det er flere faktorer i utviklingen av angioplastikkteknikken som i dag gjør denne pasientbehandlingen mulig og som gjør at den er et reelt alternativ til generell trombolytisk behandling. For det første utføres det ved de fleste angioplastikksentrene i Norge så mange prosedyrer at den enkelte operatør har tilstrekkelig trening til å utføre prosedyren raskt og med få komplikasjoner. Også utviklingen av utstyret har vært stor, og suksessraten for å åpne okkluderte arteriegrener er bedret. Dette gjelder både engangsutstyret og selve bildekjeden på laboratoriet. Vi vil spesielt trekke frem bruk av stenter, som i løpet av inklusjonsperioden ble standardbehandling (14). Selv om det fortsatt er diskusjon om hvorvidt en stent reduserer restenoseraten, erfarer vi at prosedyren går mye raskere. Samtidig har bruken av platehemmere etterpå nærmest eliminert faren for akutt og subakutt okklusjon (15). Dette var også tilfellet for våre pasienter, hvor bare 2 % hadde klinisk tegn på reokklusjon.
Hele 45 % av pasientgruppen hadde fleråresykdom. Vi behandlet andre årer hos ti pasienter. Behandlingstiden for disse var lengre enn for de øvrige, 50 minutter versus 38 minutter. På den annen side ville flere av disse pasientene ha måttet gjennomgå en ny elektiv prosedyre, enten i form av angioplastikk eller bypasskirurgi. Denne avveiningen må tas i hvert enkelt tilfelle. Noen pasienter var såpass stabile etter at den infarktrelaterte arterien var åpnet at vi syntes at vi kunne tillate oss denne tilleggsprosedyren, men vår prinsipielle holdning er fortsatt den at hos de fleste skal vi bare behandle den infarktrelaterte åren.
Antall komplikasjoner fra punksjonsstedet forventes å gå ned fordi vi har gått over til tynnere katetere (fra 8 F til 6 F), fordi innføringsstykkene fjernes raskere etter prosedyren og ikke minst nylig overgang fra punksjon i femoralarterien til radialisarterien. Bare unntaksvis valgte vi tidligere dette punksjonsstedet ved akutt infarkt, både fordi prosedyren tok noe lengre tid og fordi vi hos noen pasienter må gå over til lyskepunksjon under prosedyren da vi ikke klarer å gjennomføre behandlingen via arteria radialis. Vi har endret dette nå som vi har fått mer erfaring med teknikken ved de elektive prosedyrene.
Ressursbruken og dermed kostnadene ved angioplastikk av akutt hjerteinfarkt var ikke vesentlig forskjellig fra angioplastikk av elektive pasienter. Kostnadene ved engangsutstyr går stadig ned, men eventuelt økt bruk av GPIIb/IIIa-platehemmere vil være kraftig kostnadsdrivende. Allerede i dag utfører vi angioplastikk i samme prosedyre som den diagnostiske undersøkelsen for de fleste pasientene. Avdelingen har allerede en radiolog og en radiograf i døgnkontinuerlig vakt, for akutt angioplastikk og akutte vaskulære prosedyrer ved bl.a. traumer. Det har ikke vært behov for å innkalle ekstra personell under prosedyren, men det har vært nyttig med flere enn to til stede. Dette løste vi ved at vakthavende kardiolog og en sykepleier fra overvåkingsavdelingen var med.
Ved transport av en pasient til et sykehus hvor det utføres PTCA vil det ta lengre tid før igangsetting av behandling enn for trombolytisk behandling. Det er usikkert hvor negativt dette er for primær PTCA (16), og det har sannsynligvis sammenheng med at reetablering av blodstrøm i den infarktrelaterte åren er mye høyere ved PTCA (>90 %) enn ved trombolytisk behandling (50 – 60 %). Revaskulariseringen ved primær PTCA er også mer komplett, med etablering av god blodstrøm, og færre årer reokkluderer den første tiden etter behandlingen. Ikke alle PTCA-behandlede pasienter har en normal blodstrøm selv om stenosen/okklusjonen er fjernet. Dette så vi også hos våre pasienter, der det var redusert blodstrøm hos hele ni av 95 vellykket behandlede pasienter. Dette viste seg ved hemmet antegrad blodstrøm, forsinket utvasking av kontrastmidlet i periferien eller avkuttede små perifere grener. Graden av blodstrøm etter PTCA har betydning for prognosen etter behandlingen, og reduksjonen har sammenheng med perifer embolisering og infarktskadet myokard. Bruk av stent kan bedre det akutte resultatet og ble benyttet hos flertallet av våre pasienter. Andre foreslåtte tiltak er å bruke GPIIb/IIIa-platehemmere (17, 18). Flere arbeider har vist at dette gir bedret prognose, men medikamentet er kostbart og gir økte blødningskomplikasjoner. I dette materialet fikk bare 11 % av pasientene abciximab. Vi benyttet medikamentet ved mye tromber før rekanalisering, lokale eller perifere tromber etter behandlingen og hvis TIMI 3-blodstrøm ikke ble oppnådd på mistanken om perifer embolisering. Helt nylig er det foreslått å benytte et paraplyfilt
er (Angioguard) for å hindre perifer embolisering, det samme som nylig er tatt i bruk ved angioplastikk av halskar.
- 1.
Simes RJ, Topol EJ, Holmes DR jr., White HD, Rutsch WR, Vahanian A et al. Link between the angiographic substudy and mortality outcomes in a large randomized trial of myocardial reperfusion. Importance of early and complete infarct artery reperfusion. Circulation 1995; 91: 1923 – 8.
- 2.
Zijlstra F, Hoorntje JC, de Boer MJ, Reiffers S, Miedema K, Ottervanger JP et al. Long-term benefit of primary angioplasty as compared with thrombolytic therapy for acute myocardial infarction. N Engl J Med 1999; 341: 1413 – 9.
- 3.
Faxon DP, Heger JW. Primary angioplasty – enduring the test of time. N Engl J Med 1999; 341: 1464 – 5.
- 4.
Weaver WD, Simes RJ, Betriu A, Grines CL, Zijlstra F, Garcia E et al. Comparison of primary coronary angioplasty and intravenous thrombolytic therapy for acute myocardial infarction: a quantitative review. JAMA 1997; 278: 2093 – 8.
- 5.
Yusuf S, Pogue J. Primary angioplasty compared to thrombolytic therapy for acute myocardial infarction. JAMA 1997; 278: 2110 – 1.
- 6.
Antoniucci D, Santoro GM, Bolognese L, Valenti R, Trapani M, Fazzini PF. A clinical trial comparing primary stenting of the infarct-related artery with optimal primary angioplasty for acute myocardial infarction: results from the Florence Randomized Elective Stenting in Acute Coronary Occlusions (FRESCO) trial. J Am Coll Cardiol 1998; 31: 1234 – 9.
- 7.
Danchin N, Vaur L, Genes N, Etienne S, Angioi M, Ferrieres J et al. Treatment of acute myocardial infarction by primary coronary angioplasty or intravenous thrombolysis in the ”real world”: one-year results from a nationwide French survey. Circulation 1999; 99: 2639 – 44.
- 8.
Mangschau A, Bendz B, Rostrup M, Eritsland J, Müller C, Kjellevand TO et al. Angioplastikk ved akutt hjerteinfarkt. Tidsskr Nor Lægeforen 1998; 118: 687 – 91.
- 9.
Bendz B, Mangschau A, Eritsland J, Müller C, Brekke M. Angioplastikk ved hjertestans. Tidsskr Nor Lægeforen 1999; 119: 3410 – 3.
- 10.
The national heart, lung, and blood institute coronary artery surgery study (CASS). Circulation 1981; 63 (suppl 1): 59 – 60.
- 11.
Chesebro JH, Knatterud G, Roberts R, Borer J, Cohen LS, Dalen J et al. Thrombolysis in myocardial infarction (TIMI) trial, phase I: a comparison between intravenous tissue plasminogen activator and intravenous streptokinase. Circulation 1987; 76: 142 – 54.
- 12.
Andreassen AK, Gullestad L, Endresen K. Trombolytisk behandling ved akutt hjerteinfarkt. Preparatvalg ved norske sykehus. Tidsskr Nor Lægeforen 1998; 118: 2630 – 1.
- 13.
Hessen JO, Schei MA, Valle PC, Kildahl-Andersen O. Forbedrede rutiner for trombolytisk behandling ved akutt hjerteinfarkt. Tidsskr Nor Lægeforen 1999; 119: 2982 – 5.
- 14.
Suryapranata H, van’t Hof AW, Hoorntje JC, de Boer MJ, Zijlstra F. Randomized comparison of coronary stenting with balloon angioplasty in selected patients with acute myocardial infarction. Circulation 1998; 97: 2502 – 5.
- 15.
Myreng Y, Molstad P, Golf S. Behandling med tiklopidin etter intrakoronar stentimplantasjon. Tidsskr Nor Lægeforen 1996; 116: 1789 – 91.
- 16.
Straumann E, Yoon S, Naegeli B, Frielingsdorf J, Gerber A, Schuiki E et al. Hospital transfer for primary coronary angioplasty in high risk patients with acute myocardial infarction. Heart 1999; 82: 415 – 9.
- 17.
Brener SJ, Barr LA, Burchenal JE, Katz S, George BS, Jones AA et al. Randomized, placebo-controlled trial of platelet glycoprotein IIb/IIIa blockade with primary angioplasty for acute myocardial infarction. ReoPro and Primary PTCA Organization and Randomized Trial (RAPPORT) Investigators. Circulation 1998; 98: 734 – 41.
- 18.
Miller JM, Smalling R, Ohman EM, Bode C, Betriu A, Kleiman NS et al. Effectiveness of early coronary angioplasty and abciximab for failed thrombolysis (reteplase or alteplase) during acute myocardial infarction (results from the GUSTO-III trial). Global Use of Strategies To Open occluded coronary arteries. Am J Cardiol 1999; 84: 779 – 84._