Background.
Semen analysis is an important part of the infertility investigation, but its usefulness as a predictor of fertility is under debate.
Material and methods.
The article is based on the authors’ experience from andrology laboratories and participation in the WHO’s editorial committee for standardization of semen analysis and literature retrieved through non-systematic searches of Medline and PubMed.
Results and interpretation.
There is currently no simple and reliable method to predict the fertility of a man. Most laboratories still use semen analyses that are based on methodology introduced in the 1950s. To allow meaningful comparison of results with previous investigations, results from other laboratories or with reference intervals, it is essential that the methods are standardized and evidence-based. Several studies have shown a correlation between semen variables such as sperm concentration, progressive motility and sperm morphology, and time to pregnancy. The results of semen analysis are often difficult to interpret without patient history and other investigations and do not provide a diagnosis by themselves; they must therefore be interpreted in conjunction with other medical investigations of the couple.
Fertilitetsutredning av et par starter ofte med en sædanalyse, men nytteverdien av denne for prediksjon av fertiliteten er omdiskutert. Dette skyldes både mangel på studier som viser en klar sammenheng med mannens fertiliseringspotensial, og vanskeligheter med å standardisere metodene. Dette innebærer at henvisende lege ofte ikke vet hvordan prøvesvaret skal tolkes, dvs. hva han/hun skal si til pasienten, og hvilke behandlingsmessige konsekvenser det har.
Materiale og metode
Verdens helseorganisasjon (WHO) har siden 1980 med jevne mellomrom kommet med retningslinjer om hvordan sædanalysen skal gjennomføres. Den nyeste manualen ble utgitt i 1999 (1), og en ny er under utarbeiding. Målet er at den skal være evidensbasert i så stor grad som mulig. Sædanalysens resultat er av interesse også i andre sammenhenger enn i fertilitetsutredning, som f.eks. etter vasektomi, kartlegging av yrkes-, miljø- eller behandlingseffekter og i multisenterstudier, der ulike populasjoner skal sammenliknes.
I det følgende diskuteres sædanalysens betydning i fertilitetsutredning. For å forstå den kliniske betydningen av sædanalysen, er det nødvendig å kjenne til de biologiske og laboratorietekniske perspektivene. Artikkelen er basert på lang erfaring fra andrologiske laboratorier, fra arbeid i WHOs arbeidsgruppe om sædanalyse og fra ikke-systematisk litteratursøk i Medline og PubMed.
Spermatogenesen
Danningen av spermier er hormonelt regulert, og de viktigste hormonene som inngår er folikkelstimulerende hormon, luteiniserende hormon, testosteron og inhibin B. I tillegg er vekstfaktorer som produseres lokalt i testikkelen, viktige i reguleringen av spermatogenesen.
Hos mennesket tar det omtrent 75 dager for en spermie å utvikles i testikkelen fra stamcellen, spermatogoniet. Modningsprosessen i bitestikkelen tar ytterligere to uker. De siste tre ukene av spermatogenesen, som kalles spermiogenesen, er temperatursensitiv. Infeksjoner som forårsaker temperaturstigning, kan derfor påvirke denne prosessen. Spermatogenesen kan også påvirkes av ulike sykdommer, miljø- og livsstilsfaktorer samt visse medikamenter. Figur 1 viser en skjematisk fremstilling av en spermie.
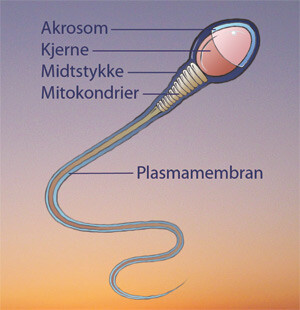
Sædprøven
Ca. to tredeler av ejakulatet består normalt av sekret fra sædblærene, mens en tredel er prostatasekret. Spermiene, væske fra testikkelen og de bulbourethrale kjertler utgjør kun noen få volumprosent. En stor del av sekretet som kommer fra prostata og sædblærer, produseres i forbindelse med ejakulasjonen og er avhengig av graden av stimulering (2). Ejakulasjonen er en sekvensiell prosess, og spermiene tømmes ut først sammen med prostatasekretet. Til slutt tømmes sædblærenes sekret ut sammen med et fåtall spermier (3). Spermiene som kommer sammen med prostatasekretet, har større bevegelighet og overlevelse enn de som er i sædblæresekretet, og spermiekromatinet synes å være bedre beskyttet (4, 5).
Laboratorieprøven produseres ved masturbasjon og oppbevares lyst i nærvær av oksygen. Den er derfor ikke nødvendigvis representativ for ejakulatet som produseres under samleiet. Prøven sier noe om funksjonen til mannens genitalia med henblikk på produksjon, transport og uttømming av spermier. Isolert sett gir den begrenset informasjon om parets sjanse til å oppnå graviditet. Ved avvikende prøvesvar anbefales det at det gjøres en ny sædanalyse etter tre måneder.
Standardisering
For å sammenlikne et sædanalysesvar med tidligere prøvesvar, resultater fra andre laboratorier eller med referanseintervaller, er det nødvendig at metodene er standardisert. Det forutsetter også at laboratoriet har rutiner for intern og ekstern kvalitetskontroll. Eksterne kvalitetskontrollprogrammer pågår med deltakere fra Europa, USA, Canada, Afrika og Australia (1).
Manualen som utgis fra Verdens helseorganisasjon, gir retningslinjer for hvordan metodene skal utføres og beskriver prosedyrer for kvalitetskontroll og kvalitetssikring (1). I tillegg har European Society of Human Reproduction and Embryology (ESHRE) i samarbeid med Nordic Association for Andrology (NAFA) gitt ut en mer detaljert beskrivelse av metodene (6). Målet er at metodene skal være enkle å utføre uten bruk av kostbart utstyr, at man i størst mulig grad skal unngå feilkilder og at eventuelle feilkilder lett skal kunne oppdages. Siden 1994 har det vært arrangert standardiserte kurs i Europa for å trene opp laboratoriepersonell i å følge WHOs retningslinjer. Behovet og nytteverdien av slike kurs er dokumentert (7).
Standard sædanalyse
Spermiekonsentrasjon og totalt antall spermier
Spermiekonsentrasjonen avhenger av produksjon, transport og uttømming av spermier, samt volumet av seminalplasma. Enkelte ganger kan en lav spermiekonsentrasjon skyldes økt sekresjon fra sædblærene og prostata, mens et lite sædvolum kan gi en høy spermiekonsentrasjon. Det er derfor viktig å bestemme totalt antall spermier i ejakulatet. Ved å telle antall spermier og måle volumet av sædprøven, kan konsentrasjonen og totalantallet av spermier i ejakulatet bestemmes. Til dette er det ikke tilstrekkelig å benytte alminnelige metoder for celletelling, for retningslinjene til WHO må følges for å få pålitelige resultater. For eksempel introduseres en betydelig feilkilde hvis volumet bestemmes ved annen metode enn ved veiing (8).
I den nyeste manualen fra WHO er en konsentrasjon på minst 20 millioner spermier per milliliter oppgitt som nedre normalgrense (1). Samtidig har andre studier, deriblant en fra Norge, vist at et referanseintervall basert på 95 % av de fertile menn som inngikk i studien, har en nedre grense som er lavere enn WHO-grensen. I det norske materialet ble 5-prosentilen beregnet til 11 millioner per milliliter (9).
Spermiemotilitet
Spermienes motilitet evalueres ved mikroskopering innen en time etter at prøven er avlagt. Motiliteten reduseres over tid, avhengig av tilgang på energi og forekomst av reaktive, skadelige oksygenforbindelser produsert av spermiene selv eller av leukocytter i seminalplasma.
Spermiene kan klassifiseres i fire kategorier ut fra sin bevegelighet, og der progressivt betyr at de beveger seg fremover: (a) raskt progressivt motile spermier, (b) langsomt progressivt motile spermier, (c) ikke-progressivt motile spermier, og (d) immotile spermier, som er ubevegelige.
Spermievitalitet
Når det er svært få eller ingen motile spermier, er det viktig å avklare om spermiene er døde eller ikke. Det har vært et problem at vitalitetsmetoder i seg selv kan skade spermiene, men ved metoden anbefalt av ESHRE unngår man dette problemet (6).
Hvis en stor del av de immotile spermiene er levende, er det sannsynlig at pasienten har den genetiske sykdommen immotile cilia-syndrom (10). Ved mange døde spermier i prøven bør pasientene utredes videre for å finne årsak, som kan være cytotoksiske antistoffer eller infeksjon.
Spermiemorfologi
De fleste spermier i en normal sædprøve har ikke normal morfologi (fig 2), noe som er et fellestrekk blant primater med relativt liten konkurranse på spermienivå. I et forsøk på å finne et godt biologisk grunnlag for evaluering av spermiemorfologi, er det utviklet svært strikte kriterier (11).
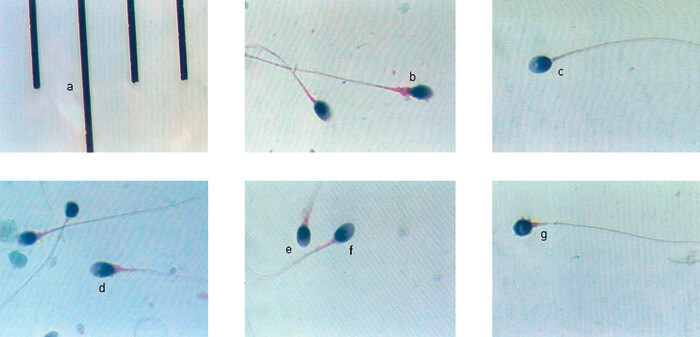
Disse kriteriene er blitt kritisert for å gi for lav andel normale spermier, og at det derfor er vanskelig å skille mellom fertile og subfertile menn. Imidlertid bygger de strikte kriteriene på observasjoner av morfologien til spermier som var i stand til å penetrere cervixsekretet samt binde til zona pellucida, og er de best evaluerte kriteriene. I den norske studien av fertile menn er 5-prosentilen for morfologisk normale (ideelle) spermier 3 % (9). I ESHRE-NAFA-manualen er det beskrevet hvordan teratozoospermiindeks beregnes ut fra fire typer defekter og er et mål på hvor mange defekter en unormal spermie har i gjennomsnitt i prøven (6).
Antistoffanalyser
Antispermieantistoffer antas å forårsake infertilitet hos en del par ved at de enten reduserer spermienes evne til å penetrere cervixsekretet eller ved at de hemmer fertiliseringen av egget. Imidlertid har undersøkelser vist at for noen menn har nærvær av antistoffer på spermienes overflate ingen betydning for muligheten til å frembringe graviditet ved in vitro-fertilisering (12). Tidligere ble antispermieantistoffer bestemt i serum, men det samsvarer ikke nødvendigvis med tilstedeværelse av antispermieantistoffer i sædprøven eller i genitaltractus hos kvinnen (13) – (15).
Minst 20 % av spermiene kan ha antistoffer festet til seg uten at det er en immunologisk årsak til infertiliteten. I de få tilfellene der stort sett alle spermiene bærer antispermieantistoffer, er det viktig å undersøke om inflammatoriske tilstander, som for eksempel prostatitt, vesikulitt og epididymitt, kan være årsak til produksjonen av antistoffene.
pH
pH reflekterer i hovedsak balansen mellom det sure prostatasekretet og det mer alkaliske sekretet fra sædblæren og er normalt i det alkaliske området (16). Som regel bestemmes pH i sædprøven, men verdien gir ingen klinisk informasjon hvis den er i det basiske området. Lavere pH-verdier enn 7,0 kan imidlertid bety at det ikke finnes sædblæresekret på grunn av obstruksjon eller bilateral agenesi av vas deferens, en tilstand der ofte sædblærene også mangler eller er dårlig utviklet.
Andre analyser
Det finnes andre analyser som kan gjøres av en sædprøve, men den kliniske verdien av disse er foreløpig uavklart. De er derfor ikke inkludert i standard rutineanalysene anbefalt av WHO, men omtales i WHO-manualen som valgfrie tester eller forskningstester.
Biokjemiske analyser
Bestemmelse av konsentrasjon og totalmengde av markører for prostata (Zn2+), sædblærer (fruktose) og bitestikkel (α-glukosidase) kan si noe om kjertlenes sekretoriske funksjon. Sekresjonsforstyrrelser kan i noen tilfeller forklare nedsatt spermiemotilitet (17) og spermievitalitet (18).
Funksjonstester
Det har lenge vært et mål å utvikle tester som kan avdekke forstyrrelser i spermienes funksjon, som ikke oppdages ved bestemmelse av spermietall, spermiemotilitet og spermiemorfologi (19). De fleste tilgjengelige metoder krever mer kostbart utstyr og er mer kompliserte å utføre enn standard sædanalyse, og den kliniske verdien er uavklart. Derfor brukes flere av disse testene, som akrosomreaksjonstest og spermiehyperaktiveringstest, mest i forskningssammenheng.
DNA-fragmentering
I de senere årene er det blitt publisert en rekke studier av såkalt DNA-fragmentering (20). Resultatene tyder på at spermie-DNA fra infertile menn er mer utsatt for skader enn tilsvarende fra fertile. Denne metoden krever avansert teknisk utstyr som vanligvis ikke finnes ved rutinelaboratoriene, for eksempel væskestrømscytometer.
Referanseverdier
For sædanalysesvar er det hensiktsmessig å betrakte det øvre 95 %-intervallet for sædvariablene i en populasjon som referanseområde, i motsetning til det sentrale 95 %-intervallet. Seleksjon av en referansepopulasjon for sædvariabler bør være menn som nylig har gjort sin partner gravid, og tid før oppnådd graviditet bør ikke overskride 12 måneder. Abstinenstiden bør dessuten være 2 – 7 dager, som anbefalt av WHO (1). Det er viktig å være klar over at referanseverdier kun angir en beskrivelse av resultater fra en befolkningsgruppe, i dette tilfellet menn som har gjort sin partner gravid, men det utelukker ikke at graviditet kan forekomme ved sædparametere utenfor intervallet. Dette gjelder 5 % av de fertile mennene i populasjonen et referanseintervall bygger på. Dessuten kan et referanseintervall basert på en etnisk gruppe ikke nødvendigvis være tilpasset en annen.
Kliniske betraktninger
Sædanalysen bør gjøres tidlig i fertilitetsutredningen (21). Prøvesvaret kan være vanskelig å tolke og gir ikke et entydig svar på en manns fertiliseringsevne. Imidlertid viser internasjonale studier en klar sammenheng mellom flere sædvariabler og sjansen for befruktning. I en dansk prospektiv studie ble det observert en omvendt korrelasjon mellom tid før oppnådd graviditet og spermiekonsentrasjonen opp til 40 mill. spermier per milliliter (22). I en europeisk multisenterstudie og i en amerikansk undersøkelse var de tilsvarende tallene henholdsvis 55 og 30 mill./ml (23, 24). I alle disse studiene var det dessuten en klar sammenheng mellom spermienes morfologi og tid før oppnådd graviditet. For spermiemotilitet ble det kun i den amerikanske studien observert en sammenheng med sannsynlighet for befruktning. Data fra studier der digital bildebehandlingsanalyse har vært benyttet, har antydet at tilstedeværelse av raskt progressive motile spermier (> 25 µm/s) er vesentlig for at fertilisering skal inntreffe (25, 26).
Kun én infertilitetsdiagnose kan bestemmes direkte ved analyse av spermienes morfologi, nemlig globozoospermi, som er en genetiske forstyrrelse der alle spermiehodene er runde (27).
I andre studier der fertile menn er blitt sammenliknet med en subfertil gruppe, er det vist forskjeller med henblikk på sædvariabler. På grunnlag av disse forskjellene har det vært antydet terskelverdier som kan benyttes til å klassifisere menn som subfertile, med ukjent fertilitetsstatus eller fertile (23). Sædprøvesvaret vil derfor ofte kunne si noe om sannsynligheten for befruktning, men dette må ses i sammenheng med kvinnens reproduktive helse og ikke minst alder. For par der mannen har dårlig sædkvalitet, vil intracytoplasmatisk spermieinjeksjon (ICSI) ofte være en aktuell behandlingsmetode. Siden det i Norge er åpnet for midlertidig behandling med intracytoplasmatisk spermieinjeksjon, der spermiene hentes ut fra testikkelen, kan dette være et behandlingstilbud til menn som ikke har spermier i ejakulatet (azoospermi) (28). I tilfeller der spermieproduksjonen gradvis reduseres, bør sæd fryses ned.
Det er et generelt problem at det i løpet av infertilitetsutredning av mannen ofte anses som tilstrekkelig å lete etter spermier som kan brukes ved ulike former for assistert befruktning, uten at den mannlige reproduksjonsforstyrrelsen utredes og behandles (29).
Konklusjon
Resultatene fra en standard sædanalyse viser spermiekonsentrasjon, morfologi og motilitet på det aktuelle tidspunkt. De må alltid sammenholdes med anamnese, klinisk undersøkelse og eventuelle andre undersøkelser som gjøres som del av fertilitetsutredningen. Ettersom målet er graviditet og fødsel av et friskt barn, bør utredningen av paret ses på som én felles utredning, der man alltid må ta i betraktning kvinnens alder. I enkelte tilfeller vil sædanalysesvaret gi klare indikasjoner på spesielle reproduksjonsforstyrrelser, som ved immotile cilia-syndrom eller globozoospermi.
Oppgitte interessekonflikter: Ingen
Tabell
| Hovedbudskap |
|
- 1.
World Health Organization. WHO laboratory manual for the examination of human semen and sperm-cervical mucus interactions. Cambridge, UK: Cambridge University Press, 1999.
- 2.
Pound N, Javed MH, Ruberto C et al. Duration of sexual arousal predicts semen parameters for masturbatory ejaculates. Physiol Behav 2002; 76: 685 – 9.
- 3.
Björndahl L, Kvist U. Sequence of ejaculation affects the spermatozoon as a carrier and its message. Reprod Biomed Online 2003; 7: 440 – 8.
- 4.
Björndahl L, Kjellberg S, Kvist U. Ejaculatory sequence in men with low sperm chromatin-zinc. Int J Androl 1991; 14: 174 – 8.
- 5.
Björndahl L, Kvist U. Influence of seminal vesicular fluid on the zinc content of human sperm chromatin. Int J Androl 1990; 13: 232 – 7.
- 6.
Kvist U, Björndahl L, red. Manual on basic semen analysis. Oxford: Oxford University Press, 2002.
- 7.
Björndahl L, Barratt CL, Fraser LR et al. ESHRE basic semen analysis courses 1995 – 1999: immediate beneficial effects of standardized training. Hum Reprod 2002; 17: 1299 – 305.
- 8.
Cooper TG, Brazil C, Swan SH et al. Ejaculate volume is seriously underestimated when semen is pipetted or decanted into cylinders from the collection vessel. J Androl 2007; 28: 1 – 4.
- 9.
Haugen TB, Egeland T, Magnus O. Semen parameters in Norwegian fertile men. J Androl 2006; 27: 66 – 71.
- 10.
Afzelius BA, Eliasson R, Johnsen O et al. Lack of dynein arms in immotile human spermatozoa. J Cell Biol 1975; 66: 225 – 32.
- 11.
Menkveld R, Stander FS, Kotze TJ et al. The evaluation of morphological characteristics of human spermatozoa according to stricter criteria. Hum Reprod 1990; 5: 586 – 92.
- 12.
Shibahara H, Shiraishi Y, Hirano Y et al. Diversity of the inhibitory effects on fertilization by anti-sperm antibodies bound to the surface of ejaculated human sperm. Hum Reprod 2003; 18: 1469 – 73.
- 13.
Hjort T. Do autoantibodies to sperm reduce fecundity? A mini-review in historical perspective. Am J Reprod Immunol 1998; 40: 215 – 22.
- 14.
Nip MM, Taylor PV, Rutherford AJ et al. Autoantibodies and antisperm antibodies in sera and follicular fluids of infertile patients; relation to reproductive outcome after in-vitro fertilization. Hum Reprod 1995; 10: 2564 – 9.
- 15.
Ohl DA, Naz RK. Infertility due to antisperm antibodies. Urology 1995; 46: 591 – 602.
- 16.
Haugen TB, Grotmol T. pH of human semen. Int J Androl 1998; 21: 105 – 8.
- 17.
Lindholmer C. The importance of seminal plasma for human sperm motility. Biol Reprod 1974; 10: 533 – 42.
- 18.
Lindholmer C. Survival of human spermatozoa in different fractions of split ejaculate. Fertil Steril 1973; 24: 521 – 6.
- 19.
Montoya JM, Bernal A, Borrero C. Diagnostics in assisted human reproduction. Reprod Biomed Online 2002; 5: 198 – 210.
- 20.
Tarozzi N, Bizzaro D, Flamigni C et al. Clinical relevance of sperm DNA damage in assisted reproduction. Reprod Biomed Online 2007; 14: 746 – 57.
- 21.
Barratt CL. Semen analysis is the cornerstone of investigation for male infertility. Practitioner 2007; 251: 8 – 10, 12, 15 – 7.
- 22.
Bonde JP, Hjollund NH, Jensen TK et al. A follow-up study of environmental and biologic determinants of fertility among 430 Danish first-pregnancy planners: design and methods. Reprod Toxicol 1998; 12: 19 – 27.
- 23.
Guzick DS, Overstreet JW, Factor-Litvak P et al. Sperm morphology, motility, and concentration in fertile and infertile men. N Engl J Med 2001; 345: 1388 – 93.
- 24.
Slama R, Eustache F, Ducot B et al. Time to pregnancy and semen parameters: a cross-sectional study among fertile couples from four European cities. Hum Reprod 2002; 17: 503 – 15.
- 25.
Comhaire FH, Vermeulen L, Hinting A et al. Accuracy of sperm characteristics in predicting the in vitro fertilizing capacity of semen. J In Vitro Fert Embryo Transf 1988; 5: 326 – 31.
- 26.
Hinting A, Comhaire F, Schoonjans F. Capacity of objectively assessed sperm motility characteristics in differentiating between semen of fertile and subfertile men. Fertil Steril 1988; 50: 635 – 9.
- 27.
Dam AH, Feenstra I, Westphal JR et al. Globozoospermia revisited. Hum Reprod Update 2007; 13: 63 – 75.
- 28.
Hanevik HI, Friberg UM, Bergh A et al. Spermieuthenting fra testikkel for assistert befruktning ved azoospermi Tidsskr Nor Lægeforen 2007; 127: 2504 – 6.
- 29.
Jequier AM. The importance of diagnosis in the clinical management of infertility in the male. Reprod Biomed Online 2006; 13: 331 – 5.