Background.
Lung cancer is a common malignancy. Positron emission tomography (PET) has become an important tool in the staging of the disease with regard to operability and in order to determine radiation volume when surgery is not indicated.
Materials and methods.
We have assessed and discuss results recently published in major international journals.
Results.
In approximately 60 % of the patients, the planning of treatment is modified after a PET investigation.
Interpretation.
In contrast to the state the art in most industrialised countries, dedicated PET is not available in Norway. Hence lung cancer is suboptimally treated.
Lungekreft er den fjerde hyppigste kreftform i Norge, med nær 2 000 nye tilfeller per år. Sykdommen er den ledende årsak til kreftdød samlet for kvinner og menn, med en femårsoverlevelse på ca. 10 %. Insidensen er økende, sannsynligvis betinget i en økning av antall kvinnelige røykere. Røyking antas å være årsak til nær 90 % av alle lungekrefttilfellene. Lungekreft er dermed en livsstilssykdom, og forebyggende helsetiltak har i mange år vært et satsingsområde (1). Ikke minst har Helsedirektoratets seneste antirøykekampanje vakt betydelig oppsikt.
Preoperativ diagnostikk og behandling av lungekreft er tidligere beskrevet i Tidsskriftet (2) – (4), men bruk av positronemisjonstomografi (PET) ble kun berørt perifert (5).
Hva er PET?
PET er en forkorting for positronemisjonstomografi, en nukleærmedisinsk avbildningsmetode hvor det radiofarmasøytiske preparatet som benyttes er en positronemitter. De mest brukte positronemitterende radionukleider er karbon, oksygen, nitrogen og fluor. Fordelene ved å benytte en positronemitter fremfor en gammaemitter, som anvendes ved vanlige nukleærmedisinske undersøkelser, er mulighetene til å merke naturlige biologiske stoffer. Samtidig gir positronemisjon langt høyere bildeoppløsning enn konvensjonell gammakameraavbildning. PET har imidlertid dårlig anatomisk bildeoppløsning sammenliknet med computertomografi (CT). Et moderne PET-instrument er derfor bygd sammen med en CT-maskin for automatisk bildesammensmeltning, slik at et anatomisk bilde fra den integrerte CT kan brukes til å lokalisere et PET-funn. Samtidig benyttes den integrerte CT til en meget rask attenuasjonskorreksjon, slik at en helkroppsundersøkelse tar mindre enn 30 minutter.
Det vanligste radiofarmasøytiske preparatet som benyttes for PET er 18F-fluoro-2-deoksiglukose (FDG). Mange maligne tumorer, inkludert lungekreft, har økt glukoseopptak, glukoseomsetning og retensjon av dette stoffet. Også ved PET-undersøkelser av hjerte og hjerne er dette preparatet det vanligste radiofarmakon.
Ved Rikshospitalet og ved Radiumhospitalet er det i dag mulig å utføre PET med FDG ved hjelp av et modifisert gammakamera, såkalt fattigmanns-PET. En vanlig PET-helkroppsundersøkelse med gammakamera tar to timer, har rimelig god spesifisitet, men langt dårligere sensitivitet enn et dedikert PET-kamera (6, 7).
Stadieinndeling og behandling
Ikke-småcellet lungekreft utgjør 75 % av alle lungekrefttilfeller. Operativ behandling er eneste kurative mulighet, selv om også noen inoperable pasienter tilbys strålebehandling med kurativ intensjon. Utvelgelse av pasienter til operasjon er derfor meget viktig, og PET-undersøkelse har fått stor betydning i denne prosessen. For ikke-operable pasienter med ikke-småcellet lungekreft og for pasienter med begrenset småcellet lungekreft vil PET være til betydelig hjelp for å avgrense strålevolumet for strålebehandling (8) – (10). Småcellet lungekreft oppfattes som systemisk uavhengig av stadium ved diagnosetidspunkt, og opereres sjelden (1).
Kurativ behandling av lungekreft består i meget omfattende kirurgi med lang rekonvalesens, ikke ubetydelig morbiditet og en dødelighet på 1 – 5 % (11, 12). Kirurgi er som oftest ikke livsforlengende der det er spredning. Et stort invasivt inngrep hos en pasient som vil dø av metastaser vil kunne medføre betydelig redusert livskvalitet den tiden pasienten har igjen å leve. Stadiene IA og IIA (tumor mindre enn 3 cm, henholdsvis uten eller med spredning til peribronkiale/ipsilaterale lymfeknuter i hilus) og IB og IIB (tumor over 3 cm, mer enn 2 cm fra carina, henholdsvis uten eller med spredning til peribronkiale/ipsilaterale lymfeknuter i hilus) defineres som teknisk operable og har en overlevelse på henholdsvis 67 %, 55 %, 57 % og 39 % (1). Har pasientene tumor i stadium III eller IV med lymfeknuter i øvrige mediastinum og/eller metastaser, tilbys oftest multimodal terapi med utgangspunkt i strålebehandling.
PET og lungekreft
Felles for det meste av nyere internasjonal litteratur som omhandler stadieinndeling og evaluering av operabilitet av lungekreft, er at PET beskrives som et uunnværlig verktøy i primærutredningen av ikke-småcellet lungekreft (7, 13) – (15). I USA er ikke kirurgi refusjonsberettiget uten en foregående PET-evaluering.
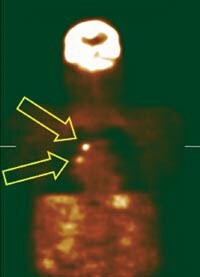
En metaanalyse, som omfatter 16 studier med til sammen 894 pasienter, viste at etter PET-undersøkelse ble stadieinndeling på grunnlag av lymfeknuter i mediastinum (fig 1) endret hos 16,7 % (8). En lavere prosentvis andel ble nedgradert til stadiene I eller II, og derfor operable (14 %), enn de som ble oppgradert til stadiene III eller IV, som ikke-operable (23 %). Ho og medarbeidere rapporterer videre at PET-undersøkelse var meget robust i differensiering mellom stadiene II og III og at PET-undersøkelsen hadde en meget høy negativ prediktiv verdi. Dersom PET-undersøkelse ikke viser lymfeknutemetastaser i mediastinum eller perifere metastaser, kan pasienten opereres. Spesifisiteten ble beregnet til 92,2 %, men det forekommer noen falskt positive undersøkelser. Forfatterene anbefaler derfor at en positiv undersøkelse etterfølges av kirurgisk stadieinndeling for å sikre at ingen pasienter mister muligheten til potensielt kurativ behandling (8).
I en prospektiv studie publisert i 2001 ble behandlingsstrategien for 153 pasienter først lagt opp i henhold til vanlig diagnostisk utredning, og på nytt etter gjennomføring av en PET-undersøkelse. PET-funn førte til endret stadieinndeling hos 43 % av pasientene, og hos hele 60 % ble behandlingen modifisert. For 34 pasienter (22 %) ble stadieinndelingen etter PET-undersøkelse endret fra kurativt behandlingsmål til palliativ behandling. Av 88 pasienter initialt klassifisert til stadiene III og IV, ble 13 (15 %) reklassifisert til stadiene I og II som et resultat av PET-undersøkelsene. Toårsoverlevelsen i gruppen som fikk kurativ behandling etter PET-diagnostikk ble estimert til vel 60 % (9).
I en sammenlikning av antall unødvendige torakotomier hos pasienter randomisert til utredning med eller uten PET unngikk 20 % unødvendig kirurgi/mediastinoskopi (14).
Metastaser til binyrene er en utfordring for konvensjonell bildediagnostikk, med diagnostiske vanskeligheter hos opptil 78 % av pasientene etter CT og MR. PET har meget høy sensitivitet for metastaser til binyrene (6, 16, 17).
En simulasjonsstudie fra 2000 viste at PET-CT i stedet for CT alene vil gi signifikant korreksjon av strålevolumet mot primærtumor og patologiske lymfeknuter (10). Hos 62 % av pasientene vil strålevolumet bli endret – redusert hos 40 % av pasientene og utvidet hos 22 %.
Diskusjon
De refererte studiene viser at nær 40 % av pasientene som ble tilbudt kurativ behandling etter PET-undersøkelse, vil dø i løpet av oppfølgingsperioden på to år. PET med FDG er derfor ikke en endelig løsning på problemet med stadieinndeling hos pasienter med ikke-småcellet lungekreft. Men når diagnosen hos mellom 5 % og 14 % av pasientene nedgraderes fra ikke-operabel til operabel sykdom, gir det grunn til å regne med at mange pasienter som i dag klassifiseres som ikke-operable, ville blitt operert dersom PET hadde vært benyttet i utredningen.
Ut fra tilgjengelig litteratur er det rimelig å anta at av de 160 som årlig opereres for lungekreft i Norge, burde vel 30 pasienter ikke vært operert og minst 15 andre burde vært tilbudt potensielt kurativ kirurgi.
Selv om positive PET-funn oftest bør verifiseres med torakotomi eller kirurgisk biopsi, bør PET-undersøkelse med sin høye negative prediktive verdi bli et tilbud også til norske pasienter. Mediastinoskopi hvor det plukkes lymfeknuter med positivt FDG-opptak etter PET, må være langt å foretrekke fremfor blind mediastinoskopi med biopsi av alle tilgjengelige lymfeknuter. Tilnærmet alle som blir operert på galt grunnlag dør, til dels etter et slitsomt postoperativt forløp. I nasjonalt handlingsprogram for lungekreft etterlyser man bedre data for stadieinndeling og TNM-klassifikasjon, slik at overlevelsesanalyser blir basert på kvalitetssikret diagnostikk og stadieutredning (1). Kliniske studier viser at man ved hjelp av PET-undersøkelse påviser fjernmetastaser hos 5 – 15 % av pasientene hvor metastaser ikke ble påvist før undersøkelsen og avkrefter mistanker om metastaser hos 5 – 10 % av pasientene (15). Vi vil anta at PET vil kunne yte et vesentlig bidrag til bedre TNM-klassifikasjon hos pasienter med lungekreft.
PET er blitt et uunnværlig klinisk redskap i den preoperative diagnostiske utredning av lungekreft i hele den industrialiserte verden – med unntak av Norge! I verden for øvrig er diskusjonen ikke lenger PET versus ikke-PET, men om PET med integrert CT bør være standarden for denne pasientgruppen (18).
Oppgitte interessekonflikter: Ingen
Hovedbudskap
PET er et viktig redskap i diagnostisk utredning av lungekreft i hele den industrialiserte del av verden – med unntak av Norge
- 1.
Lungekreft 2000 – diagnostikk og behandling. Nasjonalt handlingsprogram. 1. utg. Oslo: Norsk Lungecancergruppe og Den Norske Kreftforening.
- 2.
Bremnes RM, Aasebø U. Lungekreft – en lavstatussykdom? Tidsskr Nor Lægeforen 2002; 122: 2257.
- 3.
Rostad H, Naalsund A, Jacobsen JNR, Aaløkken TM. Er behandlingen av lungekreft i Norge god nok? Tidsskr Nor Lægeforen 2002; 122: 2258 – 62.
- 4.
Heitmann EP, Alexandersen O, Moland J. Er mediastinoskopi et nødvendig preoperativt inngrep ved ikke-småcellet lungekreft? Tidsskr Nor Lægeforen 2002; 122: 2268 – 9.
- 5.
Bach-Gansmo T, Bogsrud TV. Lungekreft. Tidsskr Nor Lægeforen 2002; 122: 2559.
- 6.
Vansteenkiste JF, Stroobants SG. The role of positron emission tomography with 18fluoro-2-deoxy-D-glucose in respiratory oncology. Eur Respir J 2001; 17: 802 – 20.
- 7.
Fischer BMB, Mortensen J, Høigaard L. PET in the diagnosis and staging of lung cancer – a systematic, quantitative review of the literature. Lancet Oncol 2001; 2: 659 – 66.
- 8.
Ho Shon I, O’Dohert MJ, Maisey MN. Positron emission tomography in lung cancer. Semin Nucl Med 2002; 32: 240 – 71.
- 9.
Hicks RJ, Kalff V, MacManus MP, Ware RE, Hogg A, McKenzie AF et al. Fluorine-18 fluorodeoxyglucose (FGD) PET provides high impact and powerful prognostic stratification in staging newly diagnosed non-small cell lung cancer. J Nucl Med 2001; 42: 1596 – 604.
- 10.
Vanytsel LJ, Vansteenkiste JF, Stroobants SG, De Leyn PR, De Wever W, Verbeken EK et al. The impact of 18F-Fluoro-2-deoxy-D-glucose positron emission tomography (FDG-PET) lymph node staging on the radiation treatment volumes in patients with non-small cell lung cancer. Radiother Oncol 2000; 55: 317 – 24.
- 11.
Dahle G, Brøyn T, Stavem K. Kirurgisk behandling av ikke-småcellet lungekreft Tidsskr Nor Lægeforen 2003; 123: 1525 – 6.
- 12.
Pearson FG. Non-small cell lung cancer. Role of surgery for stages I-III. Chest 1999; 116 (suppl 3): 500S-3S.
- 13.
Coleman RE. PET in lung cancer. J Nucl Med 1999; 40: 814 – 20.
- 14.
van Tinteren H, Hoekstra OS, Smith E, van den Bergh JH, Schreurs AJ, Stallaert RA et al. Effectiveness of positron emission tomography in the preoperative assessment of patient with suspected non-small-cell lung cancer. Lancet 2002; 359: 1388 – 92.
- 15.
Pieterman RM, van Putten JW, Meuzelaar JJ, Mooyaart EL, Vaalburg W, Koeter GH et al. Preoperativ staging of non-small-cell lung cancer with positron emission tomography. N Engl J Med 2000; 343: 254 – 61.
- 16.
Erasmus JJ, Patz EF jr., McAdams HP, Murray JG, Herndon J, Coleman RE et al. Evaluation of adrenal masses in patients with bronchogenic carcinoma using 18F-FDG PET. AJR Am J Roentgenol 1997; 168: 1357 – 60.
- 17.
Porte HL, Ernst OJ, Delebecq T, Metois D, Lemaitre LG, Wurtz AJ. Is computed tomography guided biopsy still necessary for the diagnosis of adrenal masses in patients with resectable non-small-cell-lung cancer? Eur J Cardiothorac Surg 1999; 15: 597 – 601.
- 18.
Lardinois D, Weder W, Hany TF, Kamel EM, Korom S, Seifert B et al. Staging of non-small-cell lung cancer with integrated positron-emission tomography and computed tomography. N Engl J Med 2003: 348: 2500 – 7.