Background.
It is not known to what extent information on previously unknown adverse reactions is communicated to doctors after the approval of a new drug.
Material and methods.
We included seven drugs, approved between 1982 and 1995 and the first in their class to be approved in Norway. We recorded the number of adverse reactions listed in the annual editions of the Norwegian physicians’ desk reference(Felleskatalogen) from the first edition that included the drug and up until the 2001 edition.
Results.
Only 51 % of the adverse reactions listed in the 2001 edition were included in the first post-approval edition. On average, 1.6 new adverse reactions were added for each drug every year. By contrast: in a group of 12 drugs approved before 1970, 0.14 new adverse reactions were added for each drug every year between 1989 and 2001.
Interpretation
. With a new drug it is to be expected that many adverse reactions are not acknowledged as such. Caution is warranted because of the fact that even though it is not listed in the physicians’ desk reference, any event appearing in a patient exposed to a new drug may be an adverse reaction.
Etter at et legemiddel har fått markedsføringstillatelse og er blitt tatt i vanlig klinisk bruk, oppdages det ofte bivirkninger som ikke var kjent tidligere (1, 2). Den viktigste årsaken til dette er at et legemiddel vanligvis bare prøves ut på et begrenset antall pasienter, i beste fall noen få tusen, før det godkjennes. Dessuten ekskluderes ofte presumptivt bivirkningsfølsomme pasienter, slik som eldre, personer med andre sykdommer og individer som bruker andre legemidler. I de kliniske studiene som ligger til grunn for godkjenning, er det dermed i praksis svært vanskelig å oppdage bivirkninger som har en frekvens som er lavere enn ca. 1 : 200 – 1 : 1 000 (3, 4).
En nylig publisert undersøkelse fra USA viste at rundt 3 % av alle legemidler som var godkjent i perioden 1975 – 99, senere ble trukket tilbake på grunn av bivirkninger, mens 8 % fikk betydelige restriksjoner på bruken (2). Disse tallene er i overensstemmelse med det man har funnet i europeiske studier (5) – (7). Den gjennomsnittlige tiden fra et legemiddel blir godkjent til det blir trukket tilbake eller får betydelige bruksrestriksjoner, varierer fra to til åtte år i ulike studier (2, 8).
Selv om det dermed eksisterer noe kunnskap om hvor ofte og hvor lang tid etter godkjenning nye alvorlige bivirkninger erkjennes, finnes det ingen studier som generelt sett har belyst i hvor stor grad det kommer frem opplysninger om bivirkninger som ikke var kjent på registreringstidspunktet. Formålet med vår studie var å tallfeste i hvilken grad det beskrives nye bivirkninger, forsiktighetsregler og kontraindikasjoner i produktomtalene i Felleskatalogen de første årene etter at legemidler er blitt godkjent i Norge.
Materiale og metode
De legemidlene som er inkludert i studien, ble valgt ut fra følgende forhåndsdefinerte kriterier:
Legemidlene skulle være de første som ble godkjent i Norge i sin gruppe. Dette ble gjort for å unngå at legemidlets bivirkninger skulle kunne forutsies ut fra tidligere erfaring med andre legemidler i samme gruppe (9).
Legemidlene skulle ha vært markedsført i Norge i minimum fem år og maksimum 20 år. Dette ble gjort for å få en viss minste observasjonstid samtidig som legemidlene ikke skulle være så gamle at bivirkningsovervåkingen skjedde etter metoder vesentlig forskjellig fra de som brukes i dag.
Legemidlene skulle tilhøre legemiddelgrupper som brukes i utstrakt grad i Norge.
Ut fra disse kriteriene ble det først godkjente preparatet i sju legemiddelgrupper inkludert i studien. De sju gruppene var kolesterolsenkende statiner, selektive serotoninreopptakshemmere, hemmere av angiotensinkonverterende enzym (ACE-hemmere), protonpumpehemmere, benzodiazepinliknende sovemidler, bisfosfonater og angiotensinreseptorantagonister. De aktuelle legemidlene og godkjenningsåret i Norge er presentert i tabell 1. De samme legemidlene var først i sin gruppe også på verdensmarkedet (tab 1).
Tabell 1
Legemidler inkludert i studien
| Substansnavn |
Kaptopril |
Omeprazol |
Lovastatin |
Fluvoksamin |
Zopiklon |
Losartan |
Etidronat |
| Preparatnavn |
Capoten |
Losec |
Mevacor |
Fevarin |
Imovane |
Cozaar |
Didronate |
| Godkjent for første gang på verdensmarkedet (år) |
1981 |
1988 |
1987 |
1983 |
1984 |
1994 |
1977¹ |
| Godkjent i Norge (år) |
1982 |
1989 |
1989 |
1990 |
1994 |
1995 |
1995 |
| Antall år på verdensmarkedet før godkjenning i Norge |
1 |
1 |
2 |
7 |
10 |
1 |
18 |
| Antall land legemidlet var godkjent i før godkjenning i Norge |
43 |
5 |
12 |
> 28 |
ca. 50 |
2 |
15² |
| Antall pasienter inkludert i kliniske studier før godkjenning i Norge |
> 8 000 |
2 183 |
> 1 250 |
ca. 1 600 |
ca. 24 000 |
> 2 900 |
ca. 7 000 |
| Antall år omtalt i Felleskatalogen |
18 |
13 |
12 |
11 |
7 |
7 |
6 |
| Antall bivirkninger i første aktuelle utgave av Felleskatalogen |
28 |
6 |
42 |
10 |
12 |
5 |
19 |
| Antall bivirkninger i Felleskatalogen 2001 |
31 |
47 |
54 |
59 |
11 |
13 |
22 |
| Antall bivirkninger i fullstendig preparatomtale 2001 |
41 |
47 |
54 |
– ³ |
– ³ |
13 |
22 |
| Netto økning i antall bivirkninger i Felleskatalogen |
3⁴ |
41 |
12 |
49 |
–1⁵ |
8 |
3 |
| [i] | |||||||
[i] 1 Gjelder på indikasjonen Pagets sykdom. På indikasjonen osteoporose ble legemidlet første gang godkjent i 1990
2 Gjelder på indikasjonen osteoporose. Kan ha vært godkjent i flere land på indikasjonen Pagets sykdom
3 Fullstendig preparatomtale ikke godkjent av Statens legemiddelverk
4 Det tilkom fire nye bivirkninger, mens en («enkelte dødsfall er rapportert») ble fjernet
5 Et fenomen («risiko for tilvenning») ble overflyttet fra bivirkninger til forsiktighetsregler i løpet av observasjonsperioden
Preparatomtalene i Felleskatalogen ble brukt for å fremskaffe informasjon om bivirkninger, forsiktighetsregler og kontraindikasjoner år for år fra og med det første året de aktuelle legemidlene ble omtalt og til og med 2001-utgaven (10). Felleskatalogen ble valgt fordi dette er norske legers klart viktigste kilde til informasjon om legemiddelbivirkninger. Før 1.1. 1994 ble alle preparatomtalene i Felleskatalogen godkjent av Statens legemiddelkontroll (nå Statens legemiddelverk). Etter denne datoen var det i henhold til EØS-reglene i stedet produktenes fullstendige preparatomtale (summary of product characteristics, SPC) som skulle godkjennes, og preparatomtalene i Felleskatalogen skulle bygge på disse tekstene. Vi har derfor for sammenlikningens skyld også sett på den informasjonen som blir gitt om bivirkninger i de aktuelle fullstendige preparatomtalene (SPC-tekstene).
Legemiddelprodusentene ble tilskrevet og spurt om hvilket år deres preparat ble lansert på verdensmarkedet, når det ble godkjent i Norge, hvor mange land det hadde vært godkjent i før det ble godkjent i Norge, og hvor mange pasienter som hadde deltatt i kliniske studier før det ble godkjent i Norge.
De aktuelle legemidlene var omtalt i Felleskatalogen over en periode fra seks år (f.o.m. 1996/97-utgaven t.o.m. 2001-utgaven) til 18 år (f.o.m. 1984-utgaven t.o.m. 2001-utgaven) (tab 1). Siden bare to av legemidlene var omtalt i mer enn 12 år, ble de systematiske beregningene avsluttet etter 12 år. For legemidler som hadde vært omtalt i Felleskatalogen i mindre enn 12 år, ble antallet bivirkninger etter det siste observasjonsåret satt til samme antall som i det siste året.
Samtlige bivirkninger ble klassifisert etter hyppighet, alvorlighetsgrad, type og hvilket organsystem bivirkningen rammet. Inndelingen etter hyppighet og organsystem ble gjort etter produktomtalen i Felleskatalogen. For legemidler der dette manglet, ble data fra svenske FASS (11) benyttet. For å dele inn bivirkningene i alvorlige og ikke-alvorlige ble Verdens helseorganisasjons Critical terms list (12) brukt. Inndelingen i type A-bivirkninger (doseavhengige reaksjoner som skyldes legemidlets farmakologiske egenskaper) og type B-bivirkninger (immunologiske eller idiosynkratiske reaksjoner) ble gjort ut fra vanlig aksepterte kriterier (13).
Til sammenlikning valgte vi ut noen legemidler som var blitt godkjent i Norge før 1970 og som skulle være det første eller det ledende legemidlet i store legemiddelgrupper. Videre skulle disse preparatene ha vært på markedet i hele perioden 1970 – 2001. Ut fra dette ble følgende legemidler inkludert i denne gruppen: warfarin (Marevan), digitoksin (Digitrin), glyseroltrinitrat (Nitroglycerin), furosemid (Lasix), prednisolon (Prednisolon), fenoksymetylpenicillin (Weifapenin), acetylsalisylsyre (Dispril), morfin (Morfin), klorpromazin (Largactil), diazepam (Vival), amitriptylin (Sarotex) og deksklorfeniramin (Polaramin). Siden de systematiske beregningene ble avsluttet etter 12 år for de nye legemidlene, ble 12-årsperioden 1989 – 2001 valgt ut som undersøkelsesperiode i denne gruppen.
Statistisk sammenlikning ble gjort med Wilcoxons rangsumtest og lineær regresjonsanalyse. P-verdier <= 0,05 ble ansett å være statistisk signifikante.
Resultater
Bakgrunnsdata for de sju nye legemidlene som inngikk i studien presenteres i tabell 1. Til sammen var det beskrevet 122 bivirkninger for disse legemidlene i de første preparatomtalene som ble utgitt etter godkjenning av respektive preparat. I 2001-utgaven av Felleskatalogen (10) var det tilsvarende tallet 237. Dermed var bare 51 % av bivirkningene omtalt ved godkjenningstidspunktet for legemidlene. Nettoøkningen i antall bivirkninger i løpet av observasjonsperioden var 115, men fordi to bivirkninger var blitt fjernet (tab 1), var det kommet til 117 nye bivirkninger. Dette tilsvarer en økning på 98 %, eller i gjennomsnitt 1,6 bivirkninger per preparat per år. I figur 1 vises den gjennomsnittlige bivirkningsutvilklingen år for år. Til sammenlikning var det i gruppen av legemidler godkjent før 1970 en gjennomsnittlig økning i antall bivirkninger på 12 % i perioden 1989 – 2001, eller 0,14 bivirkninger per legemiddel per år (p = 0,05 versus de nye legemidlene). Åtte av de 12 gamle preparatene (67 %) hadde identiske bivirkningsomtaler i 1989 og i 2001.
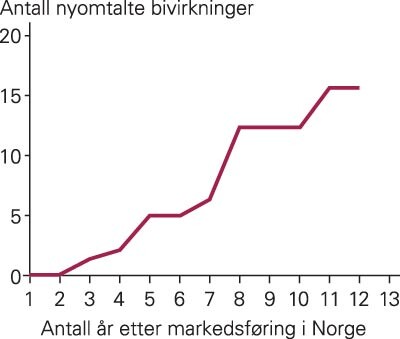
Bivirkningsavsnittene i preparatomtalene i Felleskatalogen for 2001 og i de fullstendige norske preparatomtalene skilte seg lite fra hverandre (tab 1). For fire av preparatene var de to tekstene identiske, mens ett legemiddel hadde flere bivirkninger omtalt i den fullstendige preparatomtalen enn i Felleskatalogen. For de to siste preparatene hadde Statens legemiddelverk ennå ikke godkjent noen fullstendig preparatomtale, slik at Felleskatalogteksten fortsatt gjaldt som offisielt godkjent produktomtale ved undersøkelsestidspunktet.
For de sju nye legemidlene økte de sjeldne bivirkningene signifikant mer enn de hyppige bivirkningene ( (2)). Etter 12 år var det en gjennomsnittlig økning på 10,0 sjeldne bivirkninger per legemiddel, mens det for hyppige og mindre hyppige bivirkninger var en økning på henholdsvis 2,2 og 3,5 per legemiddel (p < 0,05 for sjeldne versus hyppige og p < 0,15 for sjeldne versus mindre hyppige bivirkninger). Økningen i ikke-alvorlige og alvorlige bivirkninger presenteres i figur 3. Etter 12 år var den gjennomsnittlige økningen på henholdsvis 11,1 og 4,9 bivirkninger per legemiddel, men denne forskjellen var ikke statistisk signifikant (p > 0,20).

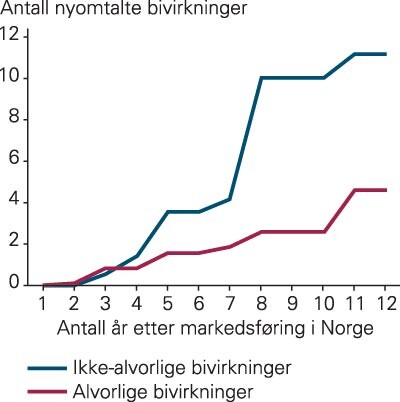
Av de 117 nye bivirkningene kunne 36 (31 %) klassifiseres som type A-bivirkninger og 36 (31 %) som type B-bivirkninger, mens de øvrige 45 (38 %) var uklassifiserbare. Det var ingen klar forskjell i økningen blant type A- og type B-bivirkninger, selv om det var en tendens til at type A-bivirkningene ble kjent noe tidligere.
Legemidlene hadde vært på markedet i 2 – 50 land og i 1 – 18 år før de ble godkjent i Norge (tab 1). Det var ingen signifikant sammenheng mellom antall land et preparat hadde vært godkjent i eller antall år det hadde vært godkjent før det kom til Norge og antall nyomtalte bivirkninger i Felleskatalogen etter godkjenning i Norge (p = henholdsvis 0,47 og 0,63).
Legemidlene hadde før godkjenning i Norge vært gjenstand for kliniske utprøvninger der fra rundt 1 250 til ca. 24 000 pasienter hadde deltatt (tab 1). Forholdet mellom antall pasienter som hadde vært inkludert i kliniske studier før godkjenning i Norge og antall nyomtalte bivirkninger i Felleskatalogen etter godkjenning i Norge illustreres i figur 4.
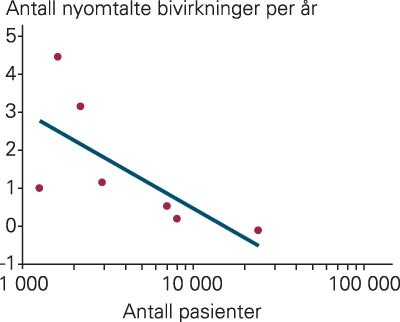
Antall kontraindikasjoner og forsiktighetsregler økte gradvis med tiden etter godkjenning. I løpet av 12 år var det en netto tilvekst på i gjennomsnitt 0,6 kontraindikasjoner og 1,3 forsiktighetsregler per legemiddel.
Diskusjon
I denne studien er det inkludert kun sju legemidler, og det er derfor et åpent spørsmål i hvor stor grad resultatene er representative for andre legemidler. Imidlertid dekker de inkluderte legemidlene store og viktige terapiområder, slik at det, selv om materialet er lite, dreier seg om legemidler og legemiddelgrupper som svært mange kommer i kontakt med. Det at legemidlene representerer forskjellige terapiområder, vil også bidra til å øke generaliserbarheten.
Felleskatalogen er brukt som kilde i studien siden dette er norske legers viktigste oppslagsverk for bivirkninger. Samtidig er det legemiddelprodusentenes viktigste arena for informasjon. I løpet av studieperioden ble prosedyrene for godkjenning av innholdet i preparatomtalene i Felleskatalogen endret, men denne omleggingen er ennå ikke sluttført og for noen av de studerte preparatene eksisterte det ikke godkjente norske fullstendige preparatomtaler ved undersøkelsestidspunktet. Formatene for bivirkningsavsnittene i Felleskatalogen og i de fullstendige preparatomtalene er forskjellige, og det var ikke for noe legemiddel mulig å skaffe til veie fullstendige preparatomtaler for hele undersøkelsesperioden. Av denne grunn valgte vi å la være å inkludere informasjon fra de fullstendige preparatomtalene i våre beregninger.
Det finnes ikke spesifikke krav til hvor mye som skal stå om et legemiddels bivirkninger i Felleskatalogen. For ett preparat i vår studie var bivirkningsavsnittet i den fullstendige preparatomtalen mer omfattende enn i Felleskatalogen, og det finnes eksempler på at firmaer har utelatt klinisk viktige bivirkningsopplysninger fra Felleskatalogens preparatomtale til tross for at de har vært angitt i den fullstendige, godkjente preparatomtalen (14).
De fullstendige preparatomtalene som er godkjent i Norge, er heller ikke nødvendigvis noen gullstandard når det gjelder bivirkningsinformasjon om et legemiddel. Det er til dels stor diskrepans mellom de norske og de svenske fullstendige preparatomtalene for ett og samme preparat, og det kan være forskjeller mellom synonympreparater godkjent i ett og samme land (15). For ett av preparatene i vår studie (Fevarin – som det ennå ikke finnes noen godkjent norsk fullstendig preparatomtale på) var faktisk den dokumentasjonen som fantes om bivirkninger i Felleskatalogen, mer omfattende enn den som fantes i de svenske og danske fullstendige preparatomtalene.
Vår studie viser at det fremfor alt er kunnskapen om et legemiddels sjeldne bivirkninger som øker etter godkjenningstidspunktet (fig 3). Dette er som ventet, siden det må inngå langt flere pasienter enn det som er vanlig i kliniske utprøvninger for å oppdage disse bivirkningene. For eksempel må 6 500 pasienter behandles med et legemiddel for at det med 95 % sannsynlighet skal opptre tre tilfeller av en bivirkning når den sanne insidensen er 1 : 1 000 (3). I vår studie var det bare tre av sju legemidler som hadde så mange pasienter inkludert i kliniske utprøvninger før godkjenning. At det ikke ble påvist noen signifikant forskjell mellom økningen i ikke-alvorlige og alvorlige bivirkninger (fig 4), skyldes trolig at materialet var for lite og dermed ikke hadde tilstrekkelig styrke for å kunne påvise dette.
Det var ikke mulig å påvise noen tydelig forskjell på frekvensen av type A- og type B-bivirkninger. Ut fra definisjonen ville man vente at type A-bivirkninger, som er vanlige og forutsigbare, skulle øke i mindre grad etter godkjenning, mens de mer uvanlige og uforutsigbare type B-bivirkningene ville forventes å øke mer. En forklaring på den manglende forskjellen kan være at såpass mange av bivirkningene var uklassifiserbare, slik at materialet var for lite for å kunne avdekke slike forskjeller. Det er også mulig at forskjellen var blitt tydeligere hvis vi ikke bare hadde inkludert det første legemidlet i hver legemiddelgruppe, siden type A-bivirkningene, som i regelen er gruppebivirkninger, da i langt større grad ville vært kjent fra tidligere.
Vi fant en tendens til at jo flere pasienter som hadde deltatt i kliniske utprøvninger, desto færre nye bivirkninger kom det til etter godkjenning i Norge. Forskjellen var ikke statistisk signifikant, men dette kan henge sammen med at materialet er lite. Resultatet antyder likevel at kliniske utprøvninger med kanskje rundt 5 000 inkluderte pasienter (der man kan anta at anslagsvis 70 – 80 % blir behandlet med det aktuelle legemidlet) er nødvendig for å få akseptabel kunnskap om et legemiddels bivirkninger ved godkjenningstidspunktet. Dette stemmer bra med beregninger som viser at det ellers vil være vanskelig å oppdage bivirkninger med en frekvens i størrelsesorden 1 : 1 000 eller lavere (3, 16).
Tidligere ble legemidler ofte godkjent i Norge relativt lang tid etter lansering på verdensmarkedet. Etter at EØS-avtalen trådte i kraft, vil legemidler bli godkjent raskere. Dette kan gi grunn til å frykte at enda færre bivirkninger vil være kjent ved godkjenningstidspunktet. Hvis dette ikke blir kompensert ved at det gjøres større kliniske studier før det søkes om godkjenning, noe som er lite trolig, er økt årvåkenhet de første årene etter godkjenning nødvendig. I denne perioden er det derfor spesielt viktig at man er oppmerksom på at et symptom som oppstår hos en pasient, kan være en bivirkning selv om det ikke er nevnt i Felleskatalogen eller i den fullstendige preparatomtalen for legemidlet. Terskelen for å rapportere slike mistenkte bivirkninger bør være lav. Selv med en optimal bivirkningsovervåking etter godkjenning vil det imidlertid ta tid før man har utfyllende kunnskap om et legemiddel, rett og slett fordi mange bivirkninger er så sjeldne at store, uselekterte pasientgrupper må ta midlet i bruk før det er mulig å oppdage dem.
Vi takker legemiddelfirmaene AstraZeneca, Aventis Pharma, Bristol-Myers Squibb, MSD (Norge), Roche Norge og Solvay Pharma, som bidrog med opplysninger om egne preparater.
Artikkelen bygger på en hovedoppgave ved Det medisinske fakultet, Norges teknisk-naturvitenskapelige universitet, vårterminen 2002
Interessekonflikter: Ingen
- 1.
Brewer T, Colditz G. Postmarketing surveillance and adverse drug reactions: current perspectives and future needs. JAMA 1999; 281: 824 – 9.
- 2.
Lasser KE, Allen PD, Woolhandler SJ, Himmlestein DU, Wolfe SM, Bor DH. Timing of new black box warnings and withdrawals for prescription medications. JAMA 2002; 287: 2215 – 20.
- 3.
Laurence DR, Bennett PN, Brown MJ. Clinical pharmacology. Edinburgh: Churchill Livingstone, 1997: 124.
- 4.
Kalant H, Roschlau WHE. Principles of medical pharmacology. New York: Oxford University Press, 1998: 791 – 8.
- 5.
Bakke OM, Wardell WM, Lasagna L. Drug discontinuation in the United Kingdom and the United States, 1964 to 1986: issues of safety. Clin Pharmacol Ther 1984; 35: 559 – 67.
- 6.
Bakke OM, Manocchia M, de Abajo F, Kaitin KI, Lasagna L. Drug safety discontinuations in the United Kingdom, the United States and Spain from 1974 through 1993: a regulatory perspective. Clin Pharmacol Ther 1995; 58: 108 – 17.
- 7.
Jefferys DB, Leakley DL, Lewis JA, Payne S, Rawlins MD. New active substances authorized in the United Kingdom between 1972 and 1994. Br J Clin Pharmacol 1998; 45: 151 – 6.
- 8.
Spriet-Pourra C, Auriche M. Drug withdrawal from the market for safety in the European countries: contributing reasons and implications. I: Fracchia GN, red. European medicines research. Amsterdam: IOS Press, 1994: 267 – 75.
- 9.
Kaufman DW, Shapiro S. Epidemiological assessment of drug-induced disease. Lancet 2000; 356: 1339 – 43.
- 10.
Felleskatalog over farmasøytiske spesialpreparater markedsført i Norge 2001. 43. utg. Oslo: Felleskatalogen AS, 2001.
- 11.
FASS. Läkemedel i Sverige 2001. Stockholm: LINFO Läkemedelsinformation AB, 2001.
- 12.
Critical terms list, December 2001. Uppsala: World Health Organisation Collaborating Centre for International Drug Monitoring, 2001.
- 13.
Gruchalla RS. Clinical assessment of drug-induced disease. Lancet 2000; 356: 1505 – 7.
- 14.
- 15.
Myhr K. Kan vi stole på preparatomtaler? Tidsskr Nor Lægeforen 2002; 122: 2644 – 6.
- 16.
Strom BL, red. Pharmacoepidemiology. 3. utg. Chichester: John Wiley & Sons, 2000.