Background.
A spinal cord injury changes body composition and metabolism over time. The main purpose of this article is to provide an overview of what is known about these changes and the consequences of those in the chronic phase, long after the acute injury.
Material and methods.
The article is based on own research and clinical experience, as well as a non-systematic search in the PubMed database.
Results.
The following has been documented for people with spinal cord injury: reduced bone and muscle mass, altered composition of muscle fibre, marked increase of body fat, decreased sensitivity to insulin and leptin and an increased activity in inflammatory signalling pathways. Changes are also demonstrated in hemostatic mechanisms and immune system.
Interpretation.
Changes in metabolism and hormonal regulation in people with spinal cord injury, may increase the risk of osteoporosis, obesity, cardiovascular disease and type 2 diabetes. Changed body composition and inflammatory activity may contribute to the higher incidence of cardiovascular disease and diabetes/metabolic syndrome, although other important risk factors (such as obesity and high blood pressure) may be absent. It has not been documented that changes in haemostatic mechanisms and the immune system are associated with the increased incidence of thromboembolic complications, severe infections or certain types of cancer.
En ryggmargsskadet pasient pådrar seg som regel umiddelbart synlige lammelser, tap av sensibilitet og autonome forstyrrelser som rammer både de naturlige funksjoner (vannlating, tarmtømming og seksualfunksjon), blodtrykk og temperaturreguleringen. Akuttfasen preges av spinalt sjokk og den akutte traumeresponsen (1). Forventet levealder etter ryggmargsskade har økt markert gjennom de siste tiårene. Likevel finner man at ryggmargsskadede personer i Norge fortsatt har høyere dødelighet av bl.a. pneumoni (16 %) og urogenitale sykdommer (13 %), og de har en økt risiko for å utvikle hjerte- og karsykdom, type 2-diabetes og osteoporose (2). For å bedre leveutsiktene til personer med kronisk ryggmargsskade kreves økt forståelse og ytterligere kartlegging av årsakene til økt sykdomsrisiko. I denne artikkelen gir vi en oversikt over metabolske forandringer hos ryggmargsskadede personer i en kronisk og mer stabil metabolsk fase.
Materiale og metode
Artikkelen er basert på egen forskning, klinisk erfaring og ikke-systematiske søk i databasen PubMed.
Forstyrrelser i beinmetabolismen
De fleste pasienter med ryggmargsskade utvikler raskt osteopeni i de affiserte deler av kroppen og senere en alvorlig grad av osteoporose med høy risiko for frakturer. Leddnære bløtdelstraumer kan gi lokal heterotop ossifikasjon, selv mange år etter skaden (3).
Historisk har beinskjørhet etter ryggmargsskade blitt vurdert som en konsekvens av den fysiske inaktiviteten som skaden medfører. Men beintapet etter ryggmargsskade er ofte mer alvorlig enn det man finner etter ren immobilisering og er observert å være progredierende i over ti år etter skaden (4). Nevrologisk skade og hormonelle forandringer er således også funnet å være av patogenetisk betydning (5). Eksempler på hormonelle endringer som kan påvirke beinmassen, og som er observert hos personer med ryggmargsskade, er høye kortison-, insulin- og leptinnivåer samt lave kjønnshormon-, gonadotropin-, veksthormon- og IGF-nivåer (5).
Innenfor en tidsperiode på ti uker etter skaden, og spesielt hos tidligere aktive unge gutter med komplette skader over Th5-nivået, ser man ofte forbigående hyperkalsemi, hyperkalsiuri og lave serumnivåer av parathyreoideahormon og 1,25(OH)₂-vitamin D (6). Demineralisering av de lange knoklene i underekstremitetene dominerer. Mest affisert er distale femur og proksimale tibia. Demineralisering og beintap skjer som regel ikke, eller i langt mindre grad, kranialt for skadenivået og i ryggsøylen (7).
Ved diagnostisering av beintap anses Dual emission X-ray absorptiometry (DEXA) som gullstandardmetoden (8). I dag behandles beinskjørhet hos ryggmargsskadede med funksjonell elektrisk stimulering (FES) (fig 1), ståtrening og medikamentell behandling (kalsium, fosfat, vitamin D og bisfosfanater). Studier viser at funksjonell elektrisk stimulering øker beintettheten hos pasientene (9).
Forstyrrelser i muskelmetabolismen
Etter en ryggmargsskade utvikles lammelser med varierende grad av muskelsvinn under skadenivået. Omfanget av muskelatrofien avhenger av om skaden rammer nedadgående nervebaner i ryggmargen (sentral skade), eller om den også rammer de motoriske forhorncellene (perifer skade). Perifer skade gir svær muskelatrofi og ses i lesjonsområdet der de tilhørende motornevronene er skadet, og etter skader av cauda equina. Muskler som har bevart normal nerveforsyning, vil derimot oftest være hypertrofiske som følge av mer bruk nå enn før skaden.
Den vanligvis lett spastiske lårmuskulaturen under skadenivået inneholder store mengder små type 2b-fibre, en del type 2a-fibre og så godt som ingen type 1-fibre, i motsetning til funksjonsfrisk muskulatur der ulike fibertyper er mer jevnt fordelt (10).
I armmuskulaturen over skadenivået dominerer typisk store type 1-fibre med rikelige mengder aerobe enzymer (11). Disse forhold gjenspeiler med stor grad av sannsynlighet både mengden og typen arbeidsbelastning disse musklene utsettes for etter en ryggmargsskade (9, 11). I dag har man ingen rutinemessig behandling av muskelhypotrofi under skadenivået etter en ryggmargsskade. Beinsykling med funksjonell elektrisk stimulering av sentralt denervert muskulatur etter komplette skader og vektavlastende tredemølletrening etter inkomplette (ufullstendige) skader ser ut til å gi en «normalisering» av muskelfibersammensetningen (med endring fra type 2b til type 2a, noen ganger også til type 1), muskelmassen og metabolske enzymer (9, 12) – (14).
Forstyrrelser i lipid- og glukosemetabolismen
Individer med ryggmargsskade har økt forekomst av hjerte- og karsykdom og type 2-diabetes. Likevel tyder studier på at personer med kronisk ryggmargsskade har en lik eller lavere, men økende, dødelighet av hjerte- og karsykdom sammenliknet med funksjonsfriske (15) – (19). I en norsk retrospektiv studie utført av Lidal og medarbeidere, døde 18 av i alt 142 ryggmargskadede personer (13 %) av hjerte- og karsykdom i perioden 1961 – 2002, noe som er mindre enn for funksjonsfriske i den samme tidsperioden (2).
Nedsatt glukosetoleranse, hyperinsulinemi, type 2-diabetes, ugunstig blodlipidprofil (lav HDL-kolesterol, høy totalkolesterol, høye triglyserider og høy LDL-kolesterol) er hyppigere registrert hos ryggmargskadede personer enn hos funksjonsfriske. Avvikene fra referanseområdene er størst ved komplette cervikale skader (19). Det er videre funnet holdepunkter for økt kalsiuminnhold i karveggene, noe som kan tyde på økt arteriosklerotisk byrde (20). Ryggmargsskadede personer med normal kroppsmasseindeks (BMI) har ofte redusert muskel- og beinmasse og økt mengde kroppsfett sammenliknet med funksjonsfriske med tilsvarende BMI (9). Den reduserte muskelmassen bidrar til lavere insulinstimulert helkroppsopptak av blodglukose. Glukosebelastning viser derfor forhøyede nivåer av både insulin og blodglukose (19). In vitro finner man imidlertid normalt insulinstimulert glukoseopptak over muskelcellemembranen (10). Redusert muskelmasse, mer bindevev og fett i musklene og forandret vaskularisering innvirker trolig sammen på insulinets effekt, internalisering og nedbrytning og kan føre til hyperinsulinemi (10). Redusert muskelmasse sammen med endret sympatisk nerveaktivitet (etter ryggmargsskader over 5. brystsegment), vil kunne redusere basalmetabolismen hos ryggmargsskadede personer med opptil 50 % sammenliknet med funksjonsfriske (21). Forlenget halveringstid for en del aminosyrer i blodet og økte konsentrasjoner av triglyserider og LDL-kolesterol øker insulinproduksjonen, som kan gi ytterligere fettdeponering.
Trening, røykeslutt og diett har positiv effekt på lipidprofilen også hos ryggmargsskadede personer. Trening i rullestol og armøvelser tre ganger i uken reduserte LDL-kolesterol med 25 % og økte HDL-kolesterol med 10 % (22). Funksjonell elektrisk stimulering har vist å ha en gunstig påvirkning på glukosemetabolismen og blodlipidene (14). Daglig energiforbruk hos personer med tetraplegi er funnet å være signifikant redusert. Dette skyldes først og fremst redusert fysisk aktivitet, men også redusert hvilestoffskifte (23). For å redusere risikoen for hjerte- og karsykdom og forstyrrelser i lipid- og glukosemetabolismen anbefales pasientene vektreduksjon ved normal kroppsmasseindeks (BMI) sammenliknet med funksjonsfriske, tilsvarende 4 – 6 kg (5 – 10 %) ved paraplegi, og 6 – 9 kg ved tetraplegi (10 – 15 %).
Forstyrrelser i hemostasen
Venøs tromboembolisme (dyp venetrombose og lungeemboli) er vanlige komplikasjoner etter ryggmargsskade. Høyest insidens av dyp venetrombose (38 %) og lungeembolier (5 %) er beskrevet de første tre månedene etter skade hos personer med paralytiske tilstander (24). Døgnvariasjonen, som man finner ved plasminogenaktivator-inhibitor 1 (PAI-1), TFPI (tissue factor pathway inhibitor), D-dimer, koagulasjonsfaktorene VII og VIII og protein C og protein S hos funksjonsfriske personer, kan være opphevet eller endret hos personer med ryggmargsskade (TFPI, fibrinspaltningsproduktet F1+2 og D-dimer) (25). Dette kan utgjøre en økt risiko for venøs tromboembolisme hos spinalskadede. I enkelte studier konkluderer man med at personer med ryggmargsskade rutinemessig bør screenes for venetrombose (26). Klinisk brukes ultralyd, CT, MR og biokjemiske markører (for eksempel D-dimer) kun diagnostisk. Profylaktisk behandling med elastiske strømper og kortkjedede hepariner i tre måneder etter skaden er kunnskapsbasert god praksis (27). Funksjonell elektrisk stimulering er i tillegg til å kompensere for normal muskelpumpe, vist å kunne normalisere fibrinolytisk aktivitet (28).
Infeksjoner og kreft
Det er observert nedsatt naturlig og adaptiv immunrespons og økte nivåer av cytokiner og interleukiner hos personer med ryggmargsskade (29, 30). De lave albuminnivåene i serum som registreres hos personer med høye ryggmargsskader i kronisk fase, oppfattes i dag som mulig indikator på en kronisk lett økt aktivitet i inflammatoriske signalkjeder. Funn av hemmet proliferasjon i alle hematopoetiske cellelinjer i desentralisert beinmarg, endret T-cellefunksjon og naturlig drepecellefunksjon kan redusere kroppens forsvar mot virus og «fremmede» celler (31, 32). Dette er interessante observasjoner i lys av at individer med spinalskade har økt risiko for å utvikle kreft i urinblære og muligens i tarm (33, 34). Nedsatt glukosetoleranse, insulinresistens og høye leptinnivåer er imidlertid også assosiert med nedsatt cellulær immunitet og kliniske infeksjoner (32). Forbedret immunitet er funnet etter gåtrening hos ryggmargsskadede personer (35).
Infertilitet og hypogonadisme
Det er påvist både redusert fertilitet og svekket ereksjons- og ejakulasjonsevne hos menn med ryggmargsskader (36, 37). Studier har vist økt antall spermier med unormal morfologi og nedsatt bevegelighet (36, 38). Ovarialfunksjonen er ikke affisert i kjent grad. I eget arbeid har vi funnet opptil 30 % lavere plasmanivåer av testosteron, luteiniserende hormon (LH) og follikkelstimulerende hormon (FSH) hos seks mannlige tetraplegikere sammenliknet med åtte funksjonsfriske (39). I andre studier er det imidlertid vist både høyere, lavere og normale plasmanivåer av testosteron, LH og FSH hos ryggmargsskadede menn (40). Ryggmargsskadede menn kan gjøre sin partner gravid på naturlig måte, men de fleste må enten bruke spesialinstrumenter for vibrasjonsstimulering eller elektrisk stimulering for å fremkalle ejakulat, som kan benyttes til in vitro-fertilisering. Dersom dette heller ikke lykkes, kan spermier hentes mikrokirurgisk fra epididymis til intracytoplasmatisk spermieinjeksjon.
Diskusjon
I den kroniske fasen etter ryggmargsskade finner man økt forekomst av hjerte- og karsykdom og type 2-diabetes. Det er nærliggende å knytte disse funn til samtidig påvisning av muskelhypotrofi og økt fettmasse (41), da dette danner grunnlag for nedsatt glukosetoleranse, insulinresistens, endring av fetthormoner og en ugunstig blodlipidprofil. Immobiliseringen sammen med nevrogene og hormonelle endringer bidrar sterkt til utviklingen av alvorlig osteoporose. Det er ennå ikke funnet klare sammenhenger mellom den økte forekomsten av venøs tromboembolisme og endringer i de hemostatiske mekanismene. Svekket immunforsvar og reduserte blodnivåer av androgene hormoner er i noen studier sett i sammenheng med henholdsvis hyppigere infeksjoner eller kreft og redusert fertilitet (42) (fig 2).
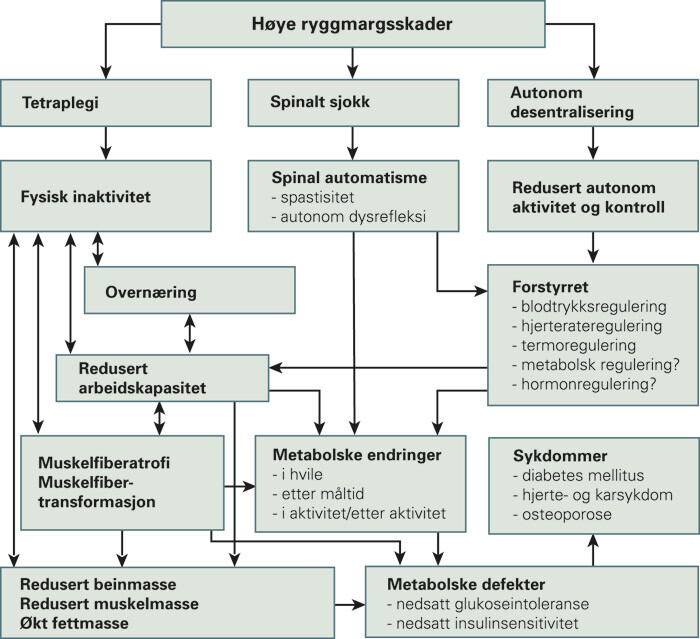
De nevnte forandringer kan fremfor alt relateres til langvarig ekstrem fysisk inaktivitet som følge av de fysiske lammelsene og til reguleringsforstyrrelser i det autonome nervesystemet. Det er naturlig å knytte sammen påviste risikofaktorer og økt hyppighet av hjerte- og karsykdom og type 2-diabetes, selv om den kausale sammenhengen ikke er dokumentert i prospektive langtidsstudier hos denne gruppen. Personer med ryggmargsskader over 6. torakale segment fremstår heller ikke med det komplette bildet av metabolsk syndrom, da blodtrykket ofte er lavt i sittende stilling, og de er utsatt for ortostatisk hypotensjon og blodtrykksfall i forbindelse med fysiske anstrengelser som følge av redusert sympatikustonus. Personer med skade under 6. torakale segment har derimot en tendens til hypertensjon på lang sikt, men har ikke samme risiko for type 2-diabetes som de med høyere skadenivåer.
Det eksisterer ikke egne retningslinjer for individuell primærforebygging og behandling av hjerte- og karsykdom og diabetes hos ryggmargskadede personer, selv om dette diskuteres (41). Likevel anbefales årlig sjekk av fastende blodsukker og blodlipider. Ved måling av blodtrykk hos personer med autonom dysrefleksi, bør ambulatoriske langtidsmålinger brukes. Dyptgripende endringer i kroppssammensetningen gjør at BMI ikke er egnet til å bedømme overvekt etter ryggmargsskade uten at en ny korrigert indeks blir tilgjengelig.
Den medikamentelle behandlingen av osteoporose hos ryggmargskadede personer skiller seg ikke ut fra den som gis til funksjonsfriske. Imidlertid har funksjonell elektrisk stimulering med sykling gitt positive resultater selv om dette fremdeles er relativt lite utbredt, særlig på grunn av kostnadene knyttet til selve instrumentet og liten brukervennlighet i hjemmet. Ståtrening og mobilisering brukes i dag i rehabilitering og i hjemmet, men dokumentasjon på at denne intervensjonen vedlikeholder beintettheten etter ryggmargsskade mangler. Det er en stor utfordring å reversere de katabole prosessene etter en ryggmargsskade. Man kan prøve å «kompensere» gjennom funksjonell elektrisk stimulering eller ved ekstra mye trening av den funksjonsfriske delen av kroppen. Det siste medfører imidlertid økt risiko for overbelastningsproblemer. Den sterkt reduserte muskelmassen medfører at serum-kreatinin er lavt, og en «normal» s-kreatinin hos en ryggmargsskadet person med omfattende muskelhypotrofi kan indikere begynnende nyresvikt. Risiko for nye tromboemboliske komplikasjoner er økt i forbindelse med sengeleie pga. interkurrente sykdommer også i kronisk fase. Ved slike anledninger anbefales forebyggende antikoagulasjonsbehandling.
Ennå vet vi lite om årsaker til en mulig immunsuppresjon etter ryggmargsskade. Forstyrret autonom regulering av mukøst og lymfoid vev og forandret signalering til immunregulerende nevroner i sentralnervesystemet bidrar sannsynligvis (43). Urinveisinfeksjoner bidrar til økt morbiditet og mortalitet etter ryggmargsskade (2, 16, 44). Dette skyldes først og fremst skadens forstyrrelse av den nervøse reguleringen av nedre urinveier som medfører resturin og som nødvendiggjør bruk av urinveiskatetre. Residiverende urinveisinfeksjoner øker risikoen for amyloide avleiringer og nyresvikt (45).
De viktigste predisponerende faktorer for lungesykdommer (pneumonier og atelektaser) og lungedød hos personer med ryggmargsskade er nedsatt hostekraft, økt bronkokonstriksjon og mukusproduksjon pga. uhemmet parasympatisk aktivitet (1, 46). Ny informasjon om immunforsvaret hos ryggmargsskadede individer har til nå ikke fått terapeutiske konsekvenser, selv om man i praksis er mindre restriktiv med bruk av antibiotika mot luftveis- og urinveisinfeksjoner.
Det er fortsatt manglende kunnskaper om hvilke hormonelle endringer en ryggmargsskade kan føre til og hvilke konsekvenser disse har for fertilitet og metabolisme. Medikamenter, det å sitte stille lenge, gjennomsnittlig forhøyet skrotal temperatur og stress er foreslått som medvirkende årsaker til redusert fertilitet (37). Det eksisterer ingen spesielle prosedyrer for å forebygge redusert fertilitet utover generelle tiltak som å forebygge urinveisinfeksjoner (inklusive epididymitt) og andre medisinske komplikasjoner som svekker almenntilstanden.
Konklusjon
Gjennomsnittlig forventet levetid øker stadig etter ryggmargsskade. Likevel er den gjennomsnittlige livslengden fremdeles redusert og komorbiditeten økt sammenliknet med funksjonsfriske (2). Flere studier har over tid gitt oss økt innsikt i bakenforliggende metabolske forandringer i den kronisk fasen. Dette øker mulighetene for både å kunne forebygge komplikasjoner og å gi bedre behandling når sykdommer inntreffer. Da det ikke vil være aktuelt å kunne kurere en ryggmargsskade i overskuelig fremtid, må ny kunnskap om metabolske og morfologiske forhold ut til fastlegen og den funksjonshemmede for å bidra til at helsen og behovene ivaretas bedre enn tidligere.
Oppgitte interessekonflikter:
Ingen
Tabell
| Hovedbudskap |
|
- 3.
Cipriano CA, Pill SG, Keenan MA. Heterotopic ossification following traumatic brain injury and spinal cord injury. J Am Acad Orthop Surg 2009; 17: 689 – 97. [PubMed]
- 6.
Bauman WA, Morrison NG, Spungen AM. Vitamin D replacement therapy in persons with spinal cord injury. J Spinal Cord Med 2005; 28: 203 – 7. [PubMed]
- 8.
Syed Z, Khan A. Bone densitometry: applications and limitations. J Obstet Gynaecol Can 2002; 24: 476 – 84. [PubMed]
- 9.
Hjeltnes N, Aksnes AK, Birkeland KI et al. Improved body composition after 8 wk of electrically stimulated leg cycling in tetraplegic patients. Am J Physiol 1997; 273: 1072 – 9. [PubMed]
- 10.
Aksnes AK, Hjeltnes N, Wahlstrom EO et al. Intact glucose transport in morphologically altered denervated skeletal muscle from quadriplegic patients. Am J Physiol 1996; 271: 593 – 600. [PubMed]
- 17.
Whiteneck GG, Charlifue SW, Frankel HL et al. Mortality, morbidity, and psychosocial outcomes of persons spinal cord injured more than 20 years ago. Paraplegia 1992; 30: 617 – 30. [PubMed]
- 19.
Bauman WA, Spungen AM. Carbohydrate and lipid metabolism in chronic spinal cord injury. J Spinal Cord Med 2001; 24: 266 – 77. [PubMed]
- 21.
Aksnes AK, Brundin T, Hjeltnes N et al. Meal-induced rise in resting energy expenditure in patients with complete cervical spinal cord lesions. Paraplegia 1993; 31: 462 – 72. [PubMed]
- 22.
Nash MS, Jacobs PL, Mendez AJ et al. Circuit resistance training improves the atherogenic lipid profiles of persons with chronic paraplegia. J Spinal Cord Med 2001; 24: 2 – 9. [PubMed]
- 26.
Furlan JC, Fehlings MG. Role of screening tests for deep venous thrombosis in asymptomatic adults with acute spinal cord injury: an evidence-based analysis. Spine 2007; 32: 1908 – 16. [PubMed]
- 28.
Katz RT, Green D, Sullivan T et al. Functional electric stimulation to enhance systemic fibrinolytic activity in spinal cord injury patients. Arch Phys Med Rehabil 1987; 68: 423 – 6. [PubMed]
- 29.
Nash MS. Known and plausible modulators of depressed immune functions following spinal cord injuries. J Spinal Cord Med 2000; 23: 111 – 20. [PubMed]
- 31.
Iversen PO, Hjeltnes N, Holm B et al. Depressed immunity and impaired proliferation of hematopoietic progenitor cells in patients with complete spinal cord injury. Blood 2000; 96: 2081 – 3. [PubMed]
- 32.
Frost FS, Pien LC. The immune system and inflammatory response in persons with SCI. I: Lin VW, Cardenas DD, red. Spinal cord medicine: principles and practice. New York, NY: Demos Medical Publishing, 2002: 213 – 21.
- 36.
Stien R. Seksuell dysfunksjon hos ryggmargsskadede menn. Tidsskr Nor Legeforen 2008; 128: 453-6. [PubMed]
- 37.
Elliot S. Sexual dysfuntion and infertility in men with spinal cord disorders. Lin VW, Cardenas DD, red. Spinal cord medicine: principles and practice. New York, NY: Demos Medical Publishing, 2002: 349 – 67.
- 42.
Hjeltnes N. Physical exercise and electrical stimulation in the management of metabolic, cardiovascular and skeletal-muscle alterations in people with tetraplegia. Doktorgradsavhandling. Stockholm: Karolinska sjukhuset, 1998: 12.
- 45.
Barton CH, Vaziri ND, Gordon S et al. Renal pathology in end-stage renal disease associated with paraplegia. Paraplegia 1984; 22: 31 – 41. [PubMed]