Fremmedlegemer som karproteser øker bakteriers sykdomsfremkallende evne blant annet ved å redusere størrelsen på det inokulatet som er nødvendig for å gi infeksjon. De gir også lavvirulente bakterier som Staphylococcus epidermidis evne til å fremkalle infeksjoner. Immunsystemets mulighet for å bekjempe og sanere infeksjoner i områder med fremmedlegemer er sterkt redusert eller umuliggjort. Fremmedlegemeinfeksjoner er ofte alvorlige, og infeksjoner i torakale aortaproteser er nærmest katastrofale, med en dødelighet på 25 – 75 % (1, 2). Vi beskriver sykehistorien til en pasient som kort tid etter innsetting av en torakal aortaprotese fikk en sårinfeksjon med sternumosteomyelitt og septikemi med gule stafylokokker, og sannsynligvis sekundært til denne utsæd av stafylokkene til aortaprotesen med residiverende septikemiepisoder.
Pasienten. En 71 år gammel mann ble innlagt i Medisinsk avdeling, Akershus universitetssykehus, med akutte brystsmerter i november 1998. Det ble påvist et dissekerende aortaaneurisme type A, og han ble umiddelbart overflyttet til regionsykehuset. Der ble han samme døgn vellykket operert med innsetting av en suprakoronar karprotese og fikk anlagt en anastomose mellom venstre mammaria interna og venstre coronaria descendens. Etter tilbakekomst til vårt sykehus ble han fjerde postoperative døgn høyfebril og dyspneisk, og det ble påvist gule stafylokokker i blodkultur. Han ble flyttet tilbake til regionsykehuset, der han ble behandlet for sepsis og tappet for 800 ml blodig pleuravæske. Retrosternal abscess kunne ikke påvises, og sternum var stabil, med kun sparsom serøs sekresjon fra nedre del av såret. I løpet av den neste uken ble det imidlertid sårruptur og sternumløsning, og to uker etter primæroperasjonen fikk han utført en dyp revisjon med fjerning av gamle suturer og anlegging av Robicseks sutur. Grunnet funn av hvite stafylokokker i sårsekret ble han behandlet med vankomycin, senere dikloksacillin i seks uker etter revisjonen. Forløpet ble komplisert av alvorlig, men reversibel nyresvikt, og man antok at det var en mulig sammenheng med vankomycin- og dikloksacillinbehandling. Tre måneder etter primæroperasjonen ble pasienten på nytt innlagt med spontan perforasjon av en abscess over sternum, hvorfra det vokste gule stafylokokker. Han ble denne gang behandlet med teikoplanin intramuskulært for mistenkt kronisk sternumosteomyelitt, men også under denne behandlingen fikk han nyresvikt, og behandlingen ble seponert etter en måned.
Fem måneder etter primæroperasjonen fikk han på ny septikemi med oppvekst av gule stafylokokker i blodkultur. Det ble gjort ny eksplorasjon under det gamle operasjonssnittet. De kraniale sternumsuturene ble fjernet, men det ble ikke funnet tegn til infeksjon i området. Det ble konkludert med at de residiverende infeksjonene hadde utgangspunkt i aortaprotesen. En leukocyttscintigrafi viste oppladning rundt proksimale proteseanastomose, og dette støttet opp under mistanken. Han ble satt på livslang suppresjonsbehandling med klindamycin 300 mg × 4, men etter tre måneder gikk man på ny tilbake til dikloksacillin 500 mg × 2 fordi han mente å ha mye ubehag av klindamycin.
14 måneder etter primæroperasjonen reduserte primærlegen dikloksacillindosen til 500 mg × 1 på grunn av stigende kreatininnivå. En uke etter dosereduksjonen fikk pasienten sin tredje septikemiepisode med gule stafylokokker i blodkultur. Han fikk dikloksacillin intravenøst i ti dager og ble ved utreise satt på dikloksacillin 500 mg × 3. Seks uker senere ble han innlagt med sin fjerde septikemi. Han fikk i to uker til intravenøst dikloksacillin, men kombinert med rifampicin, som han skulle fortsette å ta i to uker etter utskrivning. Han rakk ikke å fullføre denne behandlingen før han fikk septikemiepisode nummer fem med gule stafylokokker. Isolatet viste seg nå å være resistent mot rifampicin. Dobbelbehandling ble ansett å være nødvendig, og man la til trimetoprim-sulfametoksazol 1 tablett × 2.
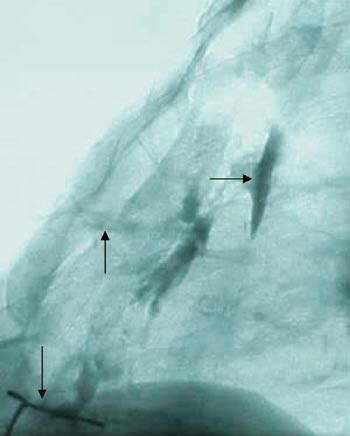
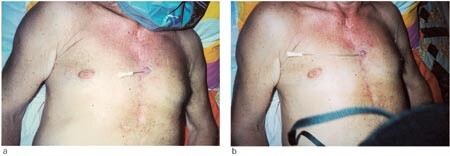
Denne behandlingen holdt ham symptomfri i sju måneder, da fikk han ny abscess over sternum. Abscessen ble incidert, og man fant en fistel. Fistulografi viste bred kommunikasjon inn mot karprotesen, men også ned mot gjenværende sternumsuturer (fig 1). De neste åtte månedene ble fistelen holdt åpen ved bruk av kvinnekateter med skyllinger (fig 2), men han fikk over en seksukersperiode tre nye septikemiepisoder, med gjentatt oppvekst av gule stafylokokker i blodkulturer. Han ble sykere for hver gang, og infeksjonen syntes å være helt ute av kontroll. Vi valgte derfor å forsterke suppresjonsbehandlingen ved å doble dosen trimetoprim-sulfametoksazol til 2 tabletter × 2, legge til fucidin 500 mg × 3, og fortsette med dikloksacillin i uendret dosering 500 mg × 3. Med denne behandlingen har pasienten vært symptomfri med normal CRP og senkning de siste 25 måneder.
Diskusjon
Insidensen av proteseinfeksjoner etter torakalaortakirurgi rapporteres å være 0,9 – 1,9 % (3, 4). De spesielle anatomiske forholdene i området gjør sanering med ekstraanatomisk bypass meget vanskelig, og in situ-proteseutskiftning fører uvegerlig til at den nye protesen kommer i kontakt med infisert materiale, med stor fare for reinfeksjon (5). Erfaringer med bruk av kryopreserverte homograft ved aortaklaffendokarditter har vist at disse er mer resistente mot reinfeksjoner enn kunststoffbaserte proteser (6, 7), og de siste ti år er kryopreserverte homograft også brukt med suksess ved in situ-utskiftninger av infiserte abdominale og torakale aortaproteser (8). Det er likevel ofte gode grunner til at man vegrer seg for å skifte ut en infisert torakal aortaprotese, f.eks. alvorlig komorbiditet hos pasienten og mindre sjanse for vellykket resultat ved mer virulente bakterier (9). Ikke minst skyldes tilbakeholdenheten at diagnosen proteseinfeksjon ofte bare er mistenkt eller sannsynliggjort, men ikke bevist, og operasjonsrisiko og perioperativ dødelighet ved utskiftningsinngrep er svært høy (10).
Diagnose
Diagnosen er vanskelig, og hos vår pasient ble den endelig først etter at fistulografi viste kontrast inn til protesen (fig 1). Gjentatte torakale computertomografiundersøkelser viste ingen forandringer fra funnene gjort umiddelbart postoperativt, og verken torakal magnetresonansundersøkelse eller transøsofageal ekkokardiografiundersøkelse var til nytte. Leukocyttscintigrafi viste imidlertid oppladning av radioaktivt merkede leukocytter rundt aortaroten og skjerpet mistanken om proteseinfeksjon. Denne undersøkelsen rapporteres å være positiv i kun 50 % av tilfellene (10). Infeksjon oppstår i de fleste tilfeller i forbindelse med selve innsettingen av protesen (11), men proteseinfeksjon fra tilstøtende infeksjonsfokus eller etter bakteriemi er like sannsynlig hos vår pasient. Pasienten fikk alvorlig septikemi med gule stafylokokker bare fire dager etter innsetting av protesen og således før denne var epitelialiseret. Sternumløsning 14 dager etter sternotomien tydet på hissig osteomyelittisk prosess.
Antibiotikaterapi
Etter den femte episoden med stafylokokkseptikemi ble isolater fra de septiske episodene genotypet. Forsterket fragmentlengdepolymorfisme (AFLP) viste identiske båndmønstre som uttrykk for at samme klon stadig blusset opp og gav klinisk sykdom. For å finne optimalt suppresjonsregime gjorde vi nye undersøkelser på minste inhibitoriske konsentrasjon (MIC) for flere antibiotika på isolater fra de ulike septiske episodene. Alle isolatene produserte penicillinase. De var også følsomme for penicillinasestabile penicilliner. Følsomheten for oxacillin var god hos første isolat fra november 1998 (MIC 0,5 mg/l), men MIC i februar 2000 var 1,0 mg/l, og i juni 2001 4,0 mg/l. Meticillinresistensgen kunne ikke påvises ved polymerasekjedereaksjon (PCR) (mecA-negativ).
Det ble tatt prøver til serumbaktericidi, der vi så etter baktericid virkning av pasientens serum på stafylokokkisolatene to timer etter inntak av henholdsvis 500 mg dikloksacillin peroralt og dikloksacillin i kombinasjon med 300 mg rifampicin, som er et meget potent antistafylokokkmiddel. Isolatet var følsomt for rifampicin, men resistensutvikling mot rifampicin ved ettrinns mutasjon forekommer relativt hyppig. For å unngå resistensutvikling under terapi ble det kombineret med dikloksacillin. Ved den sjette septiske episoden, to uker senere, var isolatet blitt resistent for rifampicin. Samtidig kom svar om at pasienten ikke hadde baktericide konsentrasjoner i serum inntil to timer etter inntak av 500 mg dikloksacillin. Sannsynligvis supprimerte vi pasienten med for lave doser av dikloksacillin og fikk derved en betydelig risiko for resistensutvikling mot rifampicin, eller pasienten hadde et meget stort bakterieinokulat.
Ved bruk av betalaktamantibiotika er det viktig at konsentrasjonen av antibiotikum er større enn mikrobens MIC-verdi i om lag halve doseringsintervallet. Man må derfor dosere tilstrekkelig ofte og i store nok doser. Vi økte suppresjonsdosen forbigående til 1 000 mg × 3.
Isolatene har hele tiden vært meget følsomme for trimetoprim-sulfametoksazol (MIC 0,064 mg/l) og fucidinsyre (MIC 0,125 mg/l). Trimetoprim-sulfametoksazol absorberes meget godt, og den lave MIC-verdien på 0,06 mg/l gir mulighet for effektive serumkonsentrasjoner det meste av døgnet ved dosering (160 mg trimetoprim + 800 mg sulfametoksazol) to ganger daglig. Fucidinsyre er et smalspektret antibiotikum med særlig god virkning mot gule stafylokokker. Det penetrerer godt inn i avaskularisert vev, og absorberes meget godt. Dosering av 1 g tre ganger i døgnet, gir etter to døgn serumkonsentrasjoner på 80 mg/l, som er langt over MIC-verdien for følsomme gule stafylokokker. Resistensutvikling under pågående behandling skjer imidlertid hyppig, og midlet må derfor kombineres med andre antistafylokokkmidler ved langtidsbehandling. Dikloksacillin absorberes ikke så godt, men med dosering 500 mg peroralt oppnås likevel serumkonsentrasjoner på 15 mg/l, og terapeutisk serumkonsentrasjon opprettholdes i omtrent fire timer. Det er viktig å dosere tilstrekkelig ofte, og vår pasient fikk residiv når midlet ble gitt kun én gang i døgnet. Vankomycin var sannsynligvis det minst rasjonelle antibiotikavalg brukt til vår pasient. Vankomycin er mindre potent og krever lengre behandling mot stafylokokker enn f.eks. betalaktamantibiotika. Det har nesten kun plass ved infeksjoner forårsaket av meticillinresistente S aureus og meticillinresistente S epidermidis, samt ved betalaktamresistente enterokokker. Teikoplanin ble først og fremst gitt fordi vi en tid fryktet at dikloksacillin ville gi ny nyresvikt, men argumentene anført mot vankomycin gjelder også mot teikoplanin.
Konklusjon
Antibiotikabehandlingen alene forklarer neppe hvorfor det har vært mulig å få langtidsoverlevelse ved en så vidt hissig septisk infeksjon i en torakal aortaprotese. Lokale forhold rundt protesen og pasientens immunrespons må antas å være vesentlig medvirkende faktorer for det gunstige forløpet. I en slik situasjon må de marginene som ligger i en gjennomtenkt og rasjonell antibiotikabehandling utnyttes best mulig.
Bestemmelser av MIC-verdier, tilstrekkelig høy og hyppig dosering og kombinasjon av antibiotika med god peroral absorpsjon og god aktivitet mot gule stafylokokker, samt tidlig og aggressiv behandling av de septiske gjennombruddene, har sannsynligvis bidratt til langtidsoverlevelse hos vår pasient. Samarbeid med mikrobiologisk ekspertise er viktig.
Vi takker til Kjell B. Hellum, Infeksjonsmedisinsk seksjon, Medisinsk avdeling, Akershus universitetssykehus, for kritisk gjennomlesing og forslag til forbedring av manuskriptet, og Tone Tannæs, Epi-Gen instituttet, Akershus universitetssykehus, for AFLP-analyser.
- 1.
Coselli JS, Crawford ES, Williams TW jr., Bradshaw MW, Wiemer DK, Harris RL et al. Treatment of postoperative infection of ascending aorta and transverse arch, including use of viable omentum and muscle flaps. Ann Thorac Surg 1990; 50: 868 – 81.
- 2.
Lawrence PF. Management of infected aortic grafts. Surg Clin North Am 1995; 75: 783 – 97.
- 3.
Svensson LG, Crawford ES, Hess KR, Coselli JS, Safi HJ. Experience with 1509 patients undergoing thoracoabdominal aortic operations. J Vasc Surg 1993; 17: 357 – 70.
- 4.
Hargrove WC, Edmunds LH. Management of infected thoracic aortic prosthetic grafts. Ann Thorac Surg 1984; 37: 72 – 7.
- 5.
O’Hara PJ, Hertzer NR, Beven EG, Krajewski LP. Surgical management of infected abdominal aortic grafts: review of a 25 year experience. J Vasc Surg 1986; 3: 725 – 31.
- 6.
Donaldson RM, Ross DM. Homograft aortic root replacement for complicated prosthetic valve endocarditis. Circulation 1984; 70: 170 – 81.
- 7.
Zwischenberger JB, Shalaby TZ, Conti VR. Viable cryopreserved aortic homograft for aortic valve endocarditis and annular abscesses. Ann Thorac Surg 1989; 48: 365 – 9.
- 8.
Vogt PR, von Segesser LK, Goffin Y, Niederhauser J, Genomi M, Kunzli A et al. Eradication of aortic infections with the use of cryopreserved arterial homografts. Ann Thorac Surg 1996; 62: 640 – 5.
- 9.
Henke PK, Bergamini TM, Rose SM, Richardson JD. Current opinions in prosthetic vascular graft infection. Am Surg 1998; 64: 39 – 45.
- 10.
Coselli JS, Köksoy C, LeMaire SA. Management of thoracic aortic graft infections. Ann Thorac Surg 1999; 67: 1990 – 3.
- 11.
Seeger JM. Management of patients with prosthetic vascular graft infection. Am Surg 2000; 66: 166 – 77.