Nye helseteknologier – fra utvikling til innføring
Background.
The increasing number of available health technologies requires assessments of their efficacy and patient safety, based on scientific principles.
Method.
Review and discussion of the scientific basis for the assessment of new health technologies.
Results.
Randomized controlled trials are the gold standard in health technology assessment and they are the evidence on which meta-analyses and systematic reviews are based. However, limitations, in point of principle as well as methodological, have to be recognised when randomized controlled trials are used in the context of interventional therapies. In such situations, observational studies can provide valuable results. Small area variation studies uncover regional variations and help define the need for new technologies.
Interpretation.
The introduction of new health technologies has to be based on scientific assessment and must be implemented in a structured way with continuous quality assessment. The medical profession has a strong commitment to introduce new health technologies with the greatest responsibility and self-discipline, thus facilitating improved medical care for patients.
Be not the first by whom
the new are tried,
Nor yet the last to lay the old aside.
Alexander Pope (1688 – 1744) An Essay on Criticism
Nye intervensjonsteknikker er i løpet av de siste 10 – 15 år blitt introdusert og i økende grad tatt i bruk i klinisk praksis. Det finnes flere eksempler på at nye teknologier er innført uten at disse metodene er blitt vitenskapelig evaluert på forhånd. Laparoskopisk kolecystektomi ble akseptert av det kirurgiske miljøet som ny standard på et tidspunkt da vitenskapelig evaluering så vidt var begynt (1). Motivasjonen for å ta i bruk ny teknologi er prinsipielt basert på å skape et bedre behandlingsresultat for pasienten. Det er et behov for innovasjon i de medisinske fag. Likevel kan også andre faktorer spille en rolle i en utviklingsprosess: Personlige ambisjoner hos leger, påvirkning fra utstyrsindustrien eller pasientgrupper og forventninger formidlet i medier.
Grunnlaget for medisinsk virksomhet er å gi pasientene et forsvarlig behandlingstilbud, og siktemålet er å oppnå en best mulig effekt. At innovasjon er en naturlig del av denne prosessen, er vel ubestridt. Samtidig må pasientens sikkerhet ivaretas, med tanke på et forutsigbart behandlingsresultat. Fagutviklingen skal foregå innenfor de lovmessige og vitenskapelige rammene som er satt med tanke på evaluering og dokumentasjon (2, 3). I denne artikkelen vil vi sette søkelys på hvilke vitenskapelig-metodologiske forutsetninger som må være til stede når ny teknologi skal introduseres på en kontrollert måte i klinisk praksis, samtidig som pasientsikkerheten blir ivaretatt.
Definisjoner
Begrepet helseteknologier innebærer alle tiltak som kan anvendes for å diagnostisere, behandle eller forhindre sykdom, samt tiltak innen rehabilitering og langtidspleie (4).
Med intervensjon menes å skape fysiske forandringer som tar sikte på å korrigere en sykelig forandring av anatomien og/eller fysiologien hos en pasient (4).
Behandlingseffekt er definert som den samlede oppnådde helsegevinst når det er tatt hensyn til både ønskede og uønskede virkninger hos pasienten. Behandlingseffekten måles i endepunkter: Definerte målbare kriterier for forandringer i pasientens helsetilstand som følge av den gjennomførte behandlingen. Endepunktene kan være kvantitative (f.eks. fysiologiske variabler) eller kvalitative (f.eks. livskvalitet).
Tradisjon og dagens praksis
Gjennom et tilbakeblikk på medisinske tradisjon ser vi at forandringer i medisinske metoder ofte har vært ensbetydende med et paradigmeskifte: Innføring av moderne hygieneprinsipper, anestesi og kirurgi førte til dramatiske forbedringer av morbiditet og mortalitet for en rekke tilstander. Sammenliknet med slike historiske gjennombrudd er endringer basert på ny helseteknologi i dag heller marginale (5).
Innføring av en ny teknologi i klinisk praksis berører to viktige områder:
-
Evaluering av ny teknologi etter vitenskapelige kriterier.
-
Kontrollert opplæring av fagmiljøet.
Introduksjonen av appendektomi for litt over 100 år siden er et godt eksempel på hvordan nye helseteknologier kom til. Den kirurgiske teknikken ble etablert ved at enkelte kirurger begynte å utføre operasjonen (6). Etter hvert ble studier som som oftest gjenspeilte erfaringer hos enkelte kirurger publisert (7). Denne form for evaluering av nye metoder har så langt vært standard i kirurgisk litteratur (8). Opplæringen av fagmiljøet i den nye teknologien har tradisjonelt vært basert på individuell videreformidling fra en erfaren kollega eller på at kirurgen tilegnet seg nødvendig kunnskap på egen hånd. Dette gjenspeiler seg i ordtaket «see one, do one, teach one». Det kan stilles spørsmål ved om en slik erfaringsoverføring er tilstrekkelig for våre fagmiljøer i møtet med et stadig økende tilbud av nye helseteknologier. Konsekvensen er at nye teknologier kan spres uten nødvendig opplæring, uten at man etterspør relevant dokumentasjon og uten adekvat evaluering. I en slik situasjon blir innføring av ny teknologi basert på antakelser og hypoteser i stedet for på kvalifisert kunnskap. Nye teknologier skal være mer kostnadseffektive, resultatene skal være minst like gode og de skal kunne utføres av alle (9). Til hver ny teknologi er det knyttet en læringskurve, både med henblikk på å etablere selve prosedyren og i forhold til den enkelte utførende lege (10). Det er ikke til å unngå at enkelte pasienter vil kunne oppleve negative effekter i forløpet av denne læringskurven (11).
Vitenskapelig basis for ny teknologi
Alle medisinske avgjørelser som har konsekvenser for den enkelte pasientens behandling bør være basert på best mulig kunnskap – kunnskapsbasert medisin. Mens noen behandlingsmetoder har et dramatisk og opplagt behandlingsresultat slik at en studie ansees som unødvendig, f.eks. livreddende prosedyrer som drenasje av trykkpneumothorax, er resultatene mindre sikre i andre tilfeller (f.eks. laparoskopisk versus åpen brokkirurgi). Behandlingseffekten må evalueres med tanke på både korttids- og langtidsresultater.
Det foreligger aksepterte vitenskapelige metoder for hvordan nye behandlingsmetoder skal etableres og evalueres. Det må dokumenteres en reell behandlingseffekt. Effekten måles i forhold til forhåndsdefinerte kriterier – endepunkter. Slike endepunkter skal måle det som er vesentlig for pasienten (f.eks. morbiditet, mortalitet, overlevelse, residivrate), i motsetning til mindre relevante, såkalte surrogate endepunkter, f.eks. en statistisk signifikant, men i klinisk sammenheng marginal forskjell i operasjonstid (12). Slike surrogate endepunkter uten relevans for pasientene kan ikke danne grunnlag for å bedømme effekten av tiltak. Helsegevinsten bør ikke bare måles i forhold til objektiviserbare kvantitative variabler (f.eks. overlevelse), men også med henblikk til subjektive kriterier (f.eks. livskvalitet). Det er utviklet flere validerte evalueringsverktøy til bruk i ulike sammenhenger (13).
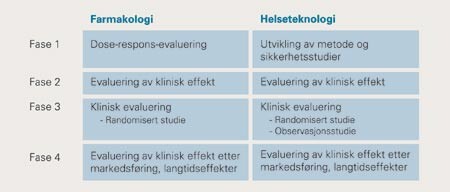
Utvikling av nye behandlingstilbud vil måtte skje gjennom ulike faser (fig 1). Denne modellen er mest kjent fra farmakologien, men det finnes analogier til helseteknologier (3). Det er imidlertid opplagte forskjeller mellom medikamentell og intervensjonsbasert behandling slik at gjennomføringen av studier kan være problematisk. Forskjellen ligger først og fremst i det at effekten av intervensjonsmetoder som regel er irreversibel, i motsetning til en reversibel effekt når et medikament seponeres. Fase 1-studier går ut på teste sikkerhetsaspekter. Et nytt medikament ville bli testet hos frivillige forsøkspersoner. Dette er ikke mulig for intervensjonsteknikker, og derfor trenger man utvalgte pasienter. I fase 2-studier vurderer man om den nye behandlingen gir den ønskede kliniske effekt. For mange intervensjoner vil effekten være såpass åpenbar at en fase 2-studie ikke vil være gjennomførbar. Dermed kan terskelen være lav fra teknisk utvikling av metoden til bred klinisk anvendelse før adekvat evaluering gjennom fase 2-og fase 3-studier er gjennomført.
Randomiserte studier – gullstandard med begrensninger
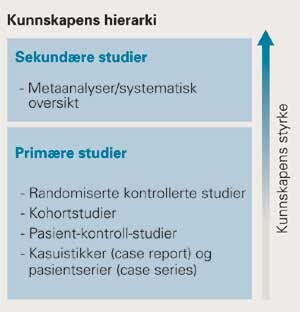
Blant de tilgjengelige vitenskapelige metodene er randomiserte kontrollerte studier (engelsk «randomised controlled trial») akseptert som den beste metoden for å sammenlikne to eller flere behandlingsalternativer (fig 2) (5). Dette er en eksperimentell studiedesign der man ved tilfeldig tilordning av pasientene til de ulike behandlingsgruppene forsøker å utelukke flest mulig systematiske feil (engelsk «bias») som påvirker resultatene. Ideelt sett skal det kun være det aktuelle behandlingsalternativet som forklarer forskjellig effekt. Ut fra prinsipielle betraktninger er det altså ønskelig at randomiserte studier gjennomføres før ny helseteknologi tas i bruk. En viktig forutsetning for en randomisert studie er at det foreligger to likeverdige alternativer som skal testes(engelsk «equipoise»). Dessuten forutsettes det at behandlingseffekten av den etablerte metoden er godt nok evaluert og dokumentert. Det finnes imidlertid mange etablerte metoder og prosedyrer hvor dette ikke eller kun delvis er tilfellet. Andre viktige forutsetninger er blant annet at den aktuelle sykdommen opptrer med en insidens som er høy nok til å inkludere et tilstrekkelig antall pasienter innenfor et rimelig tidsrom. For lang tid mellom start av behandlingen til effekten viser seg vil føre til at for mange pasienter ville falle ut av studien under oppfølgingen.
Randomiserte studier er vanskeligere å gjennomføre innen intervensjonsbasert medisin enn innen farmakologien (fig 3) (14). Dette skyldes en rekke prinsipielle og metoderelaterte forhold. Det publiseres få randomiserte studier innenfor de kirurgiske fag. Solomon og medarbeidere (15) fant at kirurgiske randomiserte studier var av relativ lav kvalitet, og bare 30 % ble utført av kirurger. Kun en tredel ble publisert i kirurgiske tidsskrifter, og kun en firedel omfattet studier der to kirurgiske behandlingsmetoder ble sammenliknet. Det viste seg at bare 35 % av studiene hadde fått uavhengig økonomisk støtte. Uavhengig finansiering av slike studier må ansees som et viktig kvalitetskriterium, da økonomisk tilskudd fra utstyrsfabrikanter kan ha innvirkning på studiens premisser. En studie kan ikke være et påskudd for å etablere en ny helseteknologi. Det kan skje først når dette er begrunnet ut fra resultatene. I motsetning til randomiserte studier innen farmakologien vil en studie av helseteknologi kreve opplæring for å bruke utstyret. Volumaspektet har her omvendt betydning i forhold til medikamentbruk. Mens økt bruk av et medikament vil gi økt forekomst av bivirkninger, vil hyppigere bruk av en teknologi føre til at den beherskes bedre. Til enhver prosedyre er det knyttet en læringskurve. Adekvat opplæring av deltakende leger er derfor et viktig krav.

At randomiserte studier er problematisk ved sammenlikning av intervensjonsmetoder, fremkommer i en undersøkelse av hvor mange slike kliniske problemstillinger som kan besvares ved hjelp av randomiserte studier (8). Kun i 40 % av tilfellene ville en randomisert studie ha gitt svar under ideelle kliniske og forskningsmessige betingelser. Randomiserte studier ble imidlertid kun publisert i 12 % av tilfellene hvor dette ville ha vært mulig.
Randomiserte studier innen helseteknologi kan være beheftet med skjevheter. Dette gjelder spesielt seleksjon av pasienter, variasjon blant utøvende leger og manglende blinding (12). Resultater fra studier gjennomført ved spesialiserte sentre og av entusiastiske leger vil ikke uten videre kunne overføres direkte til vanlig klinisk praksis. Det er likevel mulig å gjennomføre randomiserte studier der slike systemfeil er sterkt redusert. Majeed og medarbeidere (16) og Nilsson og medarbeidere (17) viste at blinding lot seg gjennomføre ved sammenlikning av laparoskopiske og åpne bukinngrep, og de påståtte fordelene ved laparoskopisk kirurgi var langt mindre enn forventet. Vurdering og analyse av studiedata ved hjelp av en uavhengig ekspertgruppe er en annen viktig forutsetning for å begrense innvirkningen av systemfeil på resultatene (18).
Metaanalyser og systematiske oversikter er anerkjente metoder for å få en samlet vurdering av foreliggende kunnskap. For å få frem meningsfulle konklusjoner stiller dette høye krav til primærstudiene som skal inngå i analysene. Metaanalyser av randomiserte studier gjort i forbindelse med laparoskopisk versus åpen appendektomi viste at de fleste studiene var uegnet til en metaanalyse på grunn av metodologiske svakheter (manglende styrkeberegning, uklare eller manglende definisjoner av endepunkter) (10, 12, 19).
Observasjonsstudier – et adekvat alternativ?
Noen hevder at bare randomiserte studier kan brukes for å vurdere helseteknologier (20). Det finnes imidlertid åpenbare begrensninger som gjør at slike studier ikke uten videre kan gjennomføres. Da kan ikke-randomiserte studier, også kalt observasjonsstudier, være et alternativ (14): Ikke-randomiserte kohortstudier der en definert pasientgruppe følges i henhold til endepunkter, enten prospektive eller retrospektive. Observasjonsstudier vil være et godt alternativ når en eksperimentell studie er vanskelig å gjennomføre: Ved en helt åpenbar behandlingseffekt er randomisering unødvendig. En randomisert studie vil ikke være hensiktsmessig for å evaluere hendelser som opptrer med lav frekvens (f.eks. sjeldne bieffekter). Dette oppnår man heller ved hjelp av store kohortstudier. Slike studier gjennomføres som regel først etter markedsføring (postmarketingstudie, fase 4-studie) av et nytt behandlingstilbud. En korrekt gjennomført studie vil dermed gi et bilde av behandlingsresultater ved bred klinisk anvendelse. Dette er spesielt viktig for intervensjonsteknologier. Forutsetningen er at man bygger opp store databaser som f.eks. hofteregisteret.
I de fem norske helseforetakene burde forholdene ligge spesielt godt til rette for opprettelsen av regionale og nasjonale databaser. Resultater fra slike databaser vil trolig ha stor interesse internasjonalt. Randomisering av ulike behandlingstilbud vil også kunne støte på etiske problemer, hvis det er åpenbart at et av alternativene innebærer en uakseptabel ulempe for pasientene. Det vil ikke lenger være forsvarlig å randomisere mellom konvensjonell rectumkirurgi og total mesorektal eksisjon ved rectumcancer i lyset av den allerede dokumenterte forbedring i resultater etter behandling med total mesorektal eksisjon. Det norske rectumcancerprosjektet er et eksempel på at en nasjonal kohortstudie er et godt alternativ (21).
Observasjonsstudier er i utgangspunktet like mye utsatt for skjevheter som randomiserte studier. Det foreligger metoder utarbeidet av Cochrane Collaboration for hvordan man kan sammenlikne observasjonsstudier (22). En god beskrivelse og definisjon av den gjeldende studiepopulasjonen er avgjørende for betydningen av resultatene. Som regel vil populasjonsbaserte studier redusere skjevheter basert på seleksjon (engelsk «selection bias»). Systematisk forskjell i utføring av behandlingen (engelsk «performance bias»), antall pasienter som er fulgt opp (engelsk «attrition bias» eller «exclusion bias»), samt systematisk forskjell i vurdering av resultatene (engelsk «detection bias»), er andre muligheter for uheldig påvirkning av resultater. Observasjonsstudier kan gi meget verdifull kunnskap, bare man er seg bevisst metodens begrensninger. Randomiserte studier og observasjonsstudier må ikke sees som konkurrerende alternativer, men heller som komplementære metoder med ulike styrker og svakheter.
Geografiske aspekter ved observasjonsstudier
Et annet aspekt ved observasjonsstudier er at de kan bidra til å oppdage geografiske forskjeller i bruk av helsetjenesten (engelsk «small area variation studies»), både i form og omfang (23). Slike studier vil kunne avsløre om pasienter i noen regioner blir over- eller underbehandlet, eller om det foreligger forskjeller i helsetjenestenes kvalitet eller tilgjengelighet. Forutsetning for slike studier er at områdene er sammenliknbare med henblikk på insidens, sykdomsprevalens og demografiske variabler. Sentralt står forekomsten av helserelaterte hendelser per innbygger i området (engelsk «per capita events»). Slike opplysninger kan være av betydning for å vurdere om pasientgrunnlaget rettferdiggjør å ta i bruk nye helseteknologier. Den nye organisasjonen av vårt helsevesen med opprettelse av fem helseforetak, og kravet om utjevning av regionale forskjeller, vil gjøre det enda mer aktuelt å foreta slike studier med tanke på bruk og innføring av nye helseteknologier på regionalt og nasjonalt plan (2). Opprettelse av egnete databaser som en basal forutsetning må derfor ansees som en naturlig oppgave for helseforetakene.
Innføring av ny helseteknologi i fagmiljøet
Ved siden av adekvat vitenskapelig evaluering er pasientsikkerhet det andre viktige momentet (2). Høy vitenskapelig standard må kombineres med en strukturert fremgangsmåte som hindrer ukritisk bruk av ny helseteknologi. Innovative tiltak og utviklingsprosesser i de operative fag må ikke fortone seg som cowboykirurgi. Innføring av ny helseteknologi bør baseres på flere forutsetninger. Sentralt står forsvarligheten, ikke bare i forhold til helselovene, men også i forhold til etikken. Bruk av ny helseteknologi stiller spesielle krav til pasientinformasjon og dokumentasjon.
Så langt foreligger det ingen entydige retningslinjer om hvem som kan ta i bruk nye metoder og under hvilke forutsetninger det kan skje. Her er det viktig at fagmiljøene pålegger seg den nødvendige selvdisiplinen og selvkritikk. At dette er praktisk mulig, viser en undersøkelse av innføring av laparoskopisk kolecystektomi ved et amerikansk sykehus (24). Cuschieri (25) foreslo nylig en modell for kontrollert evaluering av nye teknikker. Den går ut på å prøve ut en ny teknikk i selekterte sentre under ekstern overvåking av en gruppe fagfolk – tilsvarende en fase 2-studie. Data om sikkerhet og effektivitet samles i et adekvat register (engelsk Health Technology Assessment – HTA-register). Slike data resulterer i en observasjonsstudie og gir første grunnlag for en metodevurdering. Deretter vil randomiserte studier kunne gjennomføres under videre uavhengig kontroll, etterfulgt av systematisk og kontrollert opplæring av fagmiljøet. Dette vil kunne legge til rette for en kontrollert vurdering og innføring av effektive nye metoder, med minimal risiko for pasienten.
-
Helseteknologi: Alle tiltak som anvendes til diagnostikk, behandling og forebygging av sykdom samt rehabilitering og langtidspleie
-
Vitenskapelig evaluering av helseteknologier Randomiserte kontrollerte studier Observasjonsstudier
-
Behandlingseffekt: Den samlede helsegevinsten for pasienten når det er tatt hensyn til positive/ønskede effekter og negative/uønskede effekter
-
Endepunkt: Definert kriterium for å måle behandlingseffekten – Kvalitativt eller kvantitativt – Reelt endepunkt: Betydning for pasienten – Surrogatendepunkt: Uten betyd ning for pasienten
- 1.
Robert G, Stevens A, Gabbay J.«Early warning systems» for identifying new healthcare technologies. Health Technol Assess 1999; 3: 1 – 108.
- 2.
Steine V. Sykehusreformen – noen eierperspektiv. Rapport No.: I-1044 B. Oslo: Sosial- og helsedepartementet; 2001.
- 3.
Gillett G. Ethics of surgical innovation. Br J Surg 2001; 88: 897 – 8.
- 4.
National Health Service Research and Development Health Technology Assessment. www.ncchta.org/ (31.1.2002)
- 5.
McLeod R. Evidence-based surgery. I: Norton E, red. Surgery. Basic science and clinical evidence. New York: Springer-Verlag, 2001: 55 – 66.
- 6.
Seal A. Appendicitis: a historical review. Can J Surg 1981; 24: 427 – 33.
- 7.
Richardson M. Remarks upon appendicitis, based on a personal experience of one hundred and eighty-one cases. Am Med Sci 1894; 107: 1 – 23.
- 8.
Solomon MJ, McLeod RS. Should we be performing more randomized controlled trials evaluating surgical operations? Surgery 1995; 118: 459 – 67.
- 9.
Hopkins MP. The myths of laparoscopic surgery. Am J Obstet Gynecol 2000; 183: 1 – 5.
- 10.
Law S, Wong J. Use of controlled randomized trials to evaluate new technologies and new operative procedures in surgery. J Gastrointest Surg 1998; 2: 494 – 5.
- 11.
Berci G. How new technology affects practice and patient safety. J Am Assoc Gynecol Laparosc 1997; 4: 419 – 21.
- 12.
Fingerhut A, Millat B, Borrie F. Laparoscopic versus open appendectomy: time to decide. World J Surg 1999; 23: 835 – 45.
- 13.
Kaasa S. Using quality of life assessment methods in patients with advanced cancer: a clinical perspective. Eur J Cancer 1995; 6: 15 – 7.
- 14.
Black N. Why we need observational studies to evaluate the effectiveness of health care. BMJ 1996; 312: 1215 – 8.
- 15.
Solomon MJ, Laxamana A, Devore L, McLeod RS. Randomized controlled trials in surgery. Surgery 1994; 115: 707 – 12.
- 16.
Majeed AW, Troy G, Nicholl JP, Smythe A, Reed MW, Stoddard CJ et al. Randomised, prospective, single-blind comparison of laparoscopic versus small-incision cholecystectomy. Lancet 1996; 347: 989 – 94.
- 17.
Nilsson G, Larsson S, Johnsson F. Randomized clinical trial of laparoscopic versus open fundoplication: blind evaluation of recovery and discharge period. Br J Surg 2000; 87: 873 – 8.
- 18.
Patients at high risk of death after lung-volume-reduction surgery. N Engl J Med 2001; 345: 1075 – 83.
- 19.
McCall JL, Sharples K, Jadallah F. Systematic review of randomized controlled trials comparing laparoscopic with open appendicectomy. Br J Surg 1997; 84: 1045 – 50.
- 20.
Doll R. Summation of conference. Doing more good than harm: the evaluation of health care interventions. Ann N Y Acad Sci 1994; 703: 313.
- 21.
Wiig JN, Carlsen E, Soreide O. Mesorectal excision for rectal cancer: a view from Europe. Semin Surg Oncol 1998; 15: 78 – 86.
- 22.
Cochrane Reviewers" Handbook 4.1.5. Updated april 2002. The Cochrane Library. Oxford: The Cochrane Collaboration; 2002. cochrane.org/cochrane/hbook.htm (18.8.2002).
- 23.
Kreder HJ, Wright JG, McLeod R. Outcome studies in surgical research. Surgery 1997; 121: 223 – 5.
- 24.
Sequeira R, Weinbaum F, Satterfield J, Chassin J, Mock L. Credentialing physicians for new technology: the physician"s learning curve must not harm the patient. Am Surg 1994; 60: 821 – 3.
- 25.
Cuschieri A. New technologies in laparoscopic surgery. Chirurg 2001; 72: 252 – 60.