Svulster som involverer basis av hodeskallen forekommer relativt sjelden. Ikke desto mindre utgjør de en stor utfordring, idet den kirurgiske tilgangen til slike svulster er svært vanskelig og ofte ledsaget av betydelig morbiditet.
Svulster i gulvet av fremre skallegrop kan som oftest opereres via standard nevrokirurgiske tilganger, så som frontale eller bifrontale kraniotomier (1, 2). Slike kraniotomier gir god visualisering av svulster i fremre deler av fremre skallegrop (1, 2), men kan også benyttes som en øvre tilgang til svulster i øvre bihuleområder (3). Imidlertid oppnår man begrenset oversikt over de bakre områdene av fremre skallegrop, noe som er viktig ved for eksempel meningeomer ved tuberculum sellae eller større hypofysesvulster som ikke egner seg for transsfenoidal reseksjon. Legges kraniotomien i tillegg lenger lateralt og kaudalt, såkalt frontotemporalt eller pterionalt, oppnår man i tillegg til bedre oversikt over planum og tuberculum sellae-regionen, også en bedre oversikt over anteriore deler av midtre skallegrop (1, 2, 4, 5). Imidlertid kan det være svært vanskelig å angripe svulster som ligger medialt og basalt i midtre skallegrop forfra (frontal/bifrontal kraniotomi) eller fra siden (frontotemporal-anterior subtemporal kraniotomi) på grunn av luktenerven, synsnervene og synsnervekrysningen, hypofysestilken, samt de store karstammene (5).
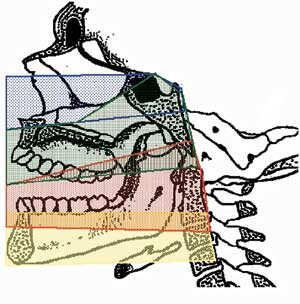
De siste tiårs etablering av multidisiplinære kraniofacialteam og transfaciale teknikker har gitt kirurgisk tilgang til mediale deler av hjernens basis og stamme fra sella turcica og ned til 4. halsvirvel (fig 1). Mens en transnasal, transsfenoidal tilgang vil være velegnet for lesjoner nær sella turcica (6), vil man ofte velge en transmaksillær, transfaryngeal tilgang for lesjoner i clivusområdet (7, 8) transoralt for lesjoner nær kraniocervikalovergangen (9) og endog transmandibulært for lesjoner kaudalt for dette (7).
Vi presenterer to pasienter som ble operert ved denne type teknikker.
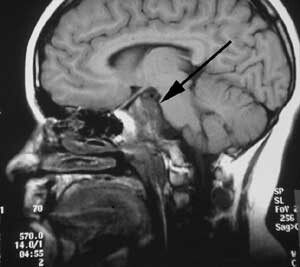
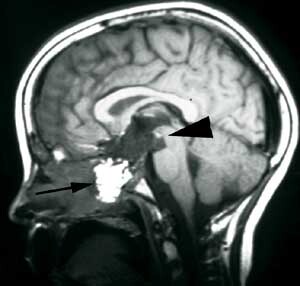
Pasient 1. Ni år gammel pike, født til termin, upåfallende psykomotorisk utvikling. Fra sju års alder klaget hun periodevis over svie/kløe i begge øynene og dobbeltsyn. Hun ble da bredt utredet uten resultat. Symptomene gikk delvis tilbake, men påfølgende år tilkom økende symptomer og man påviste da en bilateral abducensparese. Ny bildediagnostikk avslørte nå en stor ekspansiv prosess utgående fra clivus med affeksjon av pons, mest forenlig med et clivuskordom (fig 2a).
Pasienten ble henvist til Nevrokirurgisk avdeling, Rikshospitalet. Ved innleggelsen klaget hun over hodepine og økt trettbarhet. Ved klinisk undersøkelse ble det verifisert en bilateral abducensparese, mens annen nevrologisk status var uten anmerkning.
Pasienten ble operert med transfacial tilgang og ekstradural tumorreseksjon.
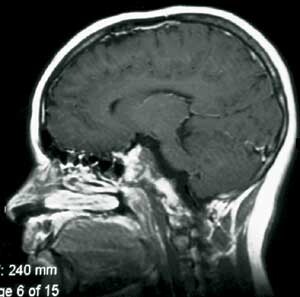
Det postoperative forløpet var meget tilfredsstillende. Hun kunne mobiliseres første dag etter inngrepet uten nye nevrologiske utfall. En postoperativ MR avslørte en liten resttumor (fig 2b). Hun ble derfor henvist og behandlet ved Stråleknivenheten, Nevrokirurgisk avdeling, Haukeland Universitetssykehus. Påfølgende år har hennes dobbeltsyn vært i jevn bedring. MR-kontroller har vist at resttumor er i regresjon.
Drøyt ett år etter kirurgi og stereotaktisk bestråling er hun normalt fungerende uten andre plager enn en lett bilateral abducensparese.
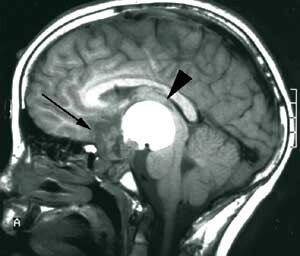
Pasient 2. Ni år gammel gutt med normal psykomotorisk utvikling frem til åtte års alder. Han utviklet da vekstretardasjon og det ble senere påvist en generell hormonsvikt og økende synstap. Radiologisk utredning viste en stor cystisk tumor i hypofyseregionen med affeksjon av synsbaner og hypothalamus. Tumor ble oppfattet som et kraniofaryngeom.
Det ble utført en stereotaktisk punksjon av cysten med instillasjon av radioaktivt yttrium. Man oppnådde imidlertid ikke tumorkontroll. Fire måneder senere utførte man derfor en kraniotomi og reseksjon av tumor. Under inngrepet viste det seg umulig å redde restsyn og hypofysefunksjon. Videre utviklet pasienten hydrocephalus postoperativt og fikk anlagt en ventrikuloperitoneal shunt.
I løpet av få måneder fikk gutten på nytt økende symptomer i form av hodepine, irritabilitet og personlighetsendringer. MR viste gjenvekst av tumor.
Pasienten ble henvist til Nevrokirurgisk avdeling, Rikshospitalet for vurdering med tanke på ytterligere kirurgi. Det forelå nå imidlertid en betydelig tumordestruksjon og invasjon i clivus av solide tumorkomponenter og ny cyste posterokaudalt mot 3. ventrikkel/hypothalamus og pons (fig 3a). Klinisk var pasienten også i meget rask forverring og hadde preoperativt redusert bevissthet, sløvet tale, ustø gange og urininkontinens.
Pasienten ble derfor operert med en transfacial tilgang med intradural reseksjon av tumor.
Postoperativt tilkom en høyresidig hemiparalyse. På MR-bilder visualiseres en liten blødning i venstre brachium pontis. Pasienten fikk også en bakteriell meningitt som ble vellykket behandlet med systemisk antibiotika og uten at den ventrikuloperitoneale shunten måtte fjernes.
Pasienten er ved tremånederskontroll betydelig restituert og har kun en mindre ekstremitetsparese. Som før den siste operasjonen er han blind og fullstendig hormonsubstituert. Postoperativ MR-undersøkelse viser ikke tegn til resttumor (fig 3b).
Operativ teknikk
Pasientene gjennomgår omfattende preoperative undersøkelser ved de involverte kliniske avdelingene. Videre kan det være viktig å be om vurdering ved andre, særlig øre-nese-hals- og øyeavdelingene (tab 1).
Tabell 1
Preoperativ utredning
| Klinisk |
Pediater/NevrologNevrokirurgØyelegeØre-nese-halskirurgKjevekirurgAnestesilege |
| Endokrinologisk |
Preoperativ hormonstatus |
| Radiologisk |
Røntgen caput front + sideCerebral CT kontrast med tette koronale snitt gjennom mellomansiktetCerebral MR kontrast3D-CTAngiografi (DSA), CT-angiografi (CTA) eller MR-angiografi (MRA) |
| Odontologisk |
Ortopantogram (OPG)Intraorale fotografiBittmodell (dental cast) inkludert bittskinne |
| Annet |
Fotografering |
Peroperativt legges pasienten på ryggen og intuberes. Ofte anlegges en trakeostomi for å bedre plassforholdene i oropharynx. Pasienten overvåkes peroperativt på standard måte. Det gis pre-, per- og postoperativ infeksjonsprofylakse, samt høydose steroid. Et nevronavigasjonssystem (f.eks. BrainLab) benyttes peroperativt for å minimalisere unødig kirurgisk reseksjon og øke sikkerheten ved inngrepet.
Operasjonen innledes ved en midtlinjeincisjon gjennom alle bløtvevslagene i den harde og bløte gane. Deretter gjøres en standard LeFort I-maksillotomi, med vestibulær incisjon fra premolar til premolar på hver side (fig 4), horisontal osteotomi og nedfrakturering av maxilla. Maxilla spaltes deretter i to og roteres så forsiktig nedad og utad, hvoretter man har full eksponering av skallebasis, fra sella turcica og ned til atlasbuens forside (fig 5).

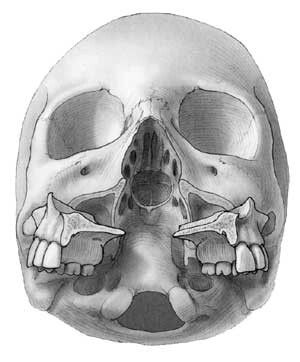
Under mikroskop åpnes deretter svelgveggen ved en midtlinjeincisjon gjennom alle lagene. Den beinete bakveggen fridissekeres subperiostalt, og ved bruk av høyhastighetsdrill fjernes deler av skallebasis i ønsket omfang inntil man kommer inn mot dura (fig 1).
Dura åpnes for intraduralt beliggende lesjoner eller forblir intakt ved ekstradurale lesjoner. Tumorreseksjon skjer deretter på vanlig måte under mikroskop.
Etter en intradural tumorreseksjon er tett lukking av dura svært viktig for å forhindre postoperativ liquorlekkasje. Ofte benyttes et fascietransplantat fra pasientens lår som sutureres på enkelte punkter til dura, hvorpå man appliserer vevslim for å oppnå god lukking.
Bakveggen i epi- og oropharynx lukkes lagvis. Deretter roteres de to maxillarhalvpartene mot hverandre og ganen lukkes.
Maxilla fikseres i sin originale posisjon ved hjelp av minititanplater, deretter lukkes incisjonen i gingiva. Til sist anlegges bittskinne og intermaksillær fiksasjon mellom over- og underkjeven.
Postoperativt blir pasienten fortsatt respiratorbehandlet med lett sedasjon og vekkes etter noen dager, dels fordi ødem kan kompromittere øvre luftveier, og dels for å forebygge raske stigninger i intrakranialt trykk ved hosting.
Avlastning av liquor er viktig i den postoperative fasen for å redusere det intradurale væsketrykket. Et lumbaldren holdes åpent den første uken. Så stenges det og pasienten observeres nøye med tanke på lekkasje av cerebrospinalvæske og ledsagende bakteriell meningitt. Profylaktisk antibiotikum benyttes de første 7 – 10 dagene postoperativt.
Pasienten tillates å spise lett kost (purré) den første måneden. Bittskinne fjernes 6 – 8 uker postoperativt.
Komplikasjoner
For å redusere postoperativ morbiditet, er det svært viktig at pasienten har en individuell behandlingsplan. De kirurgiske komplikasjonene er enten relatert til tilgangen per se eller til den nevrokirurgiske operasjonen. Her diskuteres kun tilgangsrelaterte komplikasjoner, idet prosedyrerelaterte komplikasjoner vil være avhengig en rekke faktorer, så som lesjonens art og beliggenhet.
Det hviler et særlig ansvar på kjevekirurg for å oppnå god okklusjon postoperativt. Følgelig må man samarbeide tett med kjeveortoped når man planlegger osteotomilinjene gjennom overkjeven (for ikke å skade tannrøtter eller -anlegg) og lager bittskinnen pasienten benytter postoperativt.
Den mest fryktede komplikasjonen ved LeFort I-osteotomier er avaskulær nekrose av maxilla. Slik nekrose forekommer sjelden ved rene ortognatiske inngrep, men spaltingen av overkjeven i midtlinjen og betydelig mobilisering av delene gir trolig en økt risiko ved transfacial kirurgi. Videre vil enkelte pasienter ha andre risikofaktorer som tidligere stråleterapi eller tumorinnvekst nær karforsyningen ved skallebasis.
Ettersom man ofte benytter transpalatinale tilganger, er det fordelaktig med plastikkirurgisk kompetanse i operasjonsteamet. God lukking av ganen er svært viktig for å redusere komplikasjoner som velofaryngeal insuffisiens og hypernasal tale (7).
Skade på hypofysen kan oppstå, enten som en direkte skade eller indirekte via skade på blodkar. Imidlertid vil pasientene ofte ha nedsatt eller opphørt hypofysefunksjon preoperativt som følge av sin grunnsykdom. Videre gir tilgangen et større operasjonsfelt og bedre visualisering enn ved transsfenoidale hypofyseoperasjoner, og ved sistnevnte operasjoner finner man operasjonsrelatert hypofysesvikt hos omkring 5 – 19 % (10).
Ved transsfenoidal hypofysekirurgi forekommer alvorlig vaskulær skade hos omkring 0,1 – 1 % av inngrepene (11). Forekomsten ved transfaciale inngrep er ikke kjent, men utvikling av pseudoaneurisme på a. carotis interna er rapportert i flere serier (7, 8).
Transfaciale inngrep er åpenbart forbundet med risiko for infeksjoner (7, 8, 12) idet munnhule, oropharynx og epipharynx er kolonisert av bakterier. Videre åpner man ofte sphenoidalsinus. Liquorlekkasje er kanskje viktigste risikofaktor for infeksjon.
God anestesiservice er svært viktig, særlig ved operasjoner på barn hvor blodvolumet er vesentlig mindre enn hos voksne.
Diskusjon
De siste tiårs utvikling av multidisiplinære kraniofacialteam har gjort det mulig å angripe lesjoner beliggende i de sentrale, mediale sonene av skallens basis i fremre og midtre skallegrop nedenfra via transfaciale tilganger (fig 1). Vi har presentert to pasienter med svulster i clivus som ble operert ved hjelp av slike teknikker.
Kraniofaciale teknikker tillater også kirurgisk tilgang til mer kaudalt beliggende lesjoner, både tumorer og aneurismer (13). I tillegg til rene transorale tilganger til kraniocervikalovergangen og øvre cervikalcolumna (9, 14), kan man også operere via translabiale og transmandibulære tilganger (7). Sistnevnte inngrep er imidlertid meget omfattende og forbundet med betydelig operativ morbiditet.
Det ligger et betydelig forbedringspotensial i bruk av moderne nevronavigasjonsteknikk. Ved å fusjonere CT-bilder (som visualiserer beinete strukturer) med MR-bilder (som visualiserer svulsten) og MR-angiogrammer (som visualiserer blodkarene), kan man trolig redusere komplikasjonene ved kraniofacial skallebasiskirurgi betydelig (15).
Transfacial kirurgi er kompleks og krever multidisiplinær tilnærming. Behandlingen av slike sjeldne tilstander krever høyt spesialiserte tjenester. Den bør derfor sentraliseres og utvikles innenfor rammen av et multidisiplinært kraniofacialt team.
Svulster som involverer skallebasis er ofte vanskelig tilgjengelige
Svulster i de sentrale eller mediale sonene av skallens basis i fremre og midtre skallegrop kan opereres nedenfra, gjennom ansiktet
Den kirurgiske tilgangen til slike svulster er imidlertid svært vanskelig og ofte ledsaget av betydelig morbiditet
Transfacial kirurgi bør derfor sentraliseres og videreutvikles innenfor rammen av et multidisiplinært kraniofacialt team
- 1.
Sekhar LN, Nanda A, Sen CN, Snyderman CN, Janecka IP. The extended frontal approach to tumors of the anterior, middle, and posterior skull base. J Neurosurg 1992; 76: 198 – 206.
- 2.
Al-Mefty O, Smith RR. Tuberculum sellae meningiomas. I: Al-Mefty O, red. Meningiomas. New York: Raven, 1991: 395 – 411.
- 3.
Boysen M, Due-Tønnessen B, Helseth E, Langmoen IA, Lindegaard KF, Sorteberg W et al. Reseksjon av maligne svulster med relasjon til fremre skallegrop Tidsskr Nor Lægeforen 2001; 121: 1688 – 91.
- 4.
Hassler W, Zentner J. Pterional approach for surgical treatment of olfactory groove meningioma. Neurosurgery 1989; 25: 942 – 5.
- 5.
Sekhar LN, Janecka IP, Jones NF. Subtemporal-infratemporal and basal subfrontal approach to extensive cranial base tumors. Acta Neurochir 1988; 92: 83 – 92.
- 6.
Frank G, Pasquini E, Mazzatenta D. Extended transsphenoidal approach. J Neurosurg 2001; 95: 917 – 8.
- 7.
Eisig SB, Feghali J, Hall C, Goodrich JT. The 2-piece LeFort I osteotomy for cranial base access: an evaluation of 9 patients. J Oral Maxillofac Surg 2000; 58: 482 – 6.
- 8.
Williams WG, Lo LJ, Chen YR. The LeFort I palatal split approach for skull base tumors: efficacy, complications, and outcome. Plast Reconstr Surg 1998; 102: 2310 – 9.
- 9.
James D, Crockard HA. Surgical access to the base of skull and upper cervical spine by extended maxillotomy. Neurosurgery 1991; 29: 411 – 6.
- 10.
Ross DA, Wilson CB. Results of transsphenoidal microsurgery for growth hormone-secreting pituitary adenoma in a series of 214 patients. J Neurosurg 1988; 68: 854 – 67.
- 11.
Laws ER jr. Vascular complications of transspehnoidal surgery. Pituitary 1999; 2: 163 – 70.
- 12.
Beals SP, Joganic EF, Holcombe TC, Spetzler RF. Secondary craniofacial problems following skull base surgery. Clin Plast Surg 1997; 24: 565 – 81.
- 13.
Ogilvy CS, Barker FG 2nd, Joseph MP, Cheney ML, Swearingen B, Crowell RM. Transfacial transclival approach for midline posterior circulation aneurysms. Neurosurgery 1996; 39: 736 – 41.
- 14.
Hadley MN, Spetzler RF, Sonntag VK. The transoral approach to the superior cervical spine. A review of 53 cases of extradural cervicomedullary compression. J Neurosurg 1989; 71: 16 – 23.
- 15.
Robinson JR jr, Golfinos JG, Spetzler RF. Skull base tumors. A critical appraisal and clinical series employing image guidance. Neurosurg Clin North Am 1996; 7: 297 – 311.