På verdensbasis er ovarialcancer den sjette vanligste kreftformen blant kvinner, og fører til ca. 100 000 dødsfall årlig (1, 2). I den vestlige delen av verden er mortaliteten av ovarialcancer høyest blant de gynekologiske kreftformene. I 1996 ble det diagnostisert 470 nye tilfeller i Norge, og 331 kvinner døde av sykdommen (3, 4). Sannsynligheten for at en kvinne skulle utvikle ovarialcancer i løpet av sin levetid var 1,8 % i perioden 1988 – 92 (5). Det er spesielt de eldre kvinnene som rammes. I perioden 1989 – 93 var medianalderen 65 år (6). I samme periode ble 28 % av tilfellene diagnostisert i et lokalisert stadium, 4 % med regional spredning, 64 % med fjernspredning og 3,8 % med ukjent utbredelse (6). I denne perioden var femårs relativ overlevelse for pasienter med ovarialcancer 37 %, og varierte fra 77 % for pasienter med lokalisert sykdom til 19 % for pasienter med fjernspredning (7). Mortalitetsratene i Norge er høye, og har stort sett vært uforandret siden 1960-årene (5).
Stadiefordelingen av sykdommen er lite gunstig, samtidig som det er stor forskjell i prognose mellom tilfeller som oppdages tidlig i sykdomsutviklingen i forhold til dem som oppdages sent. Dette har ført til en økende interesse for screening som kan avdekke sykdommen på et tidlig stadium, hvor utsikten til helbredelse er relativt god. Bl.a. er det vist at ved å øke andelen krefttilfeller som diagnostiseres i stadium 1 fra 25 % til 50 – 75 %, vil dødeligheten av sykdommen kunne avta med 20 – 40 % (8, 9). Relativt sett er dette sammenliknbart med effekten av mammografiscreening.
Screening er per definisjon prosessen for å identifisere preklinisk sykdom hos asymptomatiske individer, helst ved hjelp av en relativt enkel test (10). Formålet med screening er å redusere mortaliteten eller morbiditeten til pasientene som har den sykdommen man screener med henblikk på. Bare et mindre antall kreftsykdommer egner seg for screening. Dette skyldes bl.a. at en rekke forutsetninger må være til stede for at screeningprogrammene skal ha den tilsiktede effekten (11).
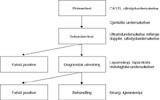
I denne artikkelen omtaler vi ulike forhold ved ovarialcancerscreening. Dette vil innbefatte forhold ved selve kreftsykdommen, ulike screeningtester, fordeler og ulemper ved screening, målgrupper, kostnad-nytte-vurderinger, pågående studier, samt screening av høyrisikogrupper. Figur 1 gir en skjematisk oversikt over de ulike trinnene i et program for ovarialcancerscreening.
Sykdom
Histologi
Ovarialcancer består av en heterogen gruppe kreftformer. Mer enn 90 % av krefttilfellene er epiteliale (6). Serøse tumorer utgjør her den største undergruppen (>40 %). Sexcord/stromacelle- og germinalcellesvulster utgjør majoriteten av de ikke-epiteliale krefttilfellene.
Borderlinetumorer i ovariene, som er epiteliale svulster med et lavt malignitetspotensial, ble først akseptert som en egen enhet i begynnelsen av 1970-årene (12, 13). Disse tumorene utgjør 10 – 15 % av de epiteliale svulstene. Majoriteten av borderlinetumorene er mucinøse (>50 %) og serøse (>40 %) (6).
Patogenese/etiologi
Selve patogenesen ved ovarialcancer er dårlig kartlagt. Gjentatte eggløsninger synes imidlertid å være av betydning for utviklingen av maligne forandringer i overflateepitelet. I 1971 ble hypotesen om ”incessant ovulation” fremsatt (14). Etter eggløsningen fører den mitotiske aktiviteten som kreves for å reparere ovarialepitelet, til en økt risiko for genetiske abnormiteter, slik som mutasjoner i p53-genet, som igjen predisponerer for malign transformasjon (15). En alternativ hypotese er at høye nivåer av sirkulerende gonadotropiner kan indusere maligne forandringer i epitelet (16).
Risikofaktorer/beskyttende faktorer
De viktigste risikofaktorene for utvikling av ovarialcancer er opphopning av ovarialcancer og brystcancer i familien, samt nedarvede mutasjoner i BRCA1- og BRCA2-genene (17). Økende alder og nordeuropeisk eller nordamerikansk avstamning har også betydning.
De to best kjente beskyttende faktorene er bruk av p-piller og høy paritet. P-pillebrukere har en ca. 40 % redusert risiko sammenliknet med ikke-brukere (18). Størrelsen på denne risikoreduksjonen øker med varigheten av og med yngre alder ved start av p-pillebruken. I tillegg er risikoen redusert minst 15 år etter avsluttet bruk. En signifikant reduksjon i risikoen for ovarialcancer er også vist blant kvinner med mutasjoner i BRCA1- og BRCA2-genene ved bruk av p-piller (19). En norsk prospektiv studie av mer enn 1,1 millioner kvinner har vist en redusert risiko for epitelial ovarialcancer med økende antall fullgåtte svangerskap. Imidlertid ble det ikke observert noen ytterligere risikoreduksjon etter den tredje fullgåtte graviditeten (20). Noen studier har også funnet en beskyttende effekt av amming (21).
Diagnose og behandling
Klinikken ved ovarialcancer kjennetegnes av ukarakteristiske abdominalplager, følelse av trykk og oppfylthet, økt abdominalomfang, endret avførings- eller vannlatingsmønster, vekttap og allmennsymptomer. Også akutte smerter kan oppstå ved torkvering eller ruptur/blødning (22).
Viktige preoperative undersøkelser er gynekologisk undersøkelse med bimanuell palpasjon (vurdering av ovariene og livmor), ultralydundersøkelse, s-CA125 og røntgen thorax. Eventuelt utføres colonundersøkelser ved mistanke om tarmaffeksjon og undersøkelse av endometriet ved uklar tumortilstand med blødning. Den endelige diagnosen stilles som oftest først med laparotomi.
Ovarialcancer deles inn i fire stadier med undergrupper etter sykdommens utbredelse på diagnosetidspunktet. Stadieinndelingen baserer seg både på klinisk undersøkelse og operasjonsfunn.
Kirurgi er hovedbehandlingen for denne gruppen pasienter. Hensikten med primæroperasjonen er stadiebestemmelse og maksimal tumorreduksjon. Standard kirurgisk prosedyre er fjerning av uterus med begge adnekser og omentreseksjon. Ved lokalisert sykdom fjernes lymfeknuter i bekkenet, samt paraaortalt. Pasienter med diploide borderlinetumorer og høyt differensierte tumorer i stadium 1 ansees ferdigbehandlet med operasjon. Høyrisikopasienter med sykdom i stadium 1 og 2 og pasienter med mer avansert sykdom behandles med kirurgi etterfulgt av paklitaksel (Taxol)-basert kjemoterapi.
Tester
I screeningsammenheng må en hensiktsmessig test kunne identifisere sykdommen i en preklinisk fase. Testens egenskaper beskrives ofte ved dens sensitivitet og spesifisitet. Sensitiviteten uttrykker hvor godt testen er egnet til å identifisere personer med sykdommen, mens spesifisiteten er et uttrykk for testens evne til å identifisere personer uten sykdommen (11). Verdiene på de nevnte begrepene bør være nærmest mulig 1 (100 %). Lav sensitivitet fører til at mange av dem med sykdommen ikke blir oppdaget, mens lav spesifisitet medfører at mange som ikke har sykdommen blir gjenstand for unødige diagnostiske utredninger. Dette siste er spesielt viktig for ovarialcancerscreening, ettersom resultatet av en falskt positiv test vil kunne bli et unødvendig kirurgisk inngrep. Et annet viktig begrep er testens positive prediktive verdi. Dette er et mål for hvor mange av dem med et positivt testresultat som reelt sett har sykdommen. Jacobs & Oram har vist at ved årlig screening av en postmenopausal, kvinnelig befolkning i England måtte en screeningtest, selv med en 100 % sensitivitet, ha en spesifisitet på 99,6 % for å få en positiv prediktiv verdi på 10 % (23). Dette medfører at selv ved en så høy spesifisitet vil ti kirurgiske inngrep bli utført for hver ovarialcancer som oppdages.
Klinisk undersøkelse
Historisk sett har klinisk undersøkelse med bimanuell palpasjon vært den eneste måten man kunne oppdage en ovarialcancer på. En slik undersøkelse har imidlertid både for lav sensitivitet og spesifisitet til å kunne være en god screeningtest. I tillegg vil en årlig gynekologisk undersøkelse av større befolkningsgrupper være svært ressurskrevende og kostbar (24).
Tumormarkører
Cancerantigen 125 (CA125). Mange serummarkører er blitt vurdert som screeningtester for ovarialcancer. Den markøren som har fått mest oppmerksomhet er CA125, et glykoprotein som produseres ved en del former for ovarialcancer, hovedsakelig de ikke-mucinøse. Forhøyede nivåer av CA125 er blitt rapportert for ca. 80 % av alle tilfeller av ovarialcancer, og for ca. 50 % av krefttilfellene i stadium 1 (24). Forhøyede nivåer av CA125 er også blitt rapportert for andre kreftformer som f.eks. mamma-, endometrie-, ventrikkel-, lunge- og coloncancer. I tillegg er forhøyede nivåer blitt rapportert for en rekke fysiologiske tilstander som graviditet og menstruasjon, og benigne tilstander som endometriose, myomer og akutt bekkeninfeksjon (pelvic inflammatory disease, PID). Det har vist seg at CA125-målinger har lavere spesifisitet hos premenopausale enn postmenopausale kvinner. Dette skyldes trolig forhøyede CA125-nivåer i forbindelse med menstruasjon og ulike benigne tilstander. Gjentatte CA125-målinger har imidlertid indikert at pasienter med ovarialcancer har stigende nivåer, mens kvinner med andre tilstander har stabile nivåer over tid (25).
CA125 ble først beskrevet av Bast og medarbeidere (26) i 1981. Denne markøren har etter hvert vist seg som en nyttig test for å følge behandlingsresponsen, både på kirurgisk behandling og kjemoterapi (27). CA125 er også blitt brukt sammen med ultralydfunn og menopausestatus i konstruksjonen av en risikoindeks (risk of malignancy index, RMI) for preoperativt å identifisere en avansert ovarialcancer blant pasienter med oppfylning i bekkenet (28, 29).
Verdien av CA125 i tidligdiagnostikk av ovarialcancer fikk oppmerksomhet midt i 1980-årene (30). Senere ble det bl.a. i en retrospektiv studie fra den norske Janus-banken, vist at halvparten av prøvene som ble samlet innen 18 måneder før ovarialcancerdiagnosen ble stilt, hadde forhøyede nivåer av CA125 (>30 U/ml) (31). En av de første forsøkene på å bruke CA125 som screeningtest ble rapportert av Jacobs og medarbeidere i 1988 (32). Senere har også andre forfattere vurdert verdien av CA125 som screeningtest i prospektive studier (33). Det har imidlertid vist seg at CA125 ikke har høy nok sensitivitet til å bli brukt som en enkeltstående screeningtest. CA125 brukes derfor hovedsakelig som screeningtest i kombinasjon med ultralydundersøkelse eller som primærtest med etterfølgende ultralydundersøkelse av de kvinnene som har forhøyede CA125-nivåer. Sensitiviteten av en CA125-måling etterfulgt av ultralydundersøkelse er ca. 80 % (95 % konfidensintervall 49 % – 95 %), og andelen falskt positive testresultater ved denne screeningstrategien varierer fra 0,1 % til 0,6 % (9).
OVX1. En rekke andre markører er blitt kombinert med CA125 for å forsøke å forbedre sensitiviteten og spesifisiteten til denne screeningtesten. OVX1 som er et monoklonalt antistoff, er den mest lovende i så måte (34). I en amerikansk studie fra 1993 ble det vist at 70 % av pasientene med klinisk ovarialcancer hadde et forhøyet nivå av OVX1 sammenliknet med bare 5 % av kontrollpersonene (35). I samme studie ble det også vist at når CA125 (> 35 U/ml) og OVX1 (> 10,5 U/ml) ble brukt i kombinasjon, ble persisterende sykdom påvist hos 56 % av pasientene sammenliknet med 35 % når CA125 ble brukt alene. Videre er det vist at 65 % av kvinnene med sykdom i stadium 1 hadde forhøyet CA125-nivå, mens bare 48 % hadde forhøyet OVX1-nivå. Imidlertid hadde 87 % enten forhøyet nivå av CA125 eller OVX1 (36).
Andre markører. LPA (lysophosphatidic acid) er en ny markør som muligens kan representere en sensitiv test for ovarialcancer, spesielt i tidlige stadier (37). Også flere andre tumormarkører for ovarialcancer er blitt undersøkt. Mange av disse har vist seg å ha for lav sensitivitet og spesifisitet. I tillegg korrelerer mange av disse markørene dårlig med klinisk status, er bare forhøyet i avanserte stadier, eller gir liten tilleggsgevinst når de brukes sammen med CA125 (38).
Ultralydundersøkelse
Ultralydundersøkelse visualiserer ovariene, og kan vise endringer i størrelse, form og morfologi som indikerer patologiske forandringer. Ultralydundersøkelse kan utføres transabdominalt eller transvaginalt. Ettersom transvaginal ultralydundersøkelse ofte gir et mer detaljert morfologisk bilde, foretrekkes denne metoden. I tillegg trenger ikke pasienten å undersøkes med full blære når undersøkelsen utføres transvaginalt, noe som kan gjøre det lettere å akseptere metoden.
Kriterier for å definere et patologisk forstørret ovarium varierer med menopausestatus og alder. Permanent forstørrede ovarier eller ovarier med et ”patologisk” utseende kan oppstå som resultat både av benigne og maligne forandringer. Retningslinjer for å skille mellom benigne og maligne tilstander basert på ultralydforandringer foreligger, og flere ulike morfologiske skåringssystemer er blitt beskrevet (39 – 41).
Bruk av ultralydundersøkelse som screeningtest ble først foreslått i begynnelsen av 1980-årene. Den største studien der transabdominal ultralydundersøkelse ble brukt som screeningtest, ble rapportert av Campbell og medarbeidere i 1989 (42). I denne studien ble det funnet en spesifisitet på 97,7 %, en falskt positiv rate på 2,3 % og en positivt prediktiv verdi på 1,5 %.
I slutten av 1980-årene ble transvaginal ultralydundersøkelse mer aktuell som screeningtest. Selv om sensitiviteten ved bruk av transvaginal ultralydundersøkelse er høy (nærmere 100 %), har spesifisiteten og den positivt prediktive verdien vært mer moderate. Bl.a. ble det i en amerikansk studie fra 1993 rapportert en spesifisitet på 98,7 % og en positiv prediktiv verdi på 6,8 % for denne screeningtesten (43).
Fargedoppler
En nyere teknikk som kan brukes til å skille maligne tilstander fra benigne, er transvaginal fargedoppler. Denne teknikken brukes sammen med ultralydundersøkelse. Metoden visualiserer blodkarene i ovariene og karakteriserer blodstrømsmønsteret. Maligne tumorer induserer danning av nye blodkar. Disse er dårlig organiserte og har redusert mengde glatt muskulatur i veggene. Dette fører til en redusert motstand mot blodstrømmen, og således til en høyere blodstrømshastighet (9). Fargedoppler er altså et tillegg til ultralydundersøkelse (sekundærtest), og har vist seg å øke undersøkelsens sensitivitet og spesifisitet (44). Imidlertid er det rapportert store variasjoner i denne metodens evne til å skille maligne fra benigne tilstander (45).
Multimodal screening
En ideell test for ovarialcancerscreening må kombinere en svært høy spesifisitet for å unngå unødvendige kirurgiske inngrep, med en akseptabel sensitivitet. Mye tyder på at transvaginal ultralydundersøkelse er den beste screeningtesten for å oppdage tidlig ovarialcancer, men ingen enkeltstående screeningtest har så langt vist seg å ha en akseptabel spesifisitet blant postmenopausale kvinner. Imidlertid har kombinasjonen av ulike screeningtester (CA125 og ultralydundersøkelse) vist seg å øke validiteten. I en britisk screeningstudie av ca. 22 000 kvinner over 45 år fra 1993 hvor det ble brukt en sekvensiell kombinasjon av CA125 og ultralydundersøkelse, ble det oppnådd en sensitivitet på 78,6 % etter ett år, en spesifisitet på 99,9 % og en positiv prediktiv verdi på 26,8 % (46). Også senere studier har bekreftet nytten av multimodal screening (47).
Enkelte høyrisikogrupper peker seg også ut for denne typen screening. En norsk studie fra 1996 har bekreftet nytten av multimodal diagnostikk i screening av 180 kvinner med risiko for arvelig ovarialcancer. Etter ett år hadde undersøkelse med transvaginal ultralydundersøkelse en sensitivitet og spesifisitet på henholdsvis 78 % og 99,4 %. Effekten på overlevelsen er imidlertid ikke klarlagt (48).
Genetisk testing
Med arvelig ovarialcancer forstås her autosomalt dominant sykdom, med høy penetrans og relativt tidlig debut. Genetisk testing av friske kvinner er en trinnvis prosess som starter med en grundig utredning av kvinnens familiehistorie med henblikk på cancer og genetisk veiledning. Nære slektningers cancerdiagnoser kontrolleres (histologi) og kvinnens risiko for sykdom beregnes.
Per dags dato er det ingen av de eksisterende genetiske testene som egner seg for screening av friske kvinner. Derimot er screening av kvinner med ovarialcancer med henblikk på hyppige genfeil (BRCA1- og BRCA2-mutasjoner), på trappene.
Friske kvinner i familier med økt risiko bør tilbys en prediktiv gentest når:
– Genfeilen er påvist hos nær slektning med cancer
– Testen kan tolkes tilfredsstillende
– Resultatet vil føre til medisinsk oppfølging av kvinnen og hennes slektninger med tanke på tidlig cancerdiagnose og bedre overlevelse
Hvis testen er positiv, skal kvinnen informeres om egen livstidsrisiko for sykdommen og de medisinske tiltak som tilbys, slik som screening, eventuell kjemoprevensjon (p-piller) og profylaktisk kirurgi.
Fordeler og ulemper ved screening
Fordeler
Et randomisert, kontrollert forsøk for å evaluere effekten av screening på mortaliteten av ovarialcancer er til nå ikke blitt gjennomført. Imidlertid har nyere data indikert at screening kan øke overlevelsen for kvinner med denne sykdommen (47). Disse resultatene er basert på en britisk pilotstudie av ovarialcancerscreening blant postmenopausale kvinner over 45 år. Studien inkluderte ca. 22 000 kvinner randomisert i forholdet 1 : 1. Kvinnene i intervensjonsgruppen ble tilbudt årlig undersøkelse med CA125 og ultralydundersøkelse i tre år. Median overlevelsestid for kvinner med ovarialcancer i intervensjonsgruppen var 73 måneder mot 42 måneder i kontrollgruppen (p = 0,01). Forfatterne understreket imidlertid at resultatene var preliminære, og at en større randomisert studie var nødvendig for å bekrefte funnene.
En endret stadiefordeling, i den forstand at en økende andel av krefttilfellene oppdages på et tidligere stadium, er et foreløpig mål på effekten av screening. I populasjonsbaserte screeningstudier (prevalensscreening/1. screeningrunde) hvor det ble brukt CA125 som primærtest etterfulgt av ultralydundersøkelse, ble 50 % (95 % konfidensintervall 23 % – 77 %) av tilfellene oppdaget i stadium 1. I studier der man brukte ultralydundersøkelse som primærtest, ble 75 % (95 % konfidensintervall 35 % – 97 %) av tilfellene oppdaget i stadium 1 (9). Til sammenlikning ble ca. 32 % av tilfellene av epitelial ovarialcancer som ble behandlet ved Det Norske Radiumhospital fra Sørøst-Norge i perioden 1975 – 94, diagnostisert i stadium 1 (49).
En annen positiv effekt av screening er en økt oppmerksomhet omkring og økt kunnskap om sykdommen i befolkningen.
Ulemper
Screening er undersøkelse av presumptivt friske kvinner med henblikk på å oppdage tidlig sykdom i motsetning til undersøkelse av kvinner som pga. symptomer selv oppsøker helsevesenet. Fordi kvinnene i utgangspunktet er friske, har helsevesenet et spesielt ansvar for ikke å påføre dem noen ytterligere skade.
Potensielle ulemper ved ovarialcancerscreening er bl.a. overdiagnostisering og overbehandling av kvinner med benigne tilstander som ellers ikke ville ha ført til noen økt sykelighet i løpet av kvinnens levetid.
Videre har man ved ovarialcancerscreening særlig vært opptatt av de psykiske påkjenningene ved et falskt positivt prøvesvar og på risikoen for sykelighet og dødelighet i forbindelse med utredning og diagnose. Imidlertid har bare et relativt lite antall studier undersøkt de psykiske påkjenningene ved ovarialcancerscreening. For de fleste kvinner vil de psykiske påkjenningene ved et falskt positivt prøvesvar være av kort varighet, og bare et lite antall kvinner vil få langtidseffekter. Også når det gjelder diagnostisk kirurgi er det et begrenset antall studier som har dreid seg om komplikasjonsraten. Imidlertid er det på bakgrunn av noen større serier beregnet at 0,5 – 1% av kvinnene vil få ulike kirurgiske komplikasjoner i forbindelse med laparoskopisk ooforektomi (9).
Målgruppe
For at en sykdom skal egne seg for screening må den bl.a. utgjøre et alvorlig helseproblem i tillegg til at det finnes en god screeningtest for sykdommen. Den relativt lave insidensen av ovarialcancer blant premenopausale kvinner i tillegg til den lavere spesifisitet av screeningtestene i denne gruppen, gjør de postmenopausale kvinnene til en passende målgruppe for screening.
Kvinner i familier med et hereditært ovarialcancer-syndrom har en høy insidens av sykdommen, men utgjør bare 5 – 10 % av alle ovarialcancertilfellene. Screening er klart viktig for denne høyrisikogruppen, men vil bare ha en relativt beskjeden effekt på den totale mortaliteten av sykdommen.
Lite informasjon er tilgjengelig når det gjelder effekten av gjentatte screenningrunder og optimalt intervall mellom disse. Imidlertid har de fleste studier anvendt årlige screeningintervall.
Kostnad-nytte-vurderinger
Ulike matematiske modeller er blitt benyttet for å beregne hvor mange ekstra leveår ovarialcancerscreening kan gi. I et screeningprogram for kvinner over 50 år med årlige CA125-målinger, ble det beregnet at 3,4 leveår kunne spares for hvert tilfelle av ovarialcancer som ble oppdaget. Kostnaden for hvert sparte leveår varierte, 95 000 – 36 000 amerikanske dollar, avhengig av testens spesifisitet (50). En nylig presentert modell som sammenliknet årlige transvaginale ultralydundersøkelser med årlige CA125-målinger med etterfølgende ultralydundersøkelse ved forhøyede CA125-nivåer, beregnet at kostnadene per spart leveår var lavere for strategien som inkluderte CA125-målinger (51).
Pågående studier
Tre store randomiserte, kontrollerte studier som vurderer effekten av screening på mortaliteten av ovarialcancer, er blitt satt i gang. I USA har the National Cancer Institute startet ”The Prostate, Lung, Colorectal, Ovarian screening study” (PLCO study). 74 000 kvinner over 60 år vil bli rekruttert til denne studien. Halvparten av kvinnene vil årlig bli undersøkt med bimanuell palpasjon, CA125-målinger og transvaginal ultralydundersøkelse. I Bart-studien i England (St. Bartholomew’s Hospital, London) vil 120 000 postmenopausale kvinner over 50 år bli rekruttert. Halvparten av disse vil bli undersøkt med årlige CA125-målinger etterfulgt av ultralydundersøkelse. ERTOCS-studien (European Randomised Trial of Ovarian Cancer Screening) som er et europeisk samarbeidsprosjekt, tar sikte på å rekruttere 120 000 kvinner i aldersgruppen 50 – 64 år. I denne studien brukes transvaginal ultralydundersøkelse som screeningtest. Alle disse tre studiene startet omkring 1994 – 95. Data som evaluerer effekten på mortaliteten vil ikke være tilgjengelige før år 2003. Imidlertid vil en rekke foreløpige mål kunne presenteres på et tidligere tidspunkt (9).
Høyrisikogrupper
Man antar at 5 – 10 % av all ovarialcancer er arvelig, resten oppstår sporadisk. Tre syndromer er beskrevet. Hereditær mamma-/ovarialcancer er det vanligste, og karakteriseres av en økt risiko både for ovarial- og mammacancer. Om lag 80 % av familiene med hereditær mamma-/ovarialcancer har mutasjoner i BRCA1-genet. Hos BRCA1-mutasjonsbærerne varierer estimatene for risikoen for ovarialcancer før fylte 70 år fra 26 % til 85 % (17, 52 – 54). En mindre andel har mutasjoner i BRCA2-genet, hvor risikoen er beskjeden for ovarialcancer, men høy for mammacancer. Hereditær ”site-specific” ovarialcancer karakteriseres av en økt risiko for ovarialcancer, men ikke for andre kreftformer. Lynch II-syndromet (hereditær ikke-polypøs kolorektal cancer, HNPCC) skyldes mutasjoner i DNA-reparasjonsgener, og karakteriseres av en økt risiko for gastrointestinal cancer og for endometriecancer. Også ovarialcancer kan forekomme som en del av dette syndromet. Gynekologisk screening av høyrisikogruppene virker lovende per dags dato. Fortsatt mangler imidlertid påviste effekter av screening i disse gruppene, som for eksempel en bedret overlevelse og en redusert mortalitet (55).
Anbefalinger
Ekspertgruppen til UICC (The International Union Against Cancer) konkluderte i 1990 med at screening mot ovarialcancer ikke kunne anbefales som folkehelsetiltak fordi ingen data var tilgjengelig som viste noen effekt på mortaliteten av sykdommen (56). Konsensuskonferansen til National Institutes of Health i USA konkluderte i 1994 med at det ikke finnes tilgjengelige bevis for at CA125-målinger og transvaginal ultralydundersøkelse kan brukes som screeningtester i befolkningssammenheng for å redusere dødeligheten av ovarialcancer, og at bruken av disse testene vil føre til redusert i stedet for økt morbiditet og mortalitet (57). I Norsk kreftplan fra 1997 ble det også konkludert med at det ikke foreligger bevis for at populasjonsbasert screening vil føre til redusert sykelighet og dødelighet av sykdommen (58). Ovarialcancerscreening ble således ikke anbefalt. Derimot ble det anbefalt å hindre villscreening, slik at ressursene kunne brukes på å screene med henblikk på sykdommer hvor det er dokumentert at screening har en effekt.
I 1997 utformet Cancer Genetics Studies Consortium i National Human Genome Research Institute i USA retningslinjer for medisinsk oppfølging av kvinner med økt risiko for mamma- og ovarialcancer (59). Det ble anbefalt halvårlige eller årlige kontroller med gynekologisk undersøkelse, transvaginal ultralydundersøkelse med fargedoppler og CA125-målinger. Det ble ikke gitt noen anbefalinger med hensyn til profylaktisk ooforektomi, men mutasjonsbærere (BRCA1) skal informeres om at dette er et alternativ for dem. Muligheten for peritoneal karsinomatose foreligger imidlertid selv etter at ovariene er fjernet, og er rapportert for 2 – 11 % (60, 61). I Norge tilbys høyrisikogruppen bl.a. årlige transvaginale ultralydundersøkelser kombinert med CA125-målinger hvert halvår fra 30 – 35 års alder (62). Ved menopause eller fra 45-årsalderen anbefales profylaktisk salpingo-ooforektomi. Hos mutasjonsbærere anbefales dette fra 40-årsalderen.
Konklusjon
Ovarialcancer er en hyppig kreftform i den vestlige delen av verden. Selv om det har vært en moderat forbedring i overlevelsesratene de siste tiårene, er prognosen ved sykdommen fortsatt dårlig. Denne kreftformen har imidlertid et stort screeningpotensial ettersom prognosen er sterkt avhengig av stadium på diagnosetidspunktet. Det er likevel flere av kravene til effektiv screening som ikke tilfredsstilles ved ovarialcancer. Sykdommens naturlige utvikling er ikke klart nok definert, gode screeningtester med høy sensitivitet og spesifisitet mangler, og effekten på mortaliteten er mangelfullt dokumentert. Ikke desto mindre har nyere data indikert at screening kan øke overlevelsen for kvinner med ovarialcancer. Screening for å avdekke tidlig sykdom kan synes å være av verdi for kvinnene i høyrisikogruppene (arvelig ovarialcancer).
- 1.
Parkin DM, Pisani P, Ferlay J. Estimates of the worldwide incidence of 25 major cancers in 1990. Int J Cancer 1999; 80: 827 – 41.
- 2.
Pisani P, Parkin DM, Bray F, Ferlay J. Estimates of the worldwide mortality from 25 cancers in 1990. Int J Cancer 1999; 83: 18 – 29.
- 3.
Kreftregisteret. Cancer in Norway 1996. Oslo: Kreftregisteret, 1999.
- 4.
Statistisk sentralbyrå. www.ssb.no/emner/03/01/10/dodsarsak/tab-1999-xx-xx-02.html (4.2.2000).
- 5.
Bjørge T, Engeland A, Hansen S, Tropé CG. Ovarialcancer og borderlinetumorer. Tidsskr Nor Lægeforen 1998; 118: 2471 – 5.
- 6.
Bjørge T, Engeland A, Hansen S, Tropé CG. Trends in the incidence of ovarian cancer and borderline tumours in Norway, 1954 – 93. Int J Cancer 1997; 71: 780 – 6.
- 7.
Bjørge T, Engeland A, Hansen S, Tropé CG. Prognosis of patients with ovarian cancer and borderline tumours diagnosed in Norway between 1954 and 1993. Int J Cancer 1998; 75: 663 – 70.
- 8.
Woodman R. Not enough evidence to justify ovarian cancer screening. BMJ 1999; 318: 687.
- 9.
Bell R, Petticrew M, Luengo S, Sheldon TA. Screening for ovarian cancer: a systematic review. Health Technol Assess 1998; 2: 1 – 84.
- 10.
Hakama M. Screening. I: Holland W, Detels R, Knox G, red. Oxford textbook of public health. Oxford: Oxford University Press, 1991: 91 – 106.
- 11.
Bjørge T, Tropé CG, Engeland A. Screening mot kreft. Tidsskr Nor Lægeforen 1999; 119: 1129 – 36.
- 12.
Ingelman-Sundberg A. Classification and staging of malignant tumors in the female pelvis. Acta Obstet Gynecol Scand 1971; 50: 1 – 7.
- 13.
Serow SF, Scully RE, Sobin LH. Histologic typing of ovarian tumors. Genève: WHO, 1973.
- 14.
Fathalla MF. Incessant ovulation – a factor in ovarian neoplasia? Lancet 1971; 2: 163.
- 15.
Godwin AK, Testa JR, Hamilton TC. The biology of ovarian cancer development. Cancer 1993; 71: 530 – 6.
- 16.
Stadel BV. The etiology and prevention of ovarian cancer. Am J Obstet Gynecol 1975; 123: 772 – 4.
- 17.
Ford D, Easton DF. The genetics of breast and ovarian cancer. Br J Cancer 1995; 72: 805 – 12.
- 18.
Franceschi S, Parazzini F, Negri E, Booth M, LaVecchia C, Beral V et al. Pooled analysis of 3 European case-control studies of epithelial ovarian cancer: III, oral contraceptive use. Int J Cancer 1991; 49: 61 – 5.
- 19.
Narod SA, Risch H, Moslehi R, Dørum A, Neuhausen S, Olsson H et al. Oral contraceptives and the risk of hereditary ovarian cancer. N Engl J Med 1998; 339: 424 – 8.
- 20.
Albrektsen G, Heuch I, Kvåle G. Reproductive factors and incidence of epithelial ovarian cancer: a Norwegian prospective study. Cancer Causes Control 1996; 7: 421 – 7.
- 21.
Whittemore AS, Harris R, Itnyre J, Collaborative Ovarian Cancer Group. Characteristics relating to ovarian cancer risk: collaborative analysis of 12 US case-control studies. II. Invasive epithelial ovarian cancers in white women. Am J Epidemiol 1992; 136: 1184 – 203.
- 22.
Onsrud M, Tropé C, Iversen O-E. Ovarialcancer. I: Norsk gynekologisk forening. Veileder i gynekologisk onkologi 1997. Oslo: Den norske lægeforening, 1997: 36 – 40.
- 23.
Jacobs I, Oram D. Screening for ovarian cancer. Biomed Pharmacother 1988; 42: 589 – 96.
- 24.
Pearson VAH. Screening for ovarian cancer: a review. Public Health 1994; 108: 367 – 82.
- 25.
Zurawski VR, Sjovall K, Schoenfeld DA, Broderick SF, Hall P, Bast RC et al. Prospective evaluation of serum CA125 levels in a normal population, Phase I: the specificities of single and serial determinations in testing for ovarian cancer. Gynecol Oncol 1990; 36: 299 – 305.
- 26.
Bast RC, Feeney M, Lazarus H, Nadler LM, Colvin RB, Knapp RC. Reactivity of a monoclonal antibody with human ovarian carcinoma. J Clin Invest 1981; 68: 1331 – 7.
- 27.
Makar AM. Prognostic studies in cancer of the ovary and fallopian tube with emphasis on the CA125 antigen and c-erbB-2 oncogene. Oslo: Det Norske Radiumhospital, 1993.
- 28.
Jacobs I, Oram D, Fairbanks J, Turner J, Frost C, Grudzinskas JG. A risk of malignancy index incorporating CA125, ultrasound and menopausal status for the accurate preoperative diagnosis of ovarian cancer. Br J Obstet Gynaecol 1990; 97: 922 – 9.
- 29.
Tingulstad S, Hagen B, Skjeldestad FE, Halvorsen T, Nustad K, Onsrud M. The risk-of-malignancy index to evaluate potential ovarian cancers in local hospitals. Obstet Gynecol 1999; 93: 448 – 52.
- 30.
Bast RC, Siegal FP, Runowicz C, Klug TL, Zurawski VR, Schonholz D et al. Elevation of serum CA125 prior to diagnosis of an epithelial ovarian carcinoma. Gynecol Oncol 1985; 22: 115 – 20.
- 31.
Zurawski VR jr., Ørjaseter H, Andersen A, Jellum E. Elevated serum CA125 levels prior to diagnosis of ovarian neoplasia: relevance for early detection of ovarian cancer. Int J Cancer 1988; 42: 677 – 80.
- 32.
Jacobs I, Stabile I, Bridges J, Kemsley P, Reynolds C, Grudzinskas J et al. Multimodal approach to screening for ovarian cancer. Lancet 1988; 1: 268 – 71.
- 33.
Einhorn N, Sjövall K, Knapp RC, Hall P, Scully RE, Bast RC et al. Prospective evaluation of serum CA125 levels for early detection of ovarian cancer. Obstet Gynecol 1992; 80: 14 – 8.
- 34.
Xu FJ, Yu YH, Li BY, Moradi M, Elg S, Lane C et al. Development of two new monoclonal antibodies reactive to a surface antigen present on human ovarian epithelial cancer cells. Cancer Res 1991; 51: 4012 – 9.
- 35.
Xu FJ, Yu YH, Daly L, DeSombre K, Anselmino L, Hass GM et al. The OVX1 radioimmunoassay complements CA125 for predicting the presence of residual ovarian carcinoma at second look surgical surveillance procedures. J Clin Oncol 1993; 11: 1506 – 10.
- 36.
Woolas RP, Xu FJ, Jacobs IJ, Yu YH, Daly L, Berchuck A et al. Elevation of multiple serum markers in patients with stage I ovarian cancer. J Natl Cancer Inst 1993; 85: 1748 – 51.
- 37.
Xu Y, Shen Z, Wiper DW, Wu M, Morton RE, Elson P et al. Lysophosphatidic acid as a potential biomarker for ovarian and other gynecologic cancers. JAMA 1998; 280: 719 – 23.
- 38.
Berek JS, Bast RC. Ovarian cancer screening. The use of serial complementary markers to improve sensitivity and specificity for early detection. Cancer 1995; 76: 2092 – 6.
- 39.
DePriest PD, Shenson D, Fried A, Hunter JE, Andrews SJ, Gallion HH et al. A morphology index based on sonographic findings in ovarian cancer. Gynecol Oncol 1993; 51: 7 – 11.
- 40.
Cohen CJ, Jennings TS. Screening for ovarian cancer: the role of noninvasive imaging techniques. Am J Obstet Gynecol 1994; 170: 1088 – 94.
- 41.
Granberg S, Norström A, Wikland M. Tumors in the lower pelvis as imaged by vaginal sonography. Gynecol Oncol 1990; 37: 224 – 9.
- 42.
Campbell S, Bhan V, Royston P, Whitehead MI, Collins WP. Transabdominal ultrasound screening for early ovarian cancer. BMJ 1989; 299: 1363 – 7.
- 43.
DePriest PD, van Nagell JR, Gallion HH, Shenson D, Hunter JE, Andrews SJ et al. Ovarian cancer screening in asymptomatic postmenopausal women. Gynecol Oncol 1993; 51: 205 – 9.
- 44.
Bourne T, Campbell S, Steer C, Whitehead MI, Collins WP. Transvaginal colour flow imaging: a possible new screening technique for ovarian cancer. BMJ 1989; 299: 1367 – 70.
- 45.
Tekay A, Jouppila P. Controversies in assessment of ovarian tumors with transvaginal color Doppler ultrasound. Acta Obstet Gynecol Scand 1996; 75: 316 – 29.
- 46.
Jacobs I, Davies AP, Bridges J, Stabile I, Fay T, Lower A et al. Prevalence screening for ovarian cancer in postmenopausal women by CA125 measurement and ultrasonography. BMJ 1993; 306: 1030 – 4.
- 47.
Jacobs IJ, Skates SJ, MacDonald N, Menon U, Rosenthal AN, Davies AP et al. Screening for ovarian cancer: a pilot randomised controlled trial. Lancet 1999; 353: 1207 – 10.
- 48.
Dørum A, Kristensen GB, Abeler VM, Tropé CG, Møller P. Early detection of familial ovarian cancer. Eur J Cancer 1996; 32A: 1645 – 51.
- 49.
Bjørge T, Engeland A, Sundfør K, Tropé CG. Prognosis of 2,800 patients with epithelial ovarian cancer diagnosed during 1975 – 94 and treated at the Norwegian Radium Hospital. Acta Obstet Gynecol Scand 1998; 77: 777 – 81.
- 50.
Carlson KJ, Skates SJ, Singer DE. Screening for ovarian cancer. Ann Intern Med 1994; 121: 124 – 32.
- 51.
Urban N, Drescher C, Etzioni R, Colby C. Use of a stochastic simulation model to identify an efficient protocol for ovarian cancer screening. Control Clin Trials 1997; 18: 251 – 70.
- 52.
Easton DF, Ford D, Bishop DT, Breast Cancer Linkage Consortium. Breast and ovarian cancer incidence in BRCA1-mutation carriers. Am J Hum Genet 1995; 56: 265 – 71.
- 53.
Ford D, Easton DF, Bishop DT, Narod SA, Goldgar DE, Breast Cancer Linkage Consortium. Risk of cancer in BRCA1-mutation carriers. Lancet 1994; 343: 692 – 5.
- 54.
Easton DF, Bishop DT, Ford D, Crockford GP, Breast Cancer Linkage Consortium. Genetic linkage analysis in familial breast and ovarian cancer: results from 214 families. Am J Hum Genet 1993; 52: 678 – 701.
- 55.
Dørum A, Heimdal K, Løvslett K, Kristensen G, Hansen LJ, Sandvei R et al. Prospectively detected cancer in familial breast/ovarian cancer screening. Acta Obstet Gynecol Scand 1999; 78: 906 – 11.
- 56.
Miller AB, Chamberlain J, Day NE, Hakama M, Prorok PC. Report on a workshop of the UICC project on evaluation of screening for cancer. Int J Cancer 1990; 46: 761 – 9.
- 57.
NIH Consensus Conference. Ovarian cancer. Screening, treatment and follow-up. NIH Consensus Development Panel on Ovarian Cancer. JAMA 1995; 273: 491 – 7.
- 58.
Norges offentlige utredninger. Omsorg og kunnskap! Norsk kreftplan. NOU 1997: 20. Oslo: Statens forvaltningstjeneste, Seksjon statens trykning, 1997.
- 59.
Burke W, Daly M, Garber J, Botkin J, Kahn MJE, Lynch P et al. Recommendations for follow-up care of individuals with an inherited predisposition to cancer. II. BRCA1 and BRCA2. JAMA 1997; 277: 997 – 1003.
- 60.
Tobacman JK, Greene MH, Tucker MA, Costa J, Kase R, Fraumeni JF jr. Intra-abdominal carcinomatosis after prophylactic oophorectomy in ovarian-cancer-prone families. Lancet 1982; 2: 795 – 7.
- 61.
Piver MS, Jishi MF, Tsukada Y, Nava G. Primary peritoneal carcinoma after prophylactic oophorectomy in women with a family history of ovarian cancer. A report of the Gilda Radner Familial Ovarian Cancer Registry. Cancer 1993; 71: 2751 – 5.
- 62.
Dørum A, Apold J, Møller P. Arvelig kreft. I: Dalaker K, red. Veileder i gynekologisk onkologi. Norsk gynekologisk forening. Oslo: Den norske lægeforening, 1997: 58 – 61.