Background.
The revised Norwegian biotechnology law implies restrictive use of preimplantation genetic diagnostics- a highly specialised procedure, which is still in an early phase of development.
Material and method.
The paper is based on more than 10 years of clinical experience in preimplantation genetic diagnostics and on literature retrieved through PubMed/Medline.
Results.
According to the biotechnology law, preimplantation genetic diagnostics can only be carried out when strict medical indications are present. Genetic counselling and a fertility work-up are compulsory for couples who wish to receive preimplantation genetic diagnostics.
Interpretation.
Few disorders have an indication for preimplantation genetic diagnostics. It will therefore take time to build up adequate national expertise. For couples with a known risk of serious hereditary disease, preimplantation genetic diagnosis is useful in achieving an uncomplicated pregnancy and a healthy child.
Stortinget vedtok nylig regjeringens forslag til endringer i bioteknologiloven (1, 2). En sentral endring er at man vil tillate begrenset bruk av preimplantatorisk genetisk diagnostikk. Slik diagnostikk utføres på befruktede egg etter in vitro-fertilisering. Egg der man ikke påviser genetiske feil, kan settes inn i livmoren eller fryses ned til en senere anledning, mens egg med genetiske feil blir destruert.
I dag tilbys gravide kvinner som har økt risiko for å få barn med alvorlig genetisk sykdom prenatal diagnostikk. Denne består i blodprøver av kvinnen og ultralyd av fosteret som en screeningmetode. Screeningen medfører at antallet invasive undersøkelser for å diagnostisere genetisk sykdom hos fosteret, som fostervannsprøve og korionbiopsi, blir redusert. Diagnostiseres alvorlig sykdom, kan kvinnen søke om abort.
Preimplantatorisk genetisk diagnostikk utføres vanligvis for å redusere risikoen for å overføre genetisk sykdom til det fremtidige barnet. Par som får utført diagnostikken, er i hovedsak befruktningsdyktige. Mange av parene er av den oppfatning at det er mer etisk riktig å destruere egg med genetiske feil enn å utføre senabort eller føde et barn med alvorlig sykdom. Det første barnet etter preimplantatorisk genetisk diagnostikk ble født i England i 1990 (3). Ved Sahlgrenska universitetssjukhuset i Göteborg tok man i bruk denne formen for diagnostikk i 1994. Nordens første barn etter preimplantatorisk genetisk diagnostikk ble født ved dette sykehuset i 1997. Fordi metoden ikke er tilgjengelig i Norge, har flere norske par søkt hjelp i Göteborg. Det første norske barnet der det ble utført preimplantatorisk genetisk diagnostikk ble født i 2001 etter behandling ved Sahlgrenska universitetssjukhuset.
Målet med denne artikkelen er å gi en oversikt over hvordan utredningen kan gjøres før en eventuell preimplantatorisk genetisk diagnostikk, omtale indikasjonene for undersøkelsen og beskrive metoden samt belyse visse aspekter ved diagnostikken.
Materiale og metode
Artikkelen er basert på mer enn ti års erfaring i bruk av preimplantatorisk genetisk diagnostikk ved Sahlgrenska universitetssjukhuset. Det gis et innblikk i hvordan diagnostikken utføres i Göteborg. I tillegg er det foretatt litteratursøk for å gi en oversikt over viktige sider ved metoden slik den praktiseres internasjonalt.
Genetisk veiledning og fertilitetsutredning
I Göteborg er hvert enkelt par både til genetisk veiledning og til fertilitetsutredning før man beslutter om det skal gjøres preimplantatorisk genetisk diagnostikk. Målet med denne prosessen er ikke at den skal resultere i at det fødes færre barn med arvelig sykdom, men at paret får tilstrekkelig informasjon til å kunne foreta egne valg knyttet til en eventuell ny graviditet. Den genetiske veiledningen gis av en klinisk genetiker som ikke er knyttet til kvinneklinikken. Her diskuteres blant annet risikoen for at et fremtidig barn har den aktuelle sykdommen om diagnostikken ikke blir utført, sykdommens alvorlighetsgrad, hvordan behandlingen gjennomføres og diagnostikkens sikkerhet. I tillegg gis informasjon om alternativer for å få et friskt barn, som bruk av prenatal diagnostikk og mulighetene for adopsjon, sæddonasjon og eggdonasjon.
Ved kvinneklinikken gjennomgår paret en ultralydbasert fertilitetsutredning (4). Paret møter også til samtale hos en av klinikkens sosialkuratorer eller psykologer. På bakgrunn av den genetiske veiledningen, fertilitetsutredningen og den psykososiale vurderingen kommer man frem til om søknaden om preimplantatorisk genetisk diagnostikk skal godkjennes eller avvises.
Indikasjoner og formål
Det er flere indikasjoner og formål med preimplantatorisk genetisk diagnostikk.
X-bunden sykdom og monogen sykdom
For å unngå X-bundne sykdommer bestemmes oftest embryoets kjønn. Eksempler på slike lidelser er Duchennes muskeldystrofi, Beckers muskeldystrofi, Alports syndrom, hemofili A og adrenoleukodystrofi.
Ved monogen sykdom foreligger sykdom knyttet til ett enkelt gen. Eksempler på slike sykdommer er cystisk fibrose, sigdcellesykdom og spinal muskelatrofi.
Kromosomavvik
Embryoet undersøkes for strukturelle kromosomavvik, som inversjon eller translokasjon. For den av foreldrene som for eksempel er bærer av en balansert translokasjon, vil dette vanligvis ikke ha negative helsemessige konsekvenser. Barna kan imidlertid ha ubalanserte translokasjoner, noe som typisk resulterer i misdannelser i flere organsystemer, avvikende utseende og mental retardasjon.
Bestemmelse av vevstype
Denne behandlingen har to hensikter: Ettersom en av foreldrene er bærer av eller har en alvorlig genetisk sykdom, ønsker man diagnostikken utført for å øke sjansen for å få et friskt barn. I tillegg skal det kommende barnet være vevstypelikt med et sykt søsken. Ved å bruke stamceller fra navlesnorsblod eller fra beinmargen til det kommende barnet vil det syke søskenet kunne bli helbredet. Sykdommer som talassemi og Fanconianemi kan behandles med denne metoden. Et kjent eksempel på denne formen for diagnostikk og behandling er historien om talassemisyke Mehmet. Foreldrene ønsket preimplantatorisk genetisk diagnostikk og bestemmelse av vevstype for å få et friskt barn som også kunne være donor for sin bror.
Genetisk screening
Her utføres screening av visse kromosomer ved hjelp av preimplantatorisk genetisk diagnostikk for å undersøke om disse kromosomene er normale i befruktede egg hos par som ikke har noen kjent genetisk sykdom. Siden forekomsten av numeriske kromosomfeil øker med kvinnens alder, er det gjerne kvinner i høy reproduktiv alder som gjennomgår preimplantatorisk genetisk screening. Dessuten blir screeningen ofte utført hos kvinner som har opplevd gjentatte spontanaborter eller som ikke har lyktes å bli gravide på tross av flere behandlinger med in vitro-fertilisering.
Genmutasjoner
Hos personer som har fått diagnostisert arvelige genmutasjoner som disponerer for blant annet tidlig utvikling av Alzheimers sykdom, brystkreft eller tykktarms-/endetarmskreft kan diagnostikken utføres. Den britiske myndigheten som regulerer bruken av preimplantatorisk genetisk diagnostikk, Human Fertilisation and Embryology Authority, vedtok i 2006 at dersom risikoen for arvelig kreft er minst 80 %, kan diagnostikken benyttes.
Kjønnsbestemmelse
Her bestemmes embryoets kjønn ved hjelp av preimplantatorisk genetisk diagnostikk fordi foreldrene ønsker at barnet skal være av et bestemt kjønn. Det foreligger ingen medisinsk indikasjon for diagnostikken.
Biopsitaking
Tre ulike typer biopsier benyttes til diagnostikken:
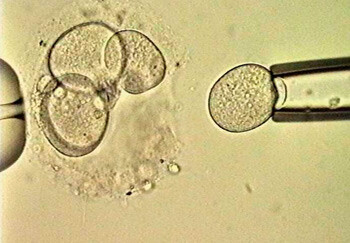
Blastomerbiopsi – Biopsien tas her vanligvis på tredje dagen etter egguttak (5, 6). Det befruktede egget består på dette tidspunktet av ca. åtte celler (blastomerer). Man lager et hull i zona pellucida (eggskallet) ved hjelp av laser eller en syre. Deretter føres en biopsipipette inn via hullet og en eller to blastomerer aspireres (fig 1). Aspirerte blastomerer blir så benyttet til preimplantatorisk genetisk diagnostikk.
Pollegemebiopsi – Ved denne metoden tas pollegemene ut fra egget via et hull i zona pellucida (7). Begge pollegemene er nødvendig for at man skal få en så bra diagnostikk som mulig. Basert på kunnskap om pollegemenes genotype kan man vurdere eggkjernens genotype.
Blastocystbiopsi – Fem dager etter egguttak har det befruktede egget normalt nådd blastocyststadiet. Ettersom en blastocyst består av 70 – 200 blastomerer, kan man med denne metoden gjøre diagnostikk på flere celler og derved få en sikrere diagnostikk (8). Etter at man har laget et hull i zona pellucida vil blastomerer som så bukter ut via hullet, kunne frigjøres fra blastocysten for preimplantatorisk genetisk diagnostikk. Ved blastocystbiopsi gjøres diagnostikken vanligvis på 3 – 10 celler.
Genetisk diagnostikk
For genetisk diagnostikk av biopsimaterialet benyttes to hovedmetoder, enten fluorescens in situ-hybridisering eller polymerasekjedereaksjon. Hvilken metode som blir brukt, avhenger av hvilken sykdom som skal analyseres.
Fluorescens in situ-hybridisering. Dette er den vanligste metoden når man har en blastomerbiopsi. Ved hjelp av in situ-hybridisering og DNA-sonder som er merket med fluorescerende farger (fluorokromer) kan man lokalisere gener og kromosomfragmenter. Ved å kombinere ulike farger kan flere kromosomer undersøkes samtidig. Dette gjøres i praksis på et objektglass ved at blastomerens cellemembran løses opp og cytoplasmaet vaskes bort slik at man får frem cellekjernen. Etter fiksering av cellekjernen tilsettes spesifikke DNA-sonder. Preparatet studeres deretter ved hjelp av fluorescensmikroskopi, hvor man vil kunne se en eller flere fargede signaler i cellekjernen, avhengig av hvilke fluorokrom som har vært benyttet.
Polymerasekjedereaksjon. Forutsetningen for bruk av denne metoden er at man har identifisert mutasjonen hos den ene eller begge foreldrene. Om DNA-sekvensen for det genet som er årsak til sykdommen er kjent, kan området som inneholder mutasjonen amplifiseres og analyseres. Dette gjøres ved at pollegemet eller blastomeren plasseres i et medium som løser opp cellen slik at DNA blir frigjort. For å utføre diagnostikken benyttes enzymet DNA-polymerase og korte DNA-fragmenter som er spesifikke for den DNA-sekvensen man ønsker å analysere. For å forhindre kontaminasjon av sædceller i rommet mellom eggets skall og membran gjøres alltid mikroinjeksjon når polymerasekjedereaksjon utføres, det vil si at en sædcelle injiseres i hvert egg.
Diskusjon
De fleste lidelsene der det er indikasjon for preimplantatorisk genetisk diagnostikk er sjeldne. Behovet for slik diagnostikk i Norge er derfor begrenset, noe som blant annet bekreftes ved at man i perioden september 2004 til januar 2007 totalt fikk inn 50 søknader om denne utredningen (1).
Preimplantatorisk genetisk diagnostikk er en høyspesialisert metode som forsatt befinner seg i en utviklingsfase. Teknisk sett har diagnostikken fortsatt flere utfordringer.
Mosaikk, det at embryoet består av både diploide og aneuploide celler, vanskeliggjør diagnostikken. Studier viser at mosaikk finnes i 25 – 60 % av alle befruktede egg, selv hos unge kvinner (9, 10). Dette kan innebære at celler som blir undersøkt er normale, mens flere av cellene som embryoet består av, og som ikke blir undersøkt, er aneuploide.
En svakhet ved polymerasekjedereaksjon er risikoen for at amplifikasjon av bare det ene genet i genparet inntreffer, noe som kan resultere i feildiagnostisering og innsetting av et affisert embryo. Dessuten er det slik at ved fluorescens in situ-hybridisering kan bare 5 – 10 av cellens kromosomer analyseres. Hittil har det også vært vanskelig å utvikle en god metode for nedfrysing og opptining av embryoer der det har vært utført preimplantatorisk genetisk diagnostikk. Når det utføres diagnostikk på ferske befruktede egg, vil man i ca. en firedel av tilfellene ikke ha noe egnet egg å sette inn i livmoren.
Siden feildiagnose ikke kan utelukkes, anbefales alle par i Sverige som har oppnådd graviditet etter preimplantatorisk genetisk diagnostikk å gjennomgå prenatal diagnostikk. Risikoen for feildiagnostikk ved genetisk undersøkelse av eggene før innsetting i livmoren ligger i dag på 5 – 10 %. Viktige faktorer for forekomsten av feildiagnostikk er spesifisitet og sensitivitet til probene man benytter i diagnostikken, hyppigheten av mosaikk/aneuploiditet i hvert enkelt tilfelle og kompetansenivået hos dem som utfører diagnostikken.
Internasjonalt er den vanligste formen for preimplantatorisk genetisk diagnostikk i dag preimplantatorisk genetisk screening, noe som skyldes at mange kvinner i høy reproduktiv alder ønsker å bli mødre og at flere klinikker bare utfører screening (11). Flere studier er blitt gjennomført for å se om preimplantatorisk genetisk screening øker sjansen for fødsel av et friskt barn. Så langt har ingen studier presentert overbevisende data som viser at dette er tilfellet (12, 13). Den hyppige anvendelsen av preimplantatorisk genetisk screening kan i stor grad tilskrives kommersielle interesser.
Mulighetene for å få utført preimplantatorisk genetisk diagnostikk har ved flere tilfeller resultert i debatt om diagnostikken er etisk forsvarlig. De etiske aspektene ligger utenfor rammen for denne artikkelen, men er blitt grundig belyst i utarbeidingen av regjeringens forslag til lovendring og i flere medisinske tidsskrifter (1, 14, 15). Den endrede bioteknologiloven legger opp til en restriktiv bruk av preimplantatorisk genetisk diagnostikk. Det betyr at diagnostikken bare blir tillatt dersom det foreligger tungtveiende medisinske indikasjoner. Har man fått innvilget søknaden om behandling, må man være mentalt innstilt på at veien frem til det endelige målet, fødsel av et friskt barn, fortsatt er lang og omstendelig.
Dersom man satser på å etablere medisinsk kompetanse i Norge, betyr det at færre norske par med anlegg for alvorlig genetisk sykdom i fremtiden behøver å reise utenlands for å få hjelp. Hvis derimot adekvat kompetanse ikke etableres, vil lovendringen innebære at norske par får tilnærmet de samme rettighetene for behandling som andre skandinaviske par, men at behandlingen fortsatt må gjennomføres i utlandet.
European Society for Human Reproduction & Embryology publiserer rapporter om utviklingen innen preimplantatorisk genetisk diagostikk (www.eshre.com). Den siste rapporten viser blant annet at risikoen for medfødte misdannelser etter preimplantatorisk genetisk diagnostikk ikke er større enn for barn født etter in vitro-fertilisering med mikroinjeksjon (11). I Sverige, som i flere andre land, finnes et nasjonalt register hvor alle barn født etter in vitro-fertilisering får en nøye oppfølging for å påvise eventuelle negative konsekvenser av behandlingen (16). Nye og sikrere metoder for preimplantatorisk genetisk diagnostikk er dessuten under utvikling, hvor man for eksempel analyserer samtlige kromosomer i cellen (17). Den endrede bioteknologiloven legger grunnlaget for at par med risiko for alvorlig arvelig sykdom hos eventuelle barn kan velge denne diagnostikken etter omfattende veiledning, utredning og nøye overveielse.
Addendum
Alle søknader om preimplantatorisk genetisk diagnostikk med vedtak i Norge finnes på nettsiden til klagenemnda (www.klagenemnda.no).
Takk til genetiker Charles Hanson, Kvinneklinikken, Sahlgrenska universitetssjukhuset for kommentarer under utarbeidingen av manuskriptet.
Oppgitte interessekonflikter: Ingen
Tabell
| Hovedbudskap |
|
- 1.
Ot.prp. nr. 26 (2006 – 07). Om lov om endringer i bioteknologiloven (preimplantasjonsdiagnostikk og forskning på overtallige befruktede egg).
- 2.
Lov 2007 – 06 – 15 nr. 31. Lov om endringer i bioteknologiloven (preimplantasjonsdiagnostikk og forskning på overtallige befruktede egg). www.lovdata.no (29.3.2007).
- 3.
Handyside AH, Kontogianni EH, Hardy K et al. Pregnancies from biopsied human preimplantation embryos sexed by Y-specific DNA amplification. Nature 1990; 344: 768 – 70.
- 4.
Ekerhovd E, Fried G, Granberg S. An ultrasound-based approach to the assessment of infertility, including the evaluation of tubal patency. Best Pract Res Clin Obstet Gynaecol 2004; 18: 13 – 28.
- 5.
Sermon K, Van Steirteghem A, Liebaers I. Preimplantation genetic diagnosis. Lancet 2004; 363: 1633 – 41.
- 6.
Ogilvie CM, Braude PR, Scriven PN. Preimplantation genetic diagnosis – an overview. J Histochem Cytochem 2005; 53: 255 – 60.
- 7.
Strom CM, Ginsberg N, Rechitsky S et al. Three births after preimplantation genetic diagnosis for cystic fibrosis with sequential first and second polar body analysis. Am J Obstet Gynecol 1998; 178: 1298 – 306.
- 8.
McArthur SJ, Leigh D, Marshall JT et al. Pregnancy and live births after trophectoderm biopsy and preimplantation genetic testing of human blastocysts. Fertil Steril 2005; 84: 1628 – 36.
- 9.
Wilton L. Preimplantation genetic diagnosis for aneuploidy screening in early human embryos: a review. Prenat Diagn 2002; 22: 512 – 8.
- 10.
Baart EB, Martini E, van den Berg I et al. Preimplantation genetic screening reveals a high incidence of aneuploidy and mosaicism in embryos from young women undergoing IVF. Hum Reprod 2006; 21: 223 – 33.
- 11.
Sermon KD, Michiels A, Harton G et al. ESHRE PGD Consortium data collection VI: cycles from January to December 2003 with pregnancy follow-up to October 2004. Hum Reprod 2007; 22: 323 – 33.
- 12.
Shahine LK, Cedars M. Preimplantation genetic diagnosis does not increase pregnancy rates in patients at risk for aneuploidy. Fertil Steril 2006; 85: 51 – 6.
- 13.
Donoso P, Staessen C, Fauser BCJM et al. Current value of preimplantation genetic aneuploidy screening in IVF. Hum Reprod Update 2007; 13: 12 – 25.
- 14.
Klipstein S. Preimplantation genetic diagnosis: technological promise and ethical perils. Fertil Steril 2005; 83: 1347 – 53.
- 15.
Ethics, law and moral philosophy of reproductive biomedicine. Papers from an international conference at the Royal Society. September 30 – October 1, 2004. London, United Kingdom. Reprod Biomed Online 2005, 10 (suppl 1): 1 – 147.
- 16.
Bergh T, Hillensjö T, Nygren K-G et al. Deliveries and children born after in-vitro fertilisation in Sweden 1982 – 95: a retrospective cohort study. Lancet 1999; 354: 1579 – 85.
- 17.
Wilton L. Preimplantation genetic diagnosis and chromosome analysis of blastomeres using comparative genomic hybridization. Hum Reprod Update 2005; 11: 33 – 41.