Background.
The treatment of malignant intracranial tumours varies internationally. In our institution the treatment has been based on surgery. Adjuvant therapy has been tailored to the needs of the patient. The objective of this retrospective study was to analyse the prognostic effect of surgery and adjuvant therapy.
Material and methods.
186 patients treated in a single institution over a period of 6.5 years were included in the study. 172 were operated. Clinical information was obtained from the medical records. Survival analysis was performed using the Kaplan-Meier model.
Results.
Analysis suggests that the most important factors related to survival were repeated resection, Karnofsky Performance Score, extent of resection, and age. Patients with glioblastoma multiforme showed ten months prolonged survival after repeated resection. Our results suggest that irradiation in combination with chemotherapy is the best strategy of adjuvant therapy for glioblastoma multiforme and anaplastic astrocytoma. Patients with tumours located centrally near the skull base had a higher complication rate and a significantly reduced neurological outcome.
Behandling av hjernesvulster er omdiskutert og valg av behandlingsstrategi varierer sterkt. Ved Nevrokirurgisk avdeling, St. Olavs Hospital i Trondheim har man basert seg på kirurgi som primærbehandling ved de fleste typer maligne intrakraniale svulster, med påfølgende adjuvant behandling hvor dette er indisert.
I denne retrospektive studien gis en uselektert oversikt over alle pasientene som ble behandlet for malign intrakranial svulst ved vår avdeling over en periode på 6,5 år.
Materiale og metode
Pasientpopulasjon
Alle pasienter over 15 år registrert med diagnosen malign hjernesvulst (inkludert maligne og atypiske meningiomer) ved St. Olavs Hospital i perioden 1.1. 1995 – 1.7. 2001 ble kartlagt sammen med pasienter som ble reoperert i samme tidsrom. Fem pasienter ble ekskludert pga. manglende journalmateriale. 186 pasienter (91 kvinner og 95 menn) i alderen 16 – 87 år (gjennomsnittsalder 52 år) ble inkludert.
Metode
Journalene er gjennomgått retrospektivt, og data angående kjønn, alder, histologi, operasjonstidspunkt for primær- og sekundærtumor samt eventuell dødsdato ble registrert. Operasjonstidspunkt for primærtumor ble definert som starttidspunkt for overlevelse. Videre ble tumors lokalisering, reseksjonsgrad, eventuell nevronavigasjon, operasjonens varighet, operatør, dominerende symptomer, nevrologisk gradering, eventuell adjuvant behandling, komplikasjoner og komorbiditet registrert. Nevrologisk gradering ble vurdert med Karnofskys indeks for gradering av pasientens funksjonstilstand (KPS) basert på journalmaterialet (tab 1). Denne ble vurdert preoperativt og ved første polikliniske kontroll (vanligvis etter omtrent en måned). Pasienter med KPS-skåre på 80, 90 eller 100 ble vurdert som uavhengige av hjelp i dagliglivet. Ved KPS-skåre på 60 og 70 ble pasientene vurdert som delvis avhengige, og med KPS-skåre under 60 helt avhengige av hjelp i dagliglivet. Reseksjonsgrad ble bedømt ut fra operasjonsbeskrivelsen, hvor kirurgen har benyttet faglig skjønn, peroperativ ultralyd samt histologisvar (WHO-klassifikasjon) (1) som grunnlag for sin vurdering. Total reseksjon ble definert som fri reseksjonsrand bedømt peroperativt, understøttet med histologi (mikroskopisk radikalitet). Subtotal reseksjon ble definert som operasjonskavitet vurdert subjektivt fri for tumorvev, men ikke bekreftet med histologisk prøve (makroskopisk radikalitet). Ved partiell reseksjon var det sikkert resterende tumorvev.
Tabell 1
Karnofskys indeks for gradering av pasientens funksjonstilstand (KPS)
| Skåre |
Beskrivelse |
| 100 |
Normal, ingen plager eller subjektive tegn på sykdom |
| 90 |
Klarer normal aktivitet, sykdommen gir lite symptomer |
| 80 |
Klarer til nød normal aktivitet. Sykdommen gir en del symptomer |
| 70 |
Klarer seg selv, ute av stand til normal aktivitet eller aktivt arbeid |
| 60 |
Trenger noe assistanse, men klarer stort sett å tilfredsstille egne behov |
| 50 |
Trenger betydelig hjelp og stadig medisinsk omsorg |
| 40 |
Ufør, trenger spesiell hjelp og omsorg |
| 30 |
Helt ufør, hospitalisering nødvendig, men faren for død er ikke overhengende |
| 20 |
Svært syk, hospitalisering og understøttende behandling nødvendig |
| 10 |
Moribund, dødsprosessen er i rask fremmarsj |
| 0 |
Død |
Statistisk behandling
Overlevelsesanalyser ble gjort med Kaplan-Meier-modellen. Overlevelseskurver for de forskjellige subgruppene ble sammenliknet med logranktesten. Alle resultatene er testet med Mann-Whitneys U-test. Dersom en av gruppene hadde overvekt av en eller flere prognostiske faktorer, ble det korrigert for disse, for i størst mulig grad å unngå seleksjonsskjevhet. Alle p-verdier under 5 % ble betraktet som signifikante.
Resultater
Generelt
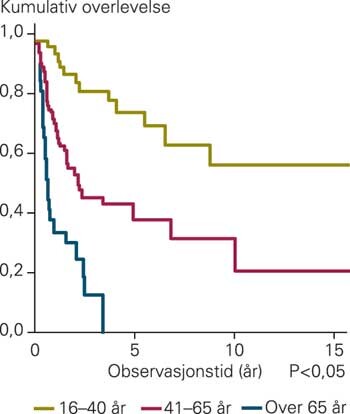
Det ble registrert 15 forskjellige typer hjernesvulster, hvorav glioblastom og metastaser var de vanligste. Median overlevelse ved de forskjellige svulsene er vist i tabell 2. 172 av de 186 pasientene ble operert. Gjennomsnittlig alder på operasjonstidspunktet (primæroperasjon) var 50 år. Overlevelse etter primæroperasjon sank med økende alder fra fylte 30 år (p < 0,05) i totalmaterialet (fig 1). Det var ingen signifikant forskjell i insidens for kvinner eller menn i totalmaterialet. Imidlertid er det en overrepresentasjon av menn med diagnosen glioblastom (p < 0,001), i forholdet 3 : 2. Vi fant ingen signifikante kjønnsforskjeller i overlevelse ved de forskjellige hjernesvulstene. De vanligste debutsymptomene på malign hjernesvulst var epilepsi/kramper (n = 47), trykksymptomer (hodepine, kvalme, oppkast) (n = 47) og svimmelhet/ustøhet (n = 21). Halvparten av pasientene var fortsatt i live etter seks og et halvt år.
Tabell 2
Antall pasienter og median overlevelse ved de forskjellige typer hjernesvulster i studien, samt median overlevelse i andre studier hvor sammenliknbare data er tilgjengelig
| Overlevelse i måneder(Kaplan-Meier) |
Overlevelse i månederi andre studier (litteraturreferanse i parentes) |
|||
| Antall |
Median |
Median |
||
| Glioblastom |
53 |
10,4 |
10,6 (10) |
|
| Metastase(r) |
25 |
7,6 |
8,9 (23) |
|
| Oligodendrogliom |
20 |
134 |
74 (22) |
|
| Anaplastisk astrocytom |
18 |
29,4 |
36 (2) |
|
| Astrocytom grad 2 |
17 |
143 (gjennomsnitt) |
60 (2) |
|
| Astrocytom grad 1 |
8 |
– |
– |
|
| Blandingsgliom |
8 |
118 |
65 (22) |
|
| Meningiom |
5 |
57,2 |
– |
|
| Ependymom |
4 |
– |
– |
|
| Hemangioblastom |
4 |
– |
– |
|
| Gangliogliom |
3 |
– |
– |
|
| Pineocytom |
2 |
– |
– |
|
| Nevrocytom |
1 |
(73,1) |
– |
|
| Lymfom |
1 |
(1,3) |
– |
|
| Annen tumor |
1 |
– |
– |
|
| Ikke-konklusiv |
6 |
49,9 |
– |
Gjentatte operasjoner
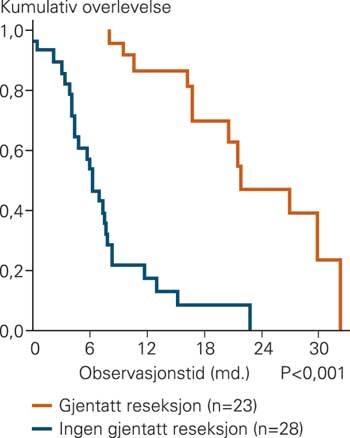
69 av de primæropererte pasientene gjennomgikk en eller flere reoperasjoner for klinisk og radiologisk påvist residiv. For glioblastom fant vi signifikant bedret overlevelse for pasienter som hadde gjennomgått en eller flere reoperasjoner, sammenliknet med pasienter som kun hadde gjennomgått primæroperasjon (p < 0,001) (fig 2). Det var imidlertid ingen signifikant sammenheng mellom overlevelse og antall reoperasjoner utover én.
I det resterende materialet (unntatt glioblastom) fant vi også signifikant bedret overlevelse ved reoperasjon (p = 0,04). Materialet var imidlertid ikke stort nok til å påvise hvilke av disse pasientene som profitterte på reoperasjon.
Reseksjonsgrad
Det forelå en signifikant bedret overlevelse hos pasienter hvor det var blitt foretatt total reseksjon i forhold til pasienter med partiell reseksjon (p = 0,03). Vi fant ingen signifikant forskjell med hensyn til overlevelse mellom de andre graderingene av reseksjon. Ved glioblastom var median overlevelse forlenget med ti måneder i gruppen hvor det ble foretatt subtotal reseksjon i forhold til partiell.
Adjuvant behandling
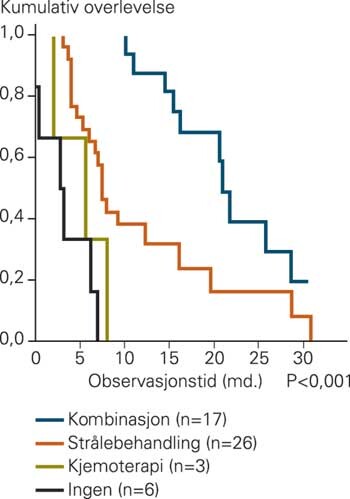
Tre av fire opererte pasienter fikk adjuvant behandling i form av strålebehandling, cytostatika eller begge deler. For glioblastomer fant vi en signifikant bedret overlevelse for pasienter som hadde mottatt adjuvant behandling (p < 0,001). Strålebehandling i tillegg til cytostatikabehandling gav en bedre overlevelse enn strålebehandling eller cytostatikabehandling alene (fig 3). Vi fant ikke forlenget overlevelse etter adjuvant behandling hos pasienter med andre histologiske diagnoser, men pasientgrunnlaget i mange av disse gruppene er lite.
Nevrologisk resultat
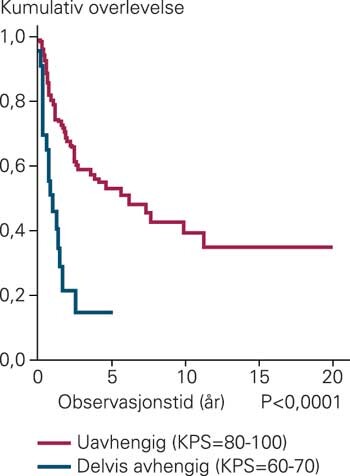
78 % av pasientene ble definert som funksjonsmessig uavhengige ved den preoperative vurderingen, 13 % som delvis avhengige og 9 % som avhengige. Ved første polikliniske kontroll (eller postoperativt, i tilfeller hvor pasienten døde før poliklinisk kontroll) ble 81 % definert som uavhengige, 12 % som delvis avhengige og 7 % som avhengige. Pasienter med preoperativ KPS-skåre 80 – 100 hadde en signifikant bedret overlevelse sammenliknet med pasienter med lavere skåre (fig 4). Pasienter som preoperativt ble definert som avhengige, hadde et bedre relativt behandlingsresultat (differanse mellom KPS-skåre vurdert ved første polikliniske kontroll og KPS-skåre preoperativt) enn pasienter med høyere KPS-skåre (p < 0,0001).
Tumors beliggenhet
Det ble ikke registrert noen signifikant forskjell i overlevelse i forhold til lokalisering av svulsten. Imidlertid fant vi et signifikant dårligere nevrologisk behandlingsresultat for pasienter med svulsten lokalisert dypt sentralt (p < 0,01). Disse pasientene skåret gjennomsnittlig 16 poeng dårligere på KPS-indeksen ved første polikliniske kontroll i forhold til preoperativ KPS-vurdering (gjennomsnitt i hele materialet er 2 poeng).
Operasjonskomplikasjoner
En tredel fikk per- eller postoperative komplikasjoner. De vanligste komplikasjonene var hemiparese (n = 11), afasi (n = 8), blødning (n = 7), hydrocephalus (n = 5) og epilepsi (n = 5). Hvor stor andel av komplikasjonene som gav permanente sekveler, er ikke registrert. Den faktoren som viste sterkest korrelasjon med komplikasjonsraten, var en dypt sentralt lokalisert tumor (p = 0,04).
Diskusjon
Kirurgi er den eldste og mest utbredte primærbehandling av intrakraniale svulster (2, 3). Det er imidlertid reist spørsmål om dette er den riktige behandlingen for alle pasientene (4). Ved vår institusjon ble nesten alle pasientene med malign hjernesvulst behandlet kirurgisk, selv de med dypt sentralt/basisnært beliggende svulst. Det er imidlertid ikke tilstrekkelig antall pasienter i den siste kategorien til å si noe om man vinner levedager med slik kirurgi. Vi fant at disse fikk et dårligere nevrologisk behandlingsresultat, noe som reiser spørsmål om man heller bør rette søkelyset mot adjuvant og konservativ behandling hos disse pasientene.
Gjentatte operasjoner
For glioblastomer tyder våre resultater på at verdien av reoperasjon er spesielt stor, noe som også er vist i andre studier (2, 3, 5, 6). Forlenget median overlevelse i andre studier er seks måneder (3). Seleksjonsskjevhet påvirker uunngåelig disse resultatene dersom det ikke korrigeres for forstyrrende faktorer. Reoperasjon er ikke aktuelt for alle pasientene. I vårt materiale hadde pasienter som ikke ble reoperert en signifikant lavere KPS-skåre ved første polikliniske kontroll, samt en signifikant høyere komplikasjonsrate enn øvrige pasienter. I tillegg hadde de en signifikant høyere alder (sju år) og færre i denne gruppen fikk adjuvant behandling. Når vi korrigerte for alder, postoperativ KPS-skåre, komplikasjoner og adjuvant behandling, hadde glioblastompasienter som hadde gjennomgått gjentatt operasjon, en forlenget median overlevelse på ti måneder (95 % KI 9,6 – 10,3 md., p < 0,001) i vår studie.
Reseksjonsgrad
Maligne hjernesvulster, som anaplastiske astrocytomer og glioblastomer, er vanligvis dårlig avgrenset til normalvevet. Det er derfor ofte ikke mulig å radikaloperere disse svulstene. Resultatet blir et kompromiss mellom høyest mulig grad av radikalitet og antatt bevart nevrologisk funksjon. Funksjonell MR kan gi nyttig informasjon ved denne vurderingen, særlig i tilfeller hvor tumor ligger nær antatt viktige områder for språk, syn og kognisjon. Kraniotomi med våken pasient har også vist seg å være en lovende metode i dette henseende (7). Vår studie tyder på at man bør tilstrebe en mest mulig radikal reseksjon, som kan gi forlenget overlevelse og et godt nevrologisk resultat, selv om litteraturen ikke er entydig på dette feltet (8) – (10).
Adjuvant behandling
Adjuvant strålebehandling ble brukt i stor utstrekning ved både høygradige og lavgradige svulster i vårt materiale. Normalt stråleregime ved vår institusjon består av en total bestråling på 54 Gy, fordelt på 30 behandlinger à 1,8 Gy. Tilsvarende regime, med visse variasjoner, brukes verden over og er vist å gi forlenget overlevelse ved høygradige tumorer (2, 11). Strålebehandling til pasienter over 80 år og pasienter med dårlig nevrologisk status anbefales ikke (12). Når det gjelder lavgradige tumorer er imidlertid strålebehandlingens rolle uklar, både med hensyn til effekt, bivirkninger og tidspunkt for oppstart av behandling (13, 14). I vårt materiale kunne vi påvise bedret overlevelse ved bruk av adjuvant strålebehandling, men signifikant effekt på overlevelse ble kun vist ved glioblastomer.
Bruk av kjemoterapi har vært kontroversielt (2, 15), men blir gitt rutinemessig hos en stor andel av pasientene. Vi har gitt en kombinasjonsbehandling med prokarbasin, lomustin og vinkristin (PCV-kur). Nyere store studier viser nå i større grad forlenget overlevelse etter adjuvant kjemoterapi ved maligne hjernesvulster (16). Oligodendrogliomer er rapportert å være spesielt følsomme for kjemoterapi (17). Vi kunne ikke påvise noen effekt av kjemoterapi alene som adjuvant behandling, men kombinert med strålebehandling gav behandlingen et signifikant bidrag til overlevelsen for glioblastom. Med det relativt lave antall pasienter i de andre undergruppene var det ikke mulig å oppnå signifikante verdier hva angikk adjuvant behandling.
Nevrologisk resultat
Vi fant at preoperativ KPS-skåre var en god prediktor for overlevelse, noe som også er rapportert tidligere (7, 18, 19). En skåre på 80 eller høyere (uavhengig) er i seg selv en god prognostisk faktor. Det var også signifikant forskjell i overlevelse mellom pasienter med KPS-skåre på henholdsvis 90 og 80 i totalmaterialet.
Kjønn
Menn er overrepresentert blant pasienter med glioblastom (20, 21). Årsaken er ukjent, men det ser ut til at kvinnelige kjønnshormoner kan ha en beskyttende effekt på utvikling av maligne gliomer (21).
Operasjonskomplikasjoner
Inngrep hvor tumor var lokalisert dypt i cerebrum, hadde en høyere komplikasjonsrate enn andre inngrep. En slik lokalisasjon vanskeliggjør tilgangen til tumor og innebærer at man må lage tunneler gjennom relativt store hjerneandeler med høy funksjonell aktivitet.
De viktigste prognostiske faktorene var:
Gjentatt reseksjon ved residiv
Alder
Nevrologisk status
Reseksjonsgrad
Interessekonflikt
Studien er støttet ved et sommerstipend fra Den Norske Kreftforening.
Interessekonflikter, se til slutt i artikkelen.
Basert på en prosjektoppgave i medisinstudiet ved Norges teknisk-naturvitenskapelige universitet (24).
- 1.
Kleihues P, Cavenee WK, red. Pathology & genetics of tumours of the nervous system. WHO classification of tumours. Lyon: IARC Press, 2000.
- 2.
DeAngelis LM. Brain tumors. N Engl J Med 2001; 344: 114 – 23.
- 3.
Obwegeser A, Ortler M, Seiwald M, Ulmer H, Kostron H. Therapy of glioblastoma multiforme: a cumulative experience of 10 years. Acta Neurochir (Wien) 1995; 137: 29 – 33.
- 4.
Kreth FW, Berlis A, Spiropoulou V, Faist M, Scheremet R, Rossner R et al. The role of tumor resection in the treatment of glioblastoma multiforme in adults. Cancer 1999; 86: 2117 – 23.
- 5.
Azizi A, Black P, Miyamoto C, Croul SE. Treatment of malignant astrocytomas with repetitive resections: a longitudinal study. Isr Med Assoc J 2001; 3: 254 – 7.
- 6.
Daneyemez M, Gezen F, Canakci Z, Kahraman S. Radical surgery and reoperation in supratentorial malignant glial tumors. Minim Invasive Neurosurg 1998; 4: 209 – 13.
- 7.
Taylor MD, Bernstein M. Awake craniotomy with brain mapping as the routine surgical approach to treating patients with supratentorial intraaxial tumors: a prospective trial of 200 cases. J Neurosurg 1999; 90: 35 – 41.
- 8.
Hess KR. Extent of resection as a prognostic variable in the treatment of gliomas. J Neurooncol 1999; 42: 227 – 31.
- 9.
Kowalczuk A, Macdonald RL, Amidei C, Dohrmann G 3rd, Erickson RK, Hekmatpanah J et al. Quantitative imaging study of extent of surgical resection and prognosis of malignant astrocytomas. Neurosurgery 1997; 41: 1028 – 36.
- 10.
Lacroix M, Abi-Said D, Fourney DR, Gokaslan ZL, Shi W, DeMonte F et al. A multivariate analysis of 416 patients with glioblastoma multiforme: prognosis, extent of resection and survival. J Neurosurg 2001; 95: 190 – 8.
- 11.
Kondziolka D, Flickinger JC, Bissonette DJ, Bozik M, Lunsford LD. Survival benefit of stereotactic radiosurgery for patients with malignant glial neoplasms. Neurosurgery 1997; 41: 776 – 83.
- 12.
Meckling S, Dold O, Forsyth PA, Brasher P, Hagen NA. Malignant supratentorial glioma in the elderly: is radiotherapy useful? Neurology 1996; 47: 901 – 5.
- 13.
Peterson K, DeAngelis LM. Weighing the benefits and risks of radiation therapy for low-grade glioma. Neurology 2001; 56: 1255 – 6.
- 14.
Surma-aho O, Niemela M, Vilkki J, Kouri M, Brander A, Salonen O et al. Adverse long-term effects of brain radiotherapy in adult low-grade glioma patients. Neurology 2001; 56: 1285 – 90.
- 15.
Kornblith PL, Walker M. Chemotherapy for malignant gliomas. J Neurosurg 1988; 68: 1 – 17.
- 16.
DeAngelis LM, Burger PC, Green SB, Cairncross JG. Malignant glioma: who benefits from adjuvant chemotherapy? Ann Neurol 1998; 44: 691 – 5.
- 17.
Hofer S, Herrmann R. Chemotherapy for malignant brain tumors of astrocytic and oligodendroglial lineage. J Cancer Res Clin Oncol 2001; 127: 91 – 5.
- 18.
Bauman G, Lote K, Larson D, Stalpers L, Leighton C, Fisher B et al. Pretreatment factors predict overall survival for patients with low-grade glioma: a recursive partitioning analysis. Int J Radiat Oncol Biol Phys 1999; 45: 923 – 9.
- 19.
Nakamura M, Konishi N, Tsunoda S, Nakase H, Tsuzuki T, Aoki H et al. Analysis of prognostic and survival factors related to treatment of low-grade astrocytomas in adults. Oncology 2000; 58: 108 – 16.
- 20.
Fleury A, Menegoz F, Grosclaude P, Daures JP, Henry-Amar M, Raverdy N et al. Descriptive epidemiology of cerebral gliomas in France. Cancer 1997; 79: 1195 – 202.
- 21.
McKinley BP, Michalek AM, Fenstermaker RA, Plunkett RJ. The impact of age and sex on the incidence of glial tumors in New York state from 1976 to 1995. J Neurosurg 2000; 93: 932 – 9.
- 22.
Lote K, Gundersen S, Hannisdal E, Hager B, Stenwig AE, Tvera K et al. Prognosen ved primære svulster i sentralnervesystemet. Tidsskr Nor Lægeforen 1996; 116: 1320 – 4.
- 23.
Lagerwaard FJ, Levendag PC, Nowak PJ, Eijkenboom WM, Hanssens PE, Schmitz PI. Identification of prognostic factors in patients with brain metastases: a review of 1292 patients. Int J Radiat Oncol Biol Phys 1999; 43: 795 – 803.
- 24.
Ianssen T, Juul R. Maligne intrakranielle hjernesvulster – hvordan går det med pasientene? Trondheim: Norges teknisk-naturvitenskapelige universitet, 2001.