I 1965 publiserte den amerikanske barnelegen Gunnar Stickler og medarbeidere en rapport om en familie i fem generasjoner med et syndrombilde han kalte arvelig progredierende artro-oftalmopati (1). Tilstanden var kjennetegnet av okulære og orofaciale anomalier, skjelettanomalier samt nedsatt hørsel, og betegnes i dag som Sticklers syndrom. I USA er den estimerte prevalensen 1 : 10 000, og Sticklers syndrom antas å være den vanligst forekommende autosomalt dominant arvelige bindevevssykdom (2 – 5).
Hensikten med vår artikkel er å presentere en pasient med Sticklers syndrom og gi en oversikt over tilstanden med bakgrunn i nyere kunnskap fra kliniske og molekylærgenetiske studier.
Pasienten. Første barn av friske, ubeslektede foreldre. Det var normalt svangerskap og fødsel. Umiddelbart etter fødsel ble det bemerket at barnet hadde Pierre Robins sekvens (triaden mikrognati, U-formet bakre ganespalte og glossoptose) samt bilateral exophthalmus (fig 1). Øyeundersøkelse i nyfødtperioden viste bilateral høygradig myopi ( − 14,5 D). Det ble konkludert med at barnet hadde Sticklers syndrom. Ved senere gjennomgang av familieanamnesen fant man en opphopning av leddplager, myopi og mandibulahypoplasi på morssiden. Ganespalten ble lukket da piken var ett år gammel, ny ganespalteplastikk da hun var fem. Hun har trengt drenbehandling grunnet serøs otitt, og hørselsutredning har vist et lettgradig konduktivt hørselstap i bassområdet. Pasienten har nasal tale og uttaleproblemer. Den mentale utvikling har vært normal. Da hun var tre år, fikk hun leddsmerter, og man fant hypermobile ledd. Øyeundersøkelse har vist typiske forandringer i corpus vitreum, forenlig med Sticklers syndrom type 1. I netthinnen er det påvist utbredte degenerative forandringer, men ingen rifter. Genetisk utredning utført i 1997 kunne ikke påvise mutasjoner i COL2A1- eller COL11A1-genene, men heller ikke med 100 % sikkerhet utelukke dette.
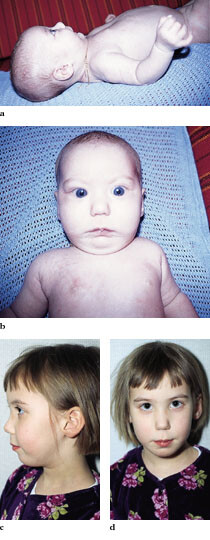
Okulære funn
Forandringer i corpus vitreum er nærmest patognomonisk ved Sticklers syndrom og gir opphav til fenotypisk inndeling i type 1 og type 2 (6 – 8). Ved type 1 sees retrolentalt et rudimentært corpus vitreum med en karakteristisk foldet corpusmembran. Bak denne membranen er corpus vitreum degenerert og tyntflytende, og corpuskaviteten oppfattes som optisk tom (6, 8, 9). Type 2 er karakterisert av kondenserte kollagenfibriller med perleformede ujevnheter som strekker seg gjennom corpus. Type 1 og type 2 korrelerer med mutasjoner i genene COL2A1 og COL11A1 (tab 1) (6 – 8, 10 – 12).
De fleste pasientene har en høygradig, vanligvis kongenitt myopi (1, 4, 6). Myopien skyldes lang øyeakse og kan hos nyfødte gi opphav til pseudoexophthalmus. Utbredte degenerative vitreoretinale forandringer er vanlig. Disse forandringene disponerer for danning av rifter i netthinnen, noe som igjen kan medføre netthinneløsning, den mest fryktede komplikasjon ved Sticklers syndrom (6). Opptil 50 % av pasientene får netthinneløsning, og opptil 40 % av disse oppstår bilateralt (6, 13). Netthinneløsning hos foreldre øker risikoen hos barna (4). Sticklers syndrom er den vanligste årsak til arvelig netthinneløsning hos barn, men dette oppstår oftest først i tenårene eller tidlig voksen alder (4). Tidligere var risikoen for blindhet meget høy. Med moderne vitreoretinal kirurgi er prognosen bedre (6). Enkelte anbefaler profylaktisk laserbehandling av degenerative netthinneforandringer, men dette er omdiskutert (13). Alvorlig vitreoretinal patologi forekommer langt sjeldnere ved Sticklers syndrom type 2 (11, 14).
Andre okulære funn er også vanlig ved Sticklers syndrom. Katarakt er ofte kongenitt, med karakteristiske kile- eller flekkformede fordunklinger i linsecortex (15). Glaukom kan oppstå på grunn av misdannelser i kammervinkelen eller sekundært til kronisk netthinneløsning (5, 6).
Okulære funn ble tidligere betraktet som en forutsetning for diagnosen. Imidlertid er det nå rapportert om familier uten øyeaffeksjon, men med de øvrige systemiske manifestasjoner man finner ved Sticklers syndrom. Denne tilstanden betegnes i dag som Sticklers syndrom type 3 eller ikke-okulært Sticklers syndrom (3, 10, 14, 16).
Orofaciale trekk
Pasienter med Sticklers syndrom har ofte et flatt hypoplastisk midtansikt, innsunket og bred neserot, oppadvendte nesebor og liten hake. Disse trekkene er tydeligst i spedbarnsalderen og blir mindre påfallende etter hvert som barnet blir eldre (fig 1) (6, 17). Det er stor variasjon i ansiktstrekkene, og isolert kan disse ikke brukes til å stille diagnosen (6).
Opptil 20 – 25 % av pasientene vil ha en bakre ganespalte, vanligst er dette hos pasienter med mutasjoner i COL2A1. Grad av alvorlighet kan variere fra en subklinisk bifid uvula til fullt utviklet Pierre Robins sekvens (4, 6, 18, 19). Sticklers syndrom er den hyppigste syndromale årsak til dette (14). I en serie på 90 pasienter med Pierre Robins sekvens hadde hele 32 Sticklers syndrom. Alvorlig luftveisobstruksjon forekom sjelden (18).
Hørsel
Nedsatt hørsel har to årsaker. En bakre ganespalte disponerer for kronisk serøs otitt, som igjen kan forårsake et konduktivt hørselstap. En del pasienter har også et sensorinevralt hørselstap (6, 20). Patogenesen for dette er ukjent, men det spekuleres i om enten endringer i pigmentert epitel eller kollagenforandringer i det indre øret kan være en årsak (4, 6).
Det synes å være fenotypiske forskjeller mellom pasienter med COL2A1-mutasjoner og pasienter med mutasjoner i COL11A1 eller COL11A2. Ved de to sistnevnte mutasjoner (Sticklers syndrom type 2 og type 3) finner man i langt høyere grad tidlig debut av et mildt til moderat hørselstap, hovedsakelig i det høyfrekvente området (4, 6, 8, 11). Ved Sticklers syndrom type 1 har også en høy andel av pasientene et høyfrekvent, men oftest lettgradig hørselstap, som først oppdages i voksen alder (6, 11).
Skjelett- og leddsymptomer
Pasienter med Sticklers syndrom har gjerne en marfanoid habitus med slanke ekstremiteter og lange fingrer, men lengdetilveksten og slutthøyden vil være innenfor normalområdet (2, 6, 17). Yngre pasienter har ofte hypermobile ledd (1, 4, 6, 17). Med økende alder avtar hypermobiliteten og andre symptomer fra skjelettsystemet kan overta (6). Hos skolebarn med hoftesmerter er det påvist skjelettforandringer som coxa valga, breddeforøket lårhals og protrusio acetabuli. Disse forandringene disponerer for utvikling av hofteleddsartrose. Femurosteotomi med varisering og rotasjon kan i slike tilfeller være indisert (2). Ved etablert artrose i voksen alder vil hofteleddsprotese være aktuelt (6). Valgusstilling i kneledd eller ustabile ankelledd, sammen med sykdomsspesifikke forandringer i leddbruskens kollagen, kan forklare utvikling av artrose i disse leddene allerede i tidlig voksen alder (2, 17). En rekke andre symptomer og radiologiske forandringer i skjelettsystemet er også beskrevet (17, 19).
Andre manifestasjoner og differensialdiagnoser
Pasientene har i de aller fleste tilfeller normal intelligens, men alvorlig hypoksi etter fødselen i forbindelse med Pierre Robins sekvens kan en sjelden gang gi hjerneskade (21). Forsinket språkutvikling kan oppstå ved nedsatt hørsel (4).
Mitralklaffprolaps har tidligere vært rapportert. I en nyere serie med over hundre pasienter som alle ble grundig undersøkt med ekkokardiografi, fant man imidlertid ingen tilfeller av mitralklaffprolaps (6, 22).
Tidligere var det en viss forvirring når det gjaldt avgrensning mot Wagners syndrom (MIM 143200). I dag regnes disse tilstandene som to separate kliniske entiteter (6, 7). Avgrensning mot Marshalls syndrom (MIM 154780) er fortsatt uavklart (6).
Patofysiologi og molekylær genetikk
Sticklers syndrom er autosomalt dominant arvelig med høy penetrans, men svært variabel ekspressivitet (1, 6, 17). Dette er et vanlig fenomen ved bindevevssykdommer med dominant arvegang (17). Variabilitet i klinisk presentasjon innen familier er vanlig, men i langt mindre grad enn interfamiliær variabilitet (23). Tilstanden skyldes en defekt i kollagensyntesen. Det er hittil identifisert 19 forskjellige kollagentyper, som hver er en trimerkombinasjon bestående av tre prokollagen polypeptid α -kjeder foldet i en trippel heliksstruktur (tab 1) (4, 6, 16).
Majoriteten av pasientene (50 – 75 %) har den karakteristiske vitreale fenotypen, forenlig med Sticklers syndrom type 1 (3, 6, 8). Denne fenotypen er sterkt assosiert med stoppmutasjoner i genet COL2A1 (6, 7, 8, 11). Dette medfører affeksjon av type II- og type XI-kollagen. Type II-kollagen er det viktigste kollagenet i brusk, corpus vitreum og nucleus pulposus, men finnes også i det indre øret (6, 7, 11, 14). Type XI-kollagen har en liknende vevsdistribusjon som type II, men utgjør kvantitativt en mindre andel (6, 7, 11, 12, 14, 16). Tabell 1 gir en oversikt over påviste genmutasjoner ved Sticklers syndrom, deres genprodukter og sammenhengen med øyeaffeksjon. Mutasjoner i COL11A2, som kun er rapportert ved Sticklers syndrom type 3, medfører endringer i α 2(XI)-kjeden. I corpus vitreum er imidlertid denne α -kjeden byttet ut med en α 2(V)-kjede, og dette forklarer manglende øyeaffeksjon (3, 7, 11, 14, 16).
Tabell 1
Sticklers syndrom, genetikk og øyeaffeksjon
| Type 1 |
Type 2 |
Type 3 |
|
| MIM¹ (10) |
108300 |
604841 |
184840 |
| Kromosomlokalisering |
12q13 |
1p21 |
6p21.3 |
| Mutert gen |
COL2A1 |
COL11A1 |
COL11A2 |
| Endret genprodukt (prokollagenkjede) |
α 1(II) og α 3(XI)² |
α 1(XI) |
α 2(XI) |
| Kollagentype affisert |
Type II-kollagen (en homotrimer av tre α 1(II)-kjeder) og type XI-kollagen |
Type XI-kollagen (en heterotrimer av α 1(XI), α 2(XI) og α 3(XI)-kjeder) |
Type XI-kollagen |
| Øyeaffeksjon |
Membranøs vitreal fenotype Netthinneløsning vanlig |
Perleformet vitreal fenotype Sjeldnere netthinneløsning |
Ingen |
| |||
I flere familier med klassisk Sticklers syndrom har man verken påvist kobling til kollagen type II- eller til type XI-genene. Dette taler for at det foreligger ytterligere minst ett gen som er assosiert med tilstanden (6, 10, 24).
Diagnostikk, oppfølging og genetisk veiledning
Molekylærgenetisk diagnostikk har til nå vært utført på forskningsbasis og er komplisert på grunn av kollagengenenes størrelse og kompleksitet og det store antall gener som er aktuelle for undersøkelse (6). En hurtig PCR-basert screening av noen av de vanligste mutasjonsstedene på COL2A1 er i dag utviklet (25), men fortsatt stilles diagnosen ut fra kliniske kriterier (6) (tab 2). Ved følgende tilstander må Sticklers syndrom alltid overveies som mulig diagnose (6):
Tabell 2
Foreslåtte diagnostiske kriterier for Sticklers syndrom type 1 og type 2 (6, 8)
| Medfødte karakteristiske forandringer i corpus vitreum og minst tre av følgende fem tilstander: |
|
– Alle nyfødte med Pierre Robins sekvens eller bakre ganespalte
– Alle pasienter med høygradig myopi og/eller netthinneløsning som er assosiert med hypermobile ledd, andre skjelettsymptomer, ganespalte eller nedsatt hørsel
– Hos pasienter med netthinneløsning i ung alder, spesielt ved positiv familieanamnese på samme tilstand
En grundig oftalmologisk undersøkelse, inkludert spaltelampeundersøkelse, vil i de fleste tilfeller være nødvendig og tilstrekkelig for å stille diagnosen, men en liten gruppe pasienter har ikke øyeaffeksjon (6, 8). Mange pasienter har kun lettere symptomer og diagnostiseres først når et alvorligere affisert familiemedlem får diagnosen (4, 17). Når diagnosen er stilt, er det viktig med koordinert tverrfaglig utredning og oppfølging (tab 3).
Tabell 3
Tverrfaglig oppfølging av pasienter med Sticklers syndrom (3, 4, 6)
| Øyelege og ev. synspedagog |
|
| Øre-nese-hals-lege og audiolog |
|
| Ortoped og fysioterapeut |
|
| Barnelege, pedagog og logoped |
|
Familier med Sticklers syndrom skal tilbys genetisk veiledning, men dette er komplisert pga. den store kliniske variabilitet man ser hos affiserte pasienter også innad i familier (6, 23, 26). Ett tilfelle av prenatal diagnostikk basert på morkakeprøver i første trimester er rapportert i en amerikansk familie med tre affiserte søsken og en kjent mutasjon i COL2A1 (26). I andre trimester kan man ved ultralydundersøkelse av fosteret påvise eventuell mikrognati og ganespalte (6, 26).
Konklusjon
Sticklers syndrom forekommer relativt sjelden, men hvis prevalensen er tilsvarende den man finner i Nord-Amerika, vil det i Norge årlig fødes ca. 5 – 6 barn med dette syndromet. Vi har ingen gode tall på insidens eller prevalens i Norge. Vårt inntrykk er at tilstanden er relativt ukjent, og vi spekulerer derfor på om en del pasienter ennå ikke er diagnostisert (2, 4). Kunnskap om sammenhengen mellom symptomer fra syn, hørsel og skjelettsystem er viktig for å kunne diagnostisere og gi best mulig oppfølging til denne gruppe pasienter.
Addendum
Det eksisterer ingen støtteforening for pasienter med Sticklers syndrom i Norge i dag. Informasjon på Internett om den engelske og den amerikanske støttegruppen for pasienter med Sticklers syndrom kan finnes under henholdsvis www.stickler.org.uk og www.sticklers.org. Kontakt med to norske familier som har barn med Sticklers syndrom kan formidles via førsteforfatter.
- 1.
Stickler GB, Belau PG, Farrell FJ, Jones JD, Pugh DG, Steinberg AG et al. Hereditary progressive arthro-ophtalmopathy. Mayo Clinic Proc 1965; 40: 433 – 55.
- 2.
Bennet J, McMurray SW. Sticklers syndrome. J Pediatr Orthop 1990; 10: 760 – 3.
- 3.
Admiraal RJ, Brunner HG, Dijkstra TL, Huygen PL, Cremers CW. Hearing loss in the non ocular Stickler syndrome caused by a COL11A2 mutation. Laryngoscope 2000; 110: 457 – 61.
- 4.
Nowak CB. Genetics and hearing loss: a review of Stickler syndrome. J Commun Disord 1998; 31: 437 – 54.
- 5.
Nielsen CE. Stickler’s syndrome. Acta Ophtalmol 1981; 59: 286 – 95.
- 6.
Snead MP, Yates JR. Clinical and molecular genetics of Stickler syndrome. J Med Genet 1999; 36: 353 – 9.
- 7.
Richards AJ, Martin S, Yates JRW, Scott JD, Baguley DM, Pope FM et al. COL2A1 exon 2 mutations: relevance to the Stickler and Wagner syndromes. Br J Ophtalmol 2000; 84: 364 – 71.
- 8.
Richards AJ, Baguley DM, Yates JR, Lane C, Nicol M, Harper PS et al. Variation in the vitreous phenotype of Stickler syndrome can be caused by different amino acid substitutions in the X position of the type II collagen Gly-X-Y triple helix. Am J Hum Genet 2000; 67: 1083 – 94.
- 9.
Brown DM, Vandenburgh K, Kimura AE, Weingeist TA, Sheffield VC, Stone EM. Novel frameshift mutations in procollagen 2 gene (COL2A1) associated with Stickler syndrome (hereditary arthro-ophtalmopathy). Hum Mol Genet 1995; 4: 141 – 2.
- 10.
Mendelian Inheritance in Man (MIM). www3.ncbi.nlm.nih.gov/OMIM/ (19.7.2001).
- 11.
Annunen S, Korkko J, Czarny M, Warman ML, Brunner HG, Kaariainen H et al. Splicing mutations of 54-bp exons in the COL11A1 gene cause Marshall syndrome, but other mutations cause overlapping Marshall/Stickler phenotypes. Am J Hum Genet 1999; 65: 974 – 83.
- 12.
Sirko-Osadsa DA, Zlotogora J, Tiller GE, Knowlton RG, Warman ML. A third Stickler syndrome locus is linked to COL11A1, the gene encoding the alpha-1 subunit of collagen XI. Abstrakt. Am J Hum Genet 1996; 59 (suppl): A17.
- 13.
Leiba H, Oliver M, Pollack A. Prophylactic laser photocoagulation in Stickler syndrome. Eye 1996; 10: 701 – 8.
- 14.
Sirko-Osadsa A, Murray MA, Scott JA, Lavery MA, Warman ML, Robin NH. Stickler syndrome without eye involvement is caused by mutations in COL11A2, the gene encoding the alpha2 (XI) chain type of collagen. J Pediatr 1998; 132: 368 – 71.
- 15.
Seery CM, Pruett RC, Liberfarb RM. Distinctive cataract in the Stickler syndrome. Am J Ophtalmol 1990; 110: 143 – 8.
- 16.
Brunner HG, van Beersum SE, Warman ML, Olsen BR, Ropers HH, Mariman EC. A Stickler syndrome gene is linked to chromosome 6 near the COL11A2 gene. Hum Mol Genet 1994; 9: 1561 – 4.
- 17.
Lewkonia RM. The arthropathy of hereditary arthroophtalmopathy (Stickler syndrome). J Rheumatol 1992; 19: 1271 – 5.
- 18.
Tomaski SM, Zalzal GH, Saal HM. Airway obstruction in the Pierre Robin sequence. Laryngoscope 1995; 105: 111 – 4.
- 19.
Trypman E. Osteochondritis dissecans of the knee in an adult with Stickler syndrome. Orthop Rev 1993; 22: 371 – 6.
- 20.
Tranebjærg L. Genetiske årsaker til hørselstap – status og perspektiver. Tidsskr Nor Lægeforen 1999; 113: 1919 – 24.
- 21.
Vintiner GM, Temple IK, Middleton-Price HR, Baraitser M, Malcolm S. Genetic and clinical heterogeneity of Stickler syndrome. Am J Med Genet 1991; 41: 44 – 8.
- 22.
Lieberfarb RM, Goldblatt A. Prevalence of mitral-valve prolapse in the Stickler syndrome. Am J Med Genet 1986; 24: 387 – 92.
- 23.
Zlotgora J, Sagi M, Schuper A, Leiba H, Merin S. Variability of Stickler syndrome. Am J Med Genet 1992; 42: 337 – 9.
- 24.
Wilkin DJ, Mortier GR, Johnson CL, Jones MC, de Paepe A, Shohat M et al. Correlation of linkage data with phenotype in eight families with Stickler syndrome. Am J Med Genet 1998; 80: 121 – 7.
- 25.
Wilkin DJ, Liberfarb R, Davis J, Levy HP, Cole WG, Francomano CA et al. Rapid determination of COL2A1 mutations in individuals with Stickler syndrome: analysis of potential premature termination codons. Am J Med Genet 2000; 94: 141 – 8.
- 26.
Zlotogora J, Granat M, Knowlton RG. Prenatal exclusion of Stickler syndrome. Prenat Diagn 1994; 14: 145 – 7.