Kreft i spiserøret er en alvorlig tilstand. Insidensen av sykdommen i Norge har vært omkring 3/100 000 for menn og i underkant av 1/100 000 for kvinner de siste årene (1). Tilstanden er likevel blant de ti hyppigste årsaker til dødsfall pga. kreft på verdensbasis og insidensen synes økende (2, 3). Særlig har økningen av adenokarsinom i oesophagus vært stor. En norsk studie har vist en årlig økning av slike adenokarsinomer i perioden 1983 – 92 på 17 % og 14 % hos henholdsvis menn og kvinner (4).
Overlevelse etter kirurgisk behandling av kreft i spiserøret har tradisjonelt vært lav. I Norge har femårsoverlevelsen vært lavere enn 20 %, selv for lokalisert sykdom (1).
Ved Rikshospitalet har vi erfaring med kirurgisk behandling av svulster i oesophagus. De siste fem-seks årene er imidlertid denne behandlingen blitt sentralisert til Det Norske Radiumhospital.
I denne artikkelen beskriver vi pasientgruppen nærmere ved å presentere et retrospektivt materiale av alle pasienter kirurgisk behandlet for kreft i oesophagus ved Rikshospitalet de siste åtte årene før sentraliseringen til Radiumhospitalet. Det er lagt særlig vekt på komplikasjoner relatert til inngrepet, ressursforbruk og overlevelse.
Materiale og metode
I alt 46 pasienter operert for kreft i oesophagus i tidsrommet 1987 – 94 ble inkludert i studien. Dette omfatter alle pasienter operert for denne tilstanden ved Rikshospitalet i den perioden som er undersøkt. Kjønnsfordelingen var 41 menn (89 %) og fem kvinner. Alderen var median 61 år (spredning 31 – 79 år). Preoperativ ASA (American Anaesthesiology Association Scoring System)-klassifikasjon av pasientene er vist i figur 1 og antall pasienter operert per år i tidsrommet undersøkt i figur 2.
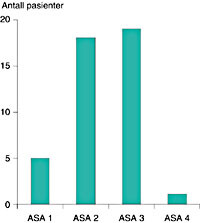
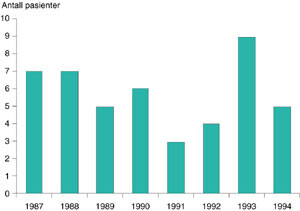
Preoperativ utredning bestod av øsofagogastroskopi med biopsi, computertomografi (CT) av øvre abdomen og mediastinum, og lungefysiologisk undersøkelse. I tillegg ble bronkoskopi utført hos de fleste pasientene. Tumor var plassert median 32 cm (spredning 22 – 40 cm) fra tannrekken målt ved endoskopi. Ni pasienter hadde tumor lokalisert nær cardia. Den histologiske inndelingen av svulstene er vist i tabell 1. Ni pasienter fikk preoperativ stråleterapi og tre pasienter preoperativ kjemoterapi. Alle disse pasientene hadde plateepitelkarsinom.
Tabell 1
Histologisk klassifikasjon av tumor
| Histologisk type |
Antall pasienter |
(%) |
| Plateepitelkarsinom |
23 |
(50) |
| Adenokarsinom |
20 |
(44) |
| Udifferensiert karsinom |
2 |
(4) |
| Leiomyosarkom |
1 |
(2) |
Pasientene ble operert med ulik kirurgisk tilgang. Vanligste tilgang var separat høyresidig torakotomi og laparotomi som ble utført hos 38 pasienter. Cervikolaparotomi ble utført hos fem pasienter. Hos en av disse pasientene ble tilgangen kombinert med sternotomi. Tre pasienter fikk utført cervikotorakolaparotomi. Type og teknikk for anastomose mellom proksimale oesophagus og magesekk/tarm er vist i tabell 2. Tre pasienter ble operert med coloninterponat mellom proksimale oesophagus og ventrikkel. Høyre colon med bibehold av tarmsegmentets egen blodforsyning ble benyttet. Fire pasienter hadde tumorinfiltrasjon i reseksjonsranden. En av disse pasientene hadde makroskopisk restvev av tumor. 20 av 30 pasienter med kjent lymfeknutestatus hadde metastaser til regionale lymfeknuter. I tillegg til reseksjon av tumor i oesophagus, fikk en pasient med en udifferensiert tumor resecert en solitær levermetastase. Hos en pasient ble fire trakealringer resecert pga. tumorvekst mot trachea. Anastomosen mellom proksimale oesophagus og tarm/ventrikkel ble rutinemessig undersøkt røntgenologisk med kontrast sjuende postoperative dag.
Tabell 2
Beskrivelse av anastomosene etter reseksjon. Anastomoselekkasje ved de ulike kirurgiske teknikkene er også angitt
| Antall |
Håndsydd/lekkasje |
EEA (maskin)/lekkasje |
|
| Øsofagogastrostomi |
32 |
18¹/3 |
14/2 |
| Øsofagojejunostomi (Roux-en-Y) |
11 |
9²/1 |
2/1 |
| Øsofagokolostomi |
3 |
3 |
|
| 46 |
30 |
16 |
|
| |||
Data er registrert retrospektivt ved journalgjennomgang. Perioperativ dødelighet er definert som død innen 30 dager eller før utskrivning fra avdelingen. Operasjonstid, antall døgn med behov for respirator og overvåking i intensivavdeling, samt total liggetid, er benyttet som indikatorer på ressursbehov i forbindelse med behandlingen. Pasientene ble utskrevet til rekonvalesens ved lokalsykehus.
Materialet ble gjort opp juli/august 2000. Fem års observasjonstid foreligger derfor for alle pasienter som har overlevd etter behandling. Observasjonstid hos pasienter i live er median 102 måneder (spredning 81 – 147 måneder). Beregning av overlevelse inkluderer perioperativ dødelighet og presenteres for hele materialet samlet og for de to største histologiske undergruppene separat. Analyser av overlevelse er utført ved hjelp av Kaplan-Meier-plott. Overlevelse mellom grupper er sammenliknet ved logranktest.
Resultater
Operasjonstid, definert som tiden fra kirurgen startet inngrepet til kirurgen avsluttet, var median sju timer (spredning 4 – 15 timer). Peroperativ blødning var median 1 000 ml (spredning 400 – 5 600 ml) og antall enheter peroperativ blodtransfusjon (SAG) var median tre enheter (spredning 0 – 17 enheter). 39 pasienter fikk blodtransfusjon peroperativt.
Åtte pasienter ble reoperert på grunn av postoperative komplikasjoner, fire pga. anastomoselekkasje, en pga. øsofagopleural fistel, en pga. trakeoøsofageal fistel, en for anleggelse av ernæringssonde, og en pasient ble reoperert for sårruptur etter overflytting til lokalsykehus. Til sammen utviklet sju pasienter anastomoselekkasje, hvorav tre ble behandlet konservativt. Øvrige postoperative komplikasjoner er vist i tabell 3. Perioperativ dødelighet var 13 % (seks pasienter). Dødsårsakene var sepsis hos fire pasienter, respirasjonssvikt hos en pasient og styrtblødning fra a. anonyma til trachea hos en pasient.
Tabell 3
Postoperative komplikasjoner
| Komplikasjoner |
Antall |
(%) |
| Alvorlige komplikasjoner |
17 |
(37) |
| Reoperasjon |
8 |
(17) |
| Trakeostomi |
7 |
(15) |
| Anastomoselekkasje |
7 |
(15) |
| Sepsis |
6 |
(13) |
| Død |
6 |
(13) |
| Hjertestans (resuscitert) |
1 |
(2) |
| Kolotrakeal fistel |
1 |
(2) |
| Andre komplikasjoner |
17 |
(37) |
| Pneumoni |
15 |
(33) |
| Venstresidig rekurrens- parese |
1 |
(2) |
| Pleuravæske tappet |
2 |
(4) |
| Elektrokonvertert atrieflimmer |
1 |
(2) |
| Hjertesvikt |
1 |
(2) |
| Aspirasjon med komplikasjoner |
2 |
(4) |
| Sårinfeksjon |
2 |
(4) |
Ti pasienter ble respiratorbehandlet mer enn ti døgn postoperativt og sju pasienter ble trakeostomert. Mediant antall intensivdøgn var åtte (spredning 2 – 50 døgn); ni pasienter hadde behov for mer enn 20 intensivdøgn. Liggetid i avdelingen inkludert opphold ved intensivavdelingen var median 18 døgn (spredning 7 – 54 døgn), 11 pasienter var innlagt mer enn 30 døgn.
Median overlevelse for hele gruppen var 11 måneder (spredning 0 – 146 måneder). Tre- og femårsoverlevelse var henholdsvis 22 % og 15 %. Sju pasienter har levd mer enn fem år postoperativt. For pasienter med adenokarsinom var median overlevelse 18 måneder (spredning 0,5 – 146 måneder) og tre- og femårsoverlevelse henholdsvis 30 % og 20 % (fig 3). Tilsvarende var median overlevelse for pasienter med plateepitelkarsinom ni måneder (spredning 2 – 138 måneder) og tre- og femårsoverlevelse 18 % og 14 % (fig 3). Forskjellen i overlevelse mellom pasienter med adenokarsinom og plateepitelkarsinom var ikke signifikant (p = 0,34).
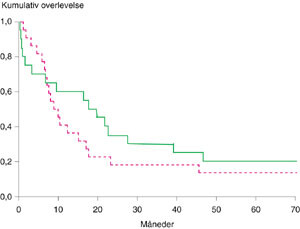
Diskusjon
Kirurgisk behandling av kreft i spiserøret er ressurskrevende. Mange pasienter utvikler alvorlige komplikasjoner med behov for lange opphold ved intensivavdeling og sengepost. Dette medfører et stort ressursforbruk og krever god tilgang på intensivplass. Selve inngrepet er også ressurskrevende, og i de fleste tilfeller må operasjonsstue og personale reserveres en hel dag.
Operativ tilgang for reseksjon av oesophagus varierer. En klassisk tilnærming er en kombinasjon av torakotomi og laparotomi som ble utført hos 83 % av pasientene i vår studie. En annen tilgang er transhiatal reseksjon av tumor hvor man unngår torakotomi og i stedet legger anastomosen på halsen. Noen hevder at torakotomi gir bedre tilgang i mediastinum for disseksjon av lymfeknuter, og dermed et bedre resultat (5). Andre finner ingen forskjell i overlevelse mellom de to teknikkene (6). Radikal eller trefelts lymfadenektomi beskrevet i japanske studier, synes å gi bedre overlevelse sammenliknet med mindre omfattende disseksjon av lymfeknuter (7, 8). Slik radikal disseksjon ble ikke benyttet hos våre pasienter hvor disseksjonen stort sett var begrenset til mediastinum.
Coloninterponat ble benyttet ved hjelp av høyre colon hos tre pasienter. Indikasjonen for å benytte interponat var tidligere ventrikkelreseksjon og/eller høy lokalisasjon av tumor i oesophagus. En av disse pasientene utviklet fistel til trachea.
Høy komplikasjonsrate og dødelighet er dokumentert etter reseksjon av oesophagus (9, 10). Dødeligheten hos pasienter operert ved vår avdeling var også høy, men sammenliknbar med andre studier (9 – 12). I en undersøkelse av mer enn 11 000 pasienter operert mellom 1990 og 1995 var dødeligheten i sykehus 11 % (12). Sentre som utfører denne type inngrep hyppig har imidlertid rapportert redusert dødelighet med årene. Dette skyldes bl.a. bedre kirurgisk erfaring og reduksjon av lungekomplikasjoner, som har vært en hyppig dødsårsak (5).
Overlevelse hos pasientene inkludert i vårt materiale presenteres samlet uavhengig av stadieinndeling. Dette begrunnes delvis med at studien er retrospektiv og at vi ikke har hatt standardiserte kriterier for identifikasjon av lymfeknuter i resektatet. I tillegg er pasientmaterialet relativt lite og inndeling av pasientene i undergrupper gir dårlig beskrivelse av overlevelse i de enkelte gruppene. Studien gir derfor kun et inntrykk av overlevelse og det ressursforbruk man må kunne forvente hos hele pasientgrupper uavhengig av stadieinndeling.
TNM-stadieinndeling og spesielt lymfeknutemetastasering er, sammen med fullstendig makroskopisk og mikroskopisk reseksjon av tumor (R0-reseksjon), de viktigste prognostiske faktorer etter reseksjon av kreft i oesophagus (3, 13, 14). Metastaser til regionale lymfeknuter forekom hos to tredeler av pasientene med kjent lymfeknutestatus i vår studie, og dette har hatt stor betydning for den samlede overlevelse som presenteres. Slik metastasering er vanskelig å avsløre preoperativt til tross for bedre bildediagnostikk med årene (15). Studier pågår for å undersøke eventuell nytte av torakoskopisk og laparoskopisk stadiebestemmelse av disse pasientene før behandling (14).
Overlevelse etter kirurgi for kreft i oesophagus har tradisjonelt vært lav og varierer mellom 25 % og 40 % avhengig av om overlevelse presenteres samlet eller relatert til TNM-stadium (2, 9). Den synes imidlertid å ha blitt bedre med årene (1). Flere studier viser overlevelse sammenliknbar med resultatene fra vårt materiale (2, 16). Våre resultater er også i samsvar med data fra Kreftregisteret i perioden 1989 – 93.
Ni pasienter med plateepitelkarsinom fikk preoperativ strålebehandling og tre pasienter fikk preoperativ kjemoterapi. For flere av disse pasientene var dette som del av en skandinavisk studie av kreft i oesophagus. Denne studien viste bedre treårsoverlevelse hos pasienter som fikk preoperativ strålebehandling, men ingen forskjell i overlevelse som resultat av preoperativ kjemoterapi (17). En metaanalyse publisert senere har imidlertid ikke påvist signifikant effekt av preoperativ strålebehandling hos pasienter med plateepitelkarsinom i oesophagus (18).
Kirurgisk behandling av kreft i spiserøret er et relativt sjeldent inngrep. Ved Rikshospitalet ble det i perioden 1987 – 94 operert (median) 5 – 6 pasienter per år med denne diagnosen. Dette medfører at erfaring i kirurgisk teknikk, perioperativ behandling og oppfølging av komplikasjoner, blir begrenset ved den enkelte avdeling (5, 19, 20). Sentralisering av denne type behandling er derfor nødvendig. Behandlingen kan være meget ressurskrevende og påvirker dermed den enkelte avdelings kapasitet. Dette har betydning for avdelingens øvrige elektive program ikke minst dersom avdelingen også har stor pågang av akutte inngrep.
- 1.
Kreftregisteret. www.kreftregisteret.no (18.7.2001).
- 2.
Lerut T, Coosemans W, De Leyn P, Van Raemdonck D, Deneffe G, Decker G. Treatment of esophageal carcinoma. Chest 1999; 116 (suppl); 463 – 5.
- 3.
Rudiger FJ, Feith M, Werner S, Hubert J. Adenocarcinoma of the esophagogastric junction. Results of surgical therapy based on anatomical/topographic classification in 1,002 consecutive patients. Ann Surg 2000; 232: 353 – 61.
- 4.
Hansen S, Wiig JN, Gierscky KE, Tretli S. Esophageal and gastric carcinoma in Norway 1958 – 1992: incidence time trend variability according to morphological subtypes and organ subsites. Int J Cancer 1997; 71: 340 – 4.
- 5.
Whooley BP, Law SMB, Murthy SC, Alexandrou A, Wong J. Analysis of reduced death and complication rates after esophageal resection. Ann Surg 2001; 233: 338 – 44.
- 6.
Boyle MJ, Franceschi D, Liningstone AS. Transhiatal versus transthoracic esophagectomy: complication and survival rates. Am Surg 1999; 65: 1137 – 41.
- 7.
Isono K, Sato H, Nakayama K. Results of a nationwide study on the three field lymph node dissection of esophageal cancer. Oncology 1991; 48: 411 – 20.
- 8.
Fujita H, Kakegawa T, Yamana H, Shima I, Toh Y, Tomota Y et al. Mortality and morbidity rates, postoperative course, quality of life, and prognosis after extended radical lymphadenectomy for esophageal cancer. Comparison of three – field lymphadenectomy with two-field lymphadenectomy. Ann Surg 1995; 222: 654 – 62.
- 9.
Graadal Ø, Stadaas J. Cancer oesophagi og cardiae ventriculi – kirurgisk behandling. Tidsskr Nor Lægeforen 1986; 106: 389 – 91.
- 10.
Roald HE, Harbitz TB. Cancer oesophagi. Tidsskr Nor Lægeforen 1991; 111: 2549 – 52.
- 11.
Muller JM, Erasmi H, Stelzer M, Zieren U, Pichlmaier H. Surgical therapy of oesophageal carcinoma. Br J Surg 1990; 77: 845 – 57.
- 12.
Jamieson GG, Mathew G. Surgical management of esophageal cancer: the Western experience. I: Daly JM, Hennessy TPJ, Reynolds JV, red. Management of upper gastrointestinal cancer. London: Saunders, 1999: 183 – 99.
- 13.
Ellis FH jr., Heatley GJ, Krasna MJ, Williamson WA, Balogh K. Esophagogastrectomy for carcinoma of the esophagus and the cardia: a comparison of findings and results after standard resection in three consecutive eight-year intervals with improved staging criteria. J Thorac Cardiovasc Surg 1997; 113: 836 – 48.
- 14.
Krasna MJ. Surgical staging and surgical treatment in esophageal cancer. Semin Oncol 1999; 26: 9 – 11.
- 15.
Sodnenaa K, Skaane P, Nygaard K, Skjennald A. Value of computed tomography in preoperative evaluation of resectability and staging in esophageal carcinoma. Eur J Surg 1992; 158: 537 – 40.
- 16.
Watson A. Operable esophageal cancer: current results from the West. World J Surg 1994; 18: 361 – 6.
- 17.
Nygaard K, Hagen S, Hansen HS, Hatlevoll R, Hultborn R, Jakobsen A et al. Preoperative radiotherapy prolongs survival in operable esophageal carcinoma: a randomized, multicenter study of preoperativ radiotherapy and chemotherapy. The second Scandinavian trial in esophageal cancer. World J Surg 1992; 16: 1104 – 9.
- 18.
Arnott SJ, Duncan W, Gignoux M, Girling DJ, Hansen HS, Launois B et al. Preoperative radiotherapy in esophageal carcinoma: a metaanalysis using individual patient data (Oesophageal Cancer Collaborative Group). Int J Rad Oncol Biol Phys 1998; 41: 579 – 83.
- 19.
Swisher SG, Deford L, Merriman KW, Walsh GL, Smythe R, Vaporicyan A et al. Effect of operative volume on morbidity, mortality, and hospital use after esophagectomy for cancer. J Thorac Cardiovasc Surg 2000; 119: 1126 – 34.
- 20.
Pasientvolum og behandlingskvalitet. Senter for Medisinsk Metodevurdering, rapport nr. 2/2001. Oslo: Sintef-Unimed, 2001.