Artikkelen publiseres også i Den norske tannlegeforenings Tidende 2002; 112: 212 – 4.
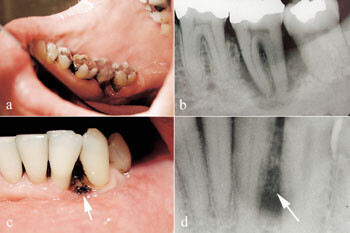
HIV-infeksjon er forbundet med høyere forekomst av spesielle former for gingivale og periodontale sykdommer som sjelden opptrer hos systemisk friske personer: lineært gingivalt erytem, nekrotiserende ulcerøs gingivitt og periodontitt (1 – 4). Nekrotiserende periodontale sykdommer (fig 1) er funnet å være assosiert med graden av pasientens immunsvikt – prevalensen i asymptomatiske HIV-positive pasienter er lav (< 0,5 %), men kan stige opp mot 10 % med progrediering av HIV-infeksjonen (5 – 7).
Flere studier har vist at HIV-positive pasienter har økt mottakelighet for kroniske gingivale og periodontale sykdommer sammenliknet med HIV-negative personer (4). Prevalensen av periodontalt festetap (tap av tannens støttevev), lommedanning, blødning og suppurasjon er høyere hos HIV-positive pasienter enn hos HIV-negative personer (3 – 4, 8 – 9). Progredieringen av preeksisterende periodontitt er funnet å være signifikant raskere hos HIV-positive pasienter, noe som ble vist i en longitudinell studie av Yeung og medarbeidere i 1993 (10). Periodontalt festetap er også mer markert og avansert i de senere stadier av HIV-infeksjonen (4 – 8, 11, 12). Lavt antall CD4-positive T-lymfocytter i perifert blod har også vist seg å være signifikant assosiert med periodontalt festetap og dets utstrekning og alvorlighetsgrad (3 – 4, 9).
Pasienten. En 38 år gammel mann ble i april 1999 henvist til Avdeling for periodonti ved Det odontologiske fakultet i Oslo fra sin private tannlege på grunn av nekrotiske og ulcerøse periodontale lesjoner (fig 1). Den kliniske undersøkelsen avdekket foruten nekrotiske periodontale lesjoner også at pasienten hadde oral candidiasis (pseudomembranøs type). Munnhygienen var god, det var ikke synlig dentalt plakk. I den videre anamnesen fortalte han at han i 1995 hadde hatt et utbrudd med herpes zoster, og at han var til behandling ved Aker sykehus for idiopatisk trombocytopenisk purpura på henvisningstidspunktet. Denne diagnosen hadde han hatt siden januar 1998 og ble for dette medisinert med immunsuppressive medikamenter (Prednisolon og Imurel). Han hadde gjennomgått en splenektomi, da trombocytopenien ikke bedret seg til tross for medisineringen.
Periodontalt og oralt ble den akutte situasjonen behandlet med subgingival tannrengjøring kombinert med metronidazol (500 mg No 30) og en mykostatinkur (100 000 IE/ml: 1 ml 4 ganger daglig i fire uker).
På grunn av det uvanlige kliniske bildet ble han henvist videre til HIV-testing, som viste at pasienten var HIV-positiv. Han begynte med antiretroviral terapi, og antall CD4-positive og CD8-positive T-lymfocytter i perifert blod økte fra nær null til over 500 per mm³ blod, og HIV-RNA-verdiene ble redusert. Trombocyttallet økte til normale verdier. Hans orale candidiasis forsvant.
Pasienten er i dag til månedlige kontroller og oppfølging ved Avdeling for periodonti. De orale, gingivale og periodontale forhold er relativt stabile.
Diskusjon
Sykehistorien er et klassisk eksempel på HIV-assosiert nekrotisk periodontitt, og viser hvor viktig det er at legen og tannlegen kjenner til orale symptomer på HIV-infeksjon. Oral candidiasis er en vanlig forekommende infeksjon hos HIV-positive pasienter. Prevalensen av oral candidiasis øker med fallende antall CD4-positive T-lymfocytter og er hyppigst i senere stadier av HIV-infeksjonen. Splenektomien og den immunsuppressive behandling som pasienten fikk på grunn av sin trombocytopeni kan ha bidratt til utviklingen av oral candidiasis og nekrotisk periodontitt. Candida albicans, som er det vanligste etiologiske agens for oral candidiasis, har vært foreslått som mulig årsak til lineært gingivalt erytem og nekrotisk periodontitt hos HIV-positive pasienter (6, 7). Splenektomi og bivirkninger fra immunsuppressiv behandling (f.eks. leukopeni og trombocytopeni) kan ha ført til økt mottakelighet overfor infeksjoner. Det er derfor mulig at dette fremskyndet utviklingen av disse HIV-assosierte infeksjonene.
Pasientens orale candidiasis forsvant etter oppstart av antifungal behandling med mykostatin, men dette kan også ha vært en direkte følge av den antivirale behandlingen.
Pasientens tidligere utbrudd av herpes zoster i 1995 kan også ha vært HIV-assosiert. Hans immunstatus ved diagnosetidspunktet tydet på en langtkommet HIV-infeksjon, og herpes zoster opptrer ofte hos immunsupprimerte personer.
Antall CD4-positive T-lymfocytter i perifert blod viste at vår pasient hadde en langt fremskreden HIV-infeksjon. Med< 200 CD4-positive T-lymfocytter per mm³ blod skulle han etter CDC-klassifiseringen for HIV-infeksjon klassifiseres som AIDS-syk (13), men ikke etter gjeldende norske kriterier. Nekrotisk periodontitt og oral candidiasis, begge aktuelle markører for progrediering av HIV-infeksjon til AIDS, tyder også på en langt fremskreden HIV-infeksjon.
Trombocytopeni er en kjent følgetilstand til HIV-infeksjon (14). HIV-assosiert trombocytopeni kan skyldes at HIV infiserer megakaryocytter i beinmargen, noe som hemmer danningen av trombocytter fra disse cellene (14, 15). Antiviral terapi har vist seg å øke antall trombocytter hos pasienter med HIV-assosiert trombocytopeni (14, 15). Dette skjer trolig ved at mengden virus reduseres og at færre megakaryocytter infiseres. Det kan forklare økningen i trombocytter hos vår pasient etter oppstart av antiviral behandling.
Man kan i ettertid spekulere på om pasientens HIV-infeksjon burde vært avslørt tidligere under behandlingen av trombocytopenien, særlig fordi han tilhørte en kjent risikogruppe for HIV-infeksjon. En tidligere oppstart med antiviral behandling kunne utsatt eller i beste fall hindret pasienten i å utvikle nekrotisk periodontitt og oral candidiasis.
Pasienten hadde et meget lavt antall CD4-positive T-lymfocytter i perifert blod da han ble henvist til Avdeling for periodonti med nekrotisk periodontitt og oral candidose. Dette er sammenfallende med tidligere rapporter, hvor lavt antall CD4-positive T-lymfocytter er assosiert med alvorlighetsgrad og progrediering av periodontitt (3 – 5, 9, 11). Klinisk hadde vår pasient et horisontalt festetap uten dype beinlommer (fig 1), noe som stemmer overens med nekrotisk periodontitt (2).
Vi har i våre studier funnet at HIV-positive pasienter med kronisk marginal periodontitt har et inflammatorisk celleinfiltrat i inflammert gingiva som ikke bare er fokusert mot periodontallommens bunn, men også mot oralt epitel (16 – 20). Det var også en signifikant økning i antall makrofager, mastceller, nøytrofile granulocytter og plasmaceller hos HIV-positive med periodontitt sammenliknet med HIV-negative pasienter (16 – 20). Den store økningen i antall leukocytter og den uvanlige lokaliseringen var uavhengig av stadium i HIV-infeksjonen. Det er mulig at en slik utbredelse av celleinfiltratet kan predisponere for nekrotisk periodontitt hos denne pasientgruppen. En massiv frigjøring av potente vevsdestruktive mediatorer kan forårsake det horisontale festetapet som ofte sees hos HIV-positive pasienter (fig 1) (16 – 20). Det siste kan tenkes skje ved bortfall av funksjonelle CD4-positive T-lymfocytter, som er viktige regulatorceller i immunforsvaret, og kan forklare den observerte korrelasjonen mellom lavt antall CD4-positive T-lymfocytter og nekrotisk periodontitt hos denne pasientgruppen.
- 1.
Winkler JR. Periodontal disease associated with HIV infection. Oral Surg Oral Med Oral Pathol Oral Radiol Endod 1992; 73: 145 – 50.
- 2.
Holmstrup P. Periodontal diseases in HIV-infected parients. J Clin Periodontol 1994; 21: 270 – 80.
- 3.
Robinson PG. Which periodontal changes are associated with HIV infection? J Clin Periodontol 1998; 25: 278 – 85.
- 4.
Narani N, Epstein JB. Classifications of oral lesions in HIV infection. J Clin Periodontol 2001; 28: 137 – 45.
- 5.
Masouredis CM, Katz MH, Greenspan D, Herrera C, Hollander H, Greenspan JS et al. Prevalence of HIV-associated periodontitis and gingivitis in HIV-infected patients attending an AIDS clinic. J AIDS 1992; 5: 479 – 83.
- 6.
Lamster IB, Grbic JT, Bucklan RS, Mitchell-Lewis D, Reynolds HS, Zambon JJ. Epidemiology and diagnosis of HIV-associated periodontal diseases. Oral Dis 1997; 3 (suppl 1): 141 – 8.
- 7.
Lamster IB, Grbic JT, Mitchell-Lewis D, Begg MD, Mitchell A. New concepts regarding the pathogenesis of periodontal disease in HIV infection. Annals of Periodontology 1998; 3: 62 – 75.
- 8.
Smith GL, Cross DL, Wray D. Comparison of periodontal disease in HIV seropositive subjects and controls (I). Clinical features. J Clin Periodontol 1995; 22: 558 – 68.
- 9.
Robinson PG, Sheiham A, Challacombe SJ, Zakrzewska JM. The periodontal health of homosexual men with HIV infection: a controlled study. Oral Dis 1996; 2: 45 – 52.
- 10.
Yeung SC, Stewart GJ, Cooper DA, Sindhusake D. Progression of periodontal disease in HIV seropositive patients. J Periodontol 1993; 64: 651 – 7.
- 11.
Barr C, Lopez MR, Rua-Dobles A. Periodontal changes by HIV serostatus in a cohort of homosexual and bisexual men. J Clin Periodontol 1992; 19: 794 – 801.
- 12.
Tomar SL, Swango PA, Kleinman DS, Burt BA. Loss of periodontal attachment in HIV-seropositive military personnel. J Periodontol 1995; 66: 421 – 8.
- 13.
CDC. 1993 Revised classification system for HIV infection and expanded surveillance case definition for AIDS among adolescents and adults. MMWR Morb Mortal Wkly Rep 1992; 41: 17.
- 14.
Northfelt DW. Hematologic aspects of HIV infection. I: Cohen PT, Sande MA, Volberding PA, red. The AIDS knowledge base. 3. utg. San Francisco, CA: Lippincott, Williams & Wilkins, 1999: 505 – 14.
- 15.
Louache F, Bettaieb A, Henri A, Oksenhendler E, Farcet JP, Bierling P et al. Infection of megakaryocytes by human immunodeficiency virus in seropositive patients with immune thrombocytopenic purpura. Blood 1991; 78: 1697 – 705.
- 16.
Myint M, Odden K, Schreurs O, Halstensen TS, Schenck K. The gingival plasma cell infiltrate in HIV-positive patients with periodontitis is disorganized. J Clin Periodontol 1999; 26: 358 – 65.
- 17.
Aboulafia DM, Bundow D, Waide S, Bennet C, Kerr D. Initial observations on the efficacy of highly active antiretroviral therapy in the treatment of HIV-associated autoimmune thrombocytopenia. Am J Med Sci 2000; 320: 117 – 23.
- 18.
Myint M, Steinsvoll S, Yuan ZN, Johne B, Helgeland K, Schenck K. Highly increased numbers of leukocytes in inflamed gingiva from patients with HIV infection. AIDS 2002; 16: 235 – 43.
- 19.
Næsse EP, Schreurs O, Helgeland K, Schenck K, Steinsvoll S. Mast cells – mediators of periodontal tissue destruction in HIV+ patients? J Dent Res 2001; 80 (Special Issue): 770.
- 20.
Steinsvoll S, Myint MM, Helgeland K, Schenck K. Aberrant distribution of leukocytes in periodontal lesions of HIV+ patients. J Dent Res 2001; 80 (Special Issue): 744.